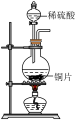
1 . 亚硝酸钠( )是一种白色结晶状粉末,易溶于水,易被氧化,可用作织物染色的媒染剂、漂白剂等;工业制取亚硝酸钠晶体的基本流程如图所示。现设计相关实验测定其产品纯度。
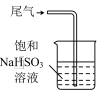
)是一种白色结晶状粉末,易溶于水,易被氧化,可用作织物染色的媒染剂、漂白剂等;工业制取亚硝酸钠晶体的基本流程如图所示。现设计相关实验测定其产品纯度。 溶液从设备顶部以雾状喷下吸收从底部通入的尾气,其优点是:
溶液从设备顶部以雾状喷下吸收从底部通入的尾气,其优点是:_____ 。
(2)还原:若硝酸在“还原”阶段只生成 ,则氧化剂与还原剂的物质的量之比为:
,则氧化剂与还原剂的物质的量之比为:____ 。
(3)测定产品中 纯度。实验操作如下:
纯度。实验操作如下:
ⅰ.用电子天平称取7.500g样品,配成500mL样品溶液。
ⅱ.向锥形瓶中准确移入50.00mL样品溶液,滴加适量的 溶液酸化,加热至40~50℃,冷却后,用0.10
溶液酸化,加热至40~50℃,冷却后,用0.10
 溶液进行滴定(已知:
溶液进行滴定(已知: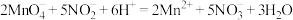 ),至恰好完全反应,消耗
),至恰好完全反应,消耗 溶液40.00mL。
溶液40.00mL。
ⅲ.重复滴定三次。
①测定时操作时间不宜过长,否则测定的结果将会___________ (填“偏大”或“偏小”)。
②该亚硝酸钠晶体产品中可能含有的杂质有:___________ 、 和
和 。
。
③试计算产品中 纯度(即
纯度(即 的质量分数)是
的质量分数)是___________ (写出计算过程)。
 )是一种白色结晶状粉末,易溶于水,易被氧化,可用作织物染色的媒染剂、漂白剂等;工业制取亚硝酸钠晶体的基本流程如图所示。现设计相关实验测定其产品纯度。
)是一种白色结晶状粉末,易溶于水,易被氧化,可用作织物染色的媒染剂、漂白剂等;工业制取亚硝酸钠晶体的基本流程如图所示。现设计相关实验测定其产品纯度。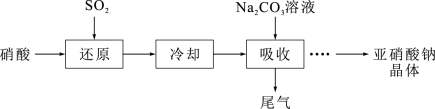
 溶液从设备顶部以雾状喷下吸收从底部通入的尾气,其优点是:
溶液从设备顶部以雾状喷下吸收从底部通入的尾气,其优点是:(2)还原:若硝酸在“还原”阶段只生成
 ,则氧化剂与还原剂的物质的量之比为:
,则氧化剂与还原剂的物质的量之比为:(3)测定产品中
 纯度。实验操作如下:
纯度。实验操作如下:ⅰ.用电子天平称取7.500g样品,配成500mL样品溶液。
ⅱ.向锥形瓶中准确移入50.00mL样品溶液,滴加适量的
 溶液酸化,加热至40~50℃,冷却后,用0.10
溶液酸化,加热至40~50℃,冷却后,用0.10
 溶液进行滴定(已知:
溶液进行滴定(已知: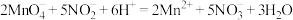 ),至恰好完全反应,消耗
),至恰好完全反应,消耗 溶液40.00mL。
溶液40.00mL。ⅲ.重复滴定三次。
①测定时操作时间不宜过长,否则测定的结果将会
②该亚硝酸钠晶体产品中可能含有的杂质有:
 和
和 。
。③试计算产品中
 纯度(即
纯度(即 的质量分数)是
的质量分数)是
您最近一年使用:0次
2023-12-22更新
|
202次组卷
|
2卷引用: 江苏省盐城市2023-2024学年高二学业水平合格性考试模拟预测化学试题
2022高三·全国·专题练习
名校
解题方法
2 . 下列关于 的实验,能达到实验目的的是
的实验,能达到实验目的的是
 的实验,能达到实验目的的是
的实验,能达到实验目的的是
|
|
|
|
A.制取 | B.验证漂白性 | C.收集 | D.尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-16更新
|
712次组卷
|
26卷引用:2023年江苏省扬州市普通高中学业水平合格性模拟试卷(二)化学试题
2023年江苏省扬州市普通高中学业水平合格性模拟试卷(二)化学试题江苏省扬州市宝应县2021-2022学年高二上学期期中检测化学(必修)试题(已下线)化学(江苏A卷)-学易金卷:2023年高考第一次模拟考试卷江苏省苏州市第三中学校2022-2023学年高一上学期12月采点评价考试化学试题江苏省徐州市铜山区2022-2023学年高一下学期期中化学(合格考)试题江苏省宿迁市2022-2023学年高一下学期6月期末化学试题(已下线)综合期末压轴85+18题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)(已下线)微专题21 二氧化硫性质四重性探究-备战2023年高考化学一轮复习考点微专题(已下线)第13讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)山东省潍坊瀚声学校2021-2022学年高一下学期4月月考化学试题河北省廊坊市三河市第三中学2021-2022学年高一下学期5月线上考试化学试题湖南省湘阴县知源高级中学2022-2023学年高三上学期第二次月考化学试题(已下线)专题十五化学实验基础上海市华东师范大学附属周浦中学2022-2023学年高一上学期教学质量检测化学试卷河南省郑州市第七高级中学2022-2023 学年高一上学期期末考试化学试题湖南省株洲市第一中学2022-2023学年高三上学期第五次月考化学试题(已下线)5.1.1 硫及其氧化物——同步学习必备知识第四章 非金属及其化合物 第20讲 硫及其氧化物天津市河北区2022- 2023学年高三上学期期末质量检测(线下考试)化学试题陕西省西安市大联考2022-2023学年高一下学期4月期中考试化学试题吉林省长春市第八中学2022-2023学年高一下学期4月考试化学试题云南省宣威市第三中学2022-2023学年高一下学期第三次月考化学试题广东省清远市博爱学校2021-2022学年高一下学期第一次教学质量检测化学试题福建省莆田华侨中学2022-2023学年高一上学期期末考试化学试题北京市第二中学2022-2023学年高一下学期期末考试化学试题北京工业大学附属中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
3 . 用 和
和 可以合成甲醇。其主要反应为
可以合成甲醇。其主要反应为
反应I
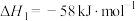
反应Ⅱ
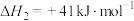
在恒容密闭容器内,充入1mol 和3mol
和3mol  ,测得平衡时
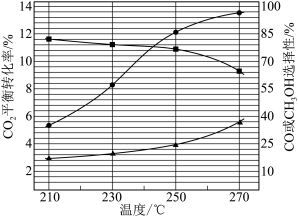
,测得平衡时 转化率,CO和
转化率,CO和 选择性随温度变化如图所示[选择性
选择性随温度变化如图所示[选择性 ]。
]。
 和
和 可以合成甲醇。其主要反应为
可以合成甲醇。其主要反应为反应I

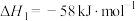
反应Ⅱ

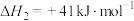
在恒容密闭容器内,充入1mol
 和3mol
和3mol  ,测得平衡时
,测得平衡时 转化率,CO和
转化率,CO和 选择性随温度变化如图所示[选择性
选择性随温度变化如图所示[选择性 ]。
]。
| A.270℃时主要发生反应Ⅱ |
| B.230℃下缩小容器的体积,n(CO)不变 |
C.250℃下达平衡时, |
D.其他条件不变,210℃比230℃平衡时生成的 多 多 |
您最近一年使用:0次
2023-02-14更新
|
1489次组卷
|
6卷引用:江苏省南通市如东中学,如东一高等四校2023-2024学年高三上学期12月学情调研化学试题
江苏省南通市如东中学,如东一高等四校2023-2024学年高三上学期12月学情调研化学试题江苏省南通市2023届高三第一次调研测试(一模)化学试题江苏省镇江第一中学2022-2023学年高二下学期学情检测调研(2)化学试题江苏省泰州市靖江高级中学2023-2024学年高二下学期4月期中考试化学试题(已下线)素养卷04 化学反应速率与平衡图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题14 化学反应速率和化学平衡
名校
解题方法
4 . 下列关于各物质用途的解释不正确 的是
| 选项 | 用途 | 解释 |
| A |  用作制冷剂 用作制冷剂 |  极易溶于水 极易溶于水 |
| B | 氧化铝用作耐火材料 | 氧化铝熔点高 |
| C | 铁粉用作食品的抗氧化剂 | 铁粉具有还原性 |
| D |  用作供氧剂 用作供氧剂 |  与水及 与水及 等反应产生 等反应产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-06更新
|
758次组卷
|
5卷引用:江苏省盐城市2022-2023学年高二上学期学业水平合格性考试模拟检测化学试题
名校
5 . 目前国际空间站处理CO2废气涉及的反应为CO2+4H2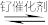 CH4+2H2O。下列关于该反应的说法正确的是
CH4+2H2O。下列关于该反应的说法正确的是
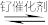 CH4+2H2O。下列关于该反应的说法正确的是
CH4+2H2O。下列关于该反应的说法正确的是| A.升高温度能减慢该反应的速率 |
| B.钌催化剂能加快该反应的速率 |
| C.达到平衡时,v(正)=v(逆)=0 |
| D.达到平衡时,CO2能100%转化为CH4 |
您最近一年使用:0次
2021-03-24更新
|
836次组卷
|
19卷引用:2016-2017学年江苏省盐城市高二学业水平模拟(一)化学试卷
2016-2017学年江苏省盐城市高二学业水平模拟(一)化学试卷2016-2017学年江苏省江阴市四校高一下学期期中考试化学试卷【校级联考】江苏省七校联盟2018-2019学年高二上学期期中联考化学试题江苏省南通市启东市吕四中学2019-2020学年高二下学期期初考试化学试题江苏省淮安市盱眙中学2020-2021学年高一下学期第一次学情调研化学试题江苏省仪征中学2020-2021学年高一下学期4月学情检测化学试题福建省永安市第三中学2020-2021学年高二10月月考化学(学考班)试题广东省广大附中、铁一、广外三校2020-2021学年高一下学期期中联考化学试题广东省广州市玉岩中学2020-2021学年高一下学期期中考试化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)安徽省宣城市七校2021-2022学年高一下学期期中联考化学试卷广东省深圳外国语学校2021-2022学年高一下学期期中考试化学试题江西省九江市五校2021-2022学年高一下学期期末测试化学试题天津市第二十一中学2022-2023学年高一下学期期中考试化学试题广东省广州市第七中学2022-2023学年高一下学期期中考试化学试题广东省江门市蓬江区三校2020-2021学年高一下学期期中联考化学试题内蒙古自治区包头市2022-2023学年高一下学期期末考试化学试题河南省济源高级中学2023-2024学年高二上学期开学考试 化学试题广东省广州市第七中学2023-2024学年高一下学期5月期中考试化学试题
11-12高一上·黑龙江绥化·期末
名校
解题方法
6 . 向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液变成红色,则下列结论错误 的是
| A.该溶液中一定含有SCN- | B.氧化性:Fe3+>Cl2 |
| C.Fe2+与SCN-不能形成红色物质 | D.Fe2+被氧化为Fe3+ |
您最近一年使用:0次
2020-08-23更新
|
986次组卷
|
25卷引用:2010—2011学江苏省扬州中学高二学业水平测试考前练习化学试卷
(已下线)2010—2011学江苏省扬州中学高二学业水平测试考前练习化学试卷(已下线)2010-2011学年黑龙江省庆安县第三中学高一上学期期末考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷2014-2015学年山东省菏泽市高一下学期期终考试化学试卷2016-2017学年江西省南昌市第十中学高一下学期分班考试化学试卷云南省景谷一中2018-2019学年高一下学期期末考试化学试题(已下线)2019年8月5日《每日一题》2020年高考一轮复习—— Fe2+、Fe3+的检验黑龙江省安达市第七中学2019-2020学年高一上学期月考化学试题山西省应县第一中学校2019-2020学年高一上学期第四次月考化学试题广西河池市都安县第二高级中学2019-2020学年高一上学期期末考试化学试题(已下线)第03章 铁 金属材料(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)鲁科版(2019)高一必修第一册高效手册——第3章 物质的性质与转化四川省自贡市田家炳中学2020-2021学年高一12月月考化学试题专题9 第二单元 探究铁及其化合物的转化-高中化学必修第二册苏教版2019(已下线)专题03 铁 金属材料-2023年高考化学一轮复习小题多维练(全国通用)天津市咸水沽第一中学2022-2023学年高三上学期学开学考试化学试题2019版鲁科化学必修第一册第3章第1节 铁的多样性课后习题辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题山东省单县第二中学2021-2022学年高一上学期11月段考化学试题山东省枣庄市滕州市2022-2023学年高一下学期开学考试化学试题广东省韶关市武江区北江实验中学2022-2023学年高三上学期第一次月考化学试题(已下线)专题九 铁及其化合物内蒙古自治区通辽市科尔沁左翼中旗实验高级中学2023-2024学年高一上学期1月期末化学试题山东省滨州市惠民县第二中学2023-2024学年高一上学期12月月考化学试题云南省祥华教育集团2023-2024学年高一下学期5月联考化学试题
7 . 用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是


| A.称量 | B.溶解 | C.转移 | D.定容 |
您最近一年使用:0次
2019-01-30更新
|
6856次组卷
|
164卷引用:人教版必修一化学第一章第二节物质的量浓度相关计算及配制一定浓度的溶液专项训练
人教版必修一化学第一章第二节物质的量浓度相关计算及配制一定浓度的溶液专项训练江苏省扬州市2021年普通高中学业水平检测模拟化学试题2013年全国普通高等学校招生统一考试化学(江苏卷)(已下线)2013-2014学年江苏省扬州市高一上学期期末调研测试化学试卷(已下线)2013-2014学年江苏省淮安高中教学协作体高二上学期期末化学试卷2018版化学(苏教版)高考总复习专题一对接高考精练--物质的量浓度及其溶液的配制【全国百强校】江苏省启东中学2018-2019学年高一(创新班)上学期期中考试化学试题江苏省沭阳县修远中学2019-2020学年高二10月月考化学(必修)试题江苏省南京师范大学附属中学2019-2020学年高一上学期期中化学试题江苏省苏州市吴江平望中学2019-2020学年高一上学期期中考试化学试题江苏省宿迁市北大附属宿迁实验学校2019-2020学年高一上学期期中考试化学试题江苏省淮安市涟水县第一中学2019-2020学年高一上学期第二次月考化学试题江苏省淮安市涟水县第一中学2020届高三上学期10月月考化学试题山西省太原市第二十一中学校2019-2020学年高二会考模拟化学试题江苏省连云港市智贤中学2021届高三9月月考化学试题江苏省宜兴第一中学2020-2021学年高一上学期期中考化学试题江苏省扬州市邗江区2020-2021高一上学期期中考试化学试题江苏省苏州中学园区校2019-2020学年高一上学期第一次月考化学试题江苏省盐城市实验高级中学(新洋高级中学)2020-2021学年高一上学期期中考试化学试题江苏省南京师范大学附属中学2021-2022学年高一上学期期中考试化学试题江苏省南京市六校2021-2022学年高一12月联合调研考试化学试题江苏省扬州市江都区大桥高级中学2021-2022学年高一上学期学情调研(一)化学试题江苏省盐城市大丰区新丰中学2022-2023学年高一上学期11月期中考试化学试题江苏省扬州市邗江区2023-2024学年高一上学期期中调研化学试题湖南省普通高中2023-2024学年高一下学期学业水平合格性考试模拟化学试卷五(已下线)2014届河南省中原名校联盟高三上学期第一次摸底考试化学试卷(已下线)2014届河南省郑州一中高三上学期期中考试化学试卷(已下线)2014高考名师推荐化学物质的量及相关计算(已下线)2015届吉林省东北师大附中高三第二次摸底考试化学试卷2014-2015福建省龙岩市一级达标校高一上学期期末化学试卷2015-2016学年湖南师大附属中学高一上三次阶段测化学卷2015-2016学年湖南省益阳市高一上学期期末化学试卷2015-2016学年山东省寿光现代中学高二6月月考化学试卷2016-2017学年山西省临汾一中高一上10月月考化学试卷2016-2017学年黑龙江哈尔滨三中高一上期中化学试卷2016-2017学年安徽铜陵市一中高一上期中考试化学试卷2016-2017学年湖南省浏阳一中高一12月月考化学试卷2016-2017学年安徽省蒙城一中高一下学期第一次月考化学试卷河南省林州市第一中学2017-2018学年高二上学期开学考试化学试题河南省南阳市七校2017-2018学年高一上学期第一次联考化学试题黑龙江省哈尔滨市第六中学2017-2018学年高一10月阶段测试化学试题福建省德化一中、永安一中、漳平一中2018届高三上学期三校联考化学试题黑龙江省大庆市第一中学2017-2018学年高一第一次阶段考试化学试题青海省西宁市第四高级中学2017-2018学年高一上学期第一次月考化学试题山西省太原市第五中学2017-2018学年高一10月月考化学试题安徽省铜陵市第一中学2016-2017学年高一上学期期中考试化学试题安徽省宿州市十三校2017-2018学年高一上学期期中考试化学试题河南省商丘市九校2017-2018学年高一上学期期中联考化学试题江西省宜春九中2017-2018学年高一上学期第一次月考化学试卷山西省忻州市2017-2018学年高一上学期期末考试化学试题黑龙江省哈尔滨市第六中学2017-2018学年高一3月月考化学试题【全国百强校】河北省武邑中学2017-2018学年高一下学期期中考试化学试题【全国百强校】黑龙江省哈尔滨市第三中学2017-2018学年高二下学期期末考试化学试题2018-2019学年高中化学鲁科版必修1章末综合测评题(一)(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第2讲 物质的量浓度及一定物质的量浓度溶液的配制(已下线)2019高考备考一轮复习精品资料 第一章 从实验学化学 第2讲 物质的量浓度及一定物质的量浓度溶液的配制【押题专练】(已下线)【备战2019年浙江新高考-考点】——考点03 物质的量浓度及溶液的配制【校级联考】福建省闽侯二中五校教学联合体2018届高三上学期期中考试化学试题(已下线)2019高考热点题型和提分秘籍 第一章 物质的量 第2讲 物质的量在化学实验中的应用( 题型专练)甘肃省孟坝中学2018-2019学年高一上学期期中考试化学试题辽宁省凌源市2018-2019学年高一下学期第一次联考化学试题河北省巨鹿县二中2017-2018学年高一期中考试化学试题陕西省吴起高级中学2018-2019学年高二下学期第二次月考基础卷化学试题吉林省长春外国语学校2018-2019学年高二下学期第二次月考化学试题(已下线)2019年7月7日 《每日一题》 2020年高考一轮复习-每周一测福建省长泰县第一中学2018-2019学年高二下学期期末考试化学试题辽宁省阜新市第二高级中学2018-2019学年高二下学期期末考试化学试题浙江省金华市2018-2019学年高一上学期期末考试化学试题河北省承德第一中学2019-2020学年高一9月月考化学试题西藏山南市第二高级中学2020届高三上学期第一次月考化学试题福建省长泰县第一中学2020届高三上学期期中考试化学试题甘肃省金昌市永昌县第四中学2019-2020学年高一上学期期中考试化学试题2020届高考化学小题狂练(全国通用版)专练19 化学实验基础(已下线)考点02 物质的量——《备战2020年高考精选考点专项突破题集》(已下线)考点20 化学基础实验——《备战2020年高考精选考点专项突破题集》广东省梅州市兴宁一中2019-2020学年高一上学期期中考试化学试题河北省衡水市阜城中学2019-2020高一上学期期中考试化学(人教版)试题河南省南阳市2019-2020学年高一上学期期中质量评估化学试题山东省济宁市第二中学2019-2020学年高二下学期第一次线上检测(实验班)化学试题甘肃省兰州师范大学附属中学2019-2020学年高一上学期期中考试化学试题吉林省长春市第一中学2019-2020学年高二下学期阶段测试化学试题福建省三明市尤溪第一中学2019-2020学年高一上学期第一次月考化学试题人教版(2019)高一必修第一册第二章 海水中的重要元素 第三节 物质的量 课时3 物质的量浓度鲁科版(2019)高一必修第一册第1章 认识化学科学 总结检测鲁科版(2019)高一必修第一册第一章第3节 化学中常用的物理量——物质的量 课时3 物质的量浓度高一必修第一册(鲁科2019)第1章第3节 化学中常用的物理量——物质的量 高考帮河南省洛阳市2021届高三上学期期中考试化学试题安徽省六安中学2021届高三上学期开学考试化学试题福建省福清西山学校高中部2021届高三9月月考化学试题人教版(2019)高一必修第一册 第二章 海水中的重要元素 第三节 物质的量 高考帮高一必修第一册(苏教2019版)专题2 第二单元 溶液组成的定量研究 课时1 物质的量浓度溶液的配制与分析河南通许县第一高级中学2021届高三上学期第一次月考化学试题河南省周口市中英文学校2020-2021学年高三上学期第一次月考化学试题福建省泰宁第一中学2020-2021学年高一上学期学分认定暨第一次阶段考试化学试题四川省沫若中学2020-2021学年高一上学期第一次月考化学试题河南省淮阳县陈州高级中学2020-2021学年高一上学期期中考试化学试题高一必修第一册(苏教2019)专题2 第二单元 溶液组成的定量研究1(已下线)2.3.3 物质的量浓度(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)安徽省合肥市第一中学2019—2020学年高一下学期期末考试化学试题(已下线)【浙江新东方】双师(5)河北唐山市第十一中学2020-2021学年高一上学期期中考试化学试题福建省南平市高级中学2020-2021学年高二上学期期中考试化学(会考)试题福建省永安市第一中学2020-2021学年高一上学期期中考试化学试题山东省泰安肥城市2020-2021学年高一上学期期中考试化学试题宁夏回族自治区固原市原州区固原市第一中学2020-2021学年高一上学期期中考试化学试题黑龙江省大庆市让胡路区大庆铁人中学2020-2021学年高一上学期期中考试化学试题西藏自治区拉萨那曲第二高级中学2021届高三第一次月考化学试题(已下线)【浙江新东方】双师 (59).黑龙江省安达市第七中学2020-2021学年高一11月份月考化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP402】【化学】(已下线)【浙江新东方】65.湖南省邵阳邵东市第一中学2020-2021学年高一上学期第三次月考化学试题山东省/(泰安市)新泰市第一中学北校2020-2021学年高一上学期第一次阶段性考试化学试题(已下线)【浙江新东方】绍兴qw93西藏拉萨市第四高级中学2020-2021学年高一上学期期中考试化学试题辽宁省朝阳市第一高级中学2020-2021学年高一上学期期末考试化学试题安徽省六安市新安中学2020-2021学年高一下学期入学考试化学试题山西省太原市第五十六中学2020-2021学年高二下学期5月月考化学试题四川省成都市蒲江县蒲江中学2019-2020学年高一上学期10月月考化学试题浙江省绍兴市柯桥区2020-2021学年高一下学期期末教学质量调测化学试题(已下线)专题02 物质的量在化学实验中的应用(热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)山东省夏津第一中学2022届高三上学期9月入学考试化学试题广东省东莞市2020-2021学年高一上学期期末考试化学试题山东省济南市长清第一中学2021-2022学年高一上学期10月阶段测试(A)化学试题河南省唐河县友兰实验高中2021-2022学年高一上学期第一次月考化学试题山东省枣庄市薛城区2021-2022学年高一上学期期中考试化学试题福建省邵武市第七中学2018-2019学年高一上学期10月月考化学试题湖南省天壹名校联盟2021-2022学年高一上学期期中考试化学试题陕西省西安中学2021-2022学年高三上学期期中考试化学试题山东省名校联盟2021-2022学年高一上学期12月联考化学试题广东省中山市2021-2022学年高一上学期期末检测化学试题河北省唐山市遵化市2021-2022学年高一上学期期中考试化学试题福建省长汀县第一中学2021-2022学年高一上学期第二次月考化学试题浙江省七彩阳光新高考研究联盟2021-2022学年高一下学期期中联考化学试题浙江省绍兴市柯桥区2021届高三下学期6月选考科目考试化学试题福建省厦门市湖滨中学2021-2022学年高一下学期5月月考化学试题重庆市求精中学2021-2022学年高一上学期第二次月考化学试题上海市上海师范大学附属嘉定高级中学2021-2022学年高一上学期期中考试化学试题(已下线)2.3.4 配制一定物质的量浓度的溶液-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)北京市首都师范大学附属中学2022-2023学年高三上学期9月阶段检测化学试题河南省实验中学022-2023学年高一上学期第一次月考化学试题福建省莆田砺志学校2021-2022学年高一下学期期中检测化学试题福建省宁德市2022-2023学年高一上学期期中质量检测化学试题山东省滨州市沾化区实验高级中学2022-2023学年高三10月月考化学试题苏教2020版化学必修第一册专题2 研究物质的基本方法 第二单元 溶液组成的定量研究课后习题河南省郑州外国语学校2021-2022学年高一上学期月考1 化学试题山东省日照市国开中学2022-2023学年高三9月月考化学试题天津市实验中学滨海学校黄南民族班2021-2022学年高三上学期期中质量监测化学试题山东省济南市天桥区黄河双语实验学校2021-2022学年高一上学期10月月考化学试题河南省濮阳市第一高级中学2022-2023学年高一上学期期中质量检测化学试题山东省潍坊市安丘市2022-2023学年高一上学期期末考试化学试题天津市静海区第一中学2020-2021学年高三下学期第三次模拟考试化学试题(已下线)题型4 一定物质的量浓度溶液的配制及误差分析(已下线)【2023】【高一下】【期中考】【杭九】【高中化学】【赵燕丽收集】(已下线)第13讲 一定物质的量浓度溶液的配制-【暑假自学课】2023年新高一暑假精品课(苏教版2019)(已下线)【知识图鉴】单元讲练测必修第一册第二单元02基础练广东省南阳中学、清新一中、佛冈一中、连州中学、连 山中学五校2022-2023学年高一上学期12月联考化学试题作业(十五) 物质的量浓度云南省宣威市第三中学2023-2024学年高二上学期收心考化学试题江西省百师联盟2024届高三上学期一轮复习联考化学试题江西省百师联盟2024届高三上学期9月复习联考化学试题福建省福州外国语学校2022-2023学年高一上学期12月期中考试化学试题
名校
8 . 某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如右图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光。下列有关该电池的说法正确的是

| A.电池工作时将电能转化成化学能 | B.锌片为电池的正极 |
| C.外电路中电子由锌片经导线流向铜片 | D.铜片上的电极反应: Cu2++2e-=Cu |
您最近一年使用:0次
2018-03-18更新
|
249次组卷
|
2卷引用:江苏省泰州中学2017-2018学年高二学业水平测试模拟(四)化学试题
9 . 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖的漂白和杀菌,其一种生产工艺流程如下:
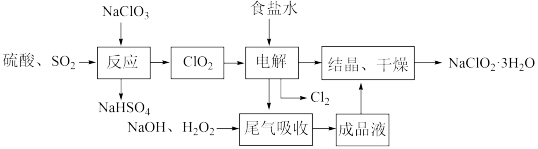
回答下列问题:
(1) 写出“反应”步骤中生成ClO2的化学方程式:________________________ 。
(2) “电解”所用食盐水由粗盐水精制而成,精制时为除去Mg2+和Ca2+,要加入的试剂分别为___________________ 、___________________ 。
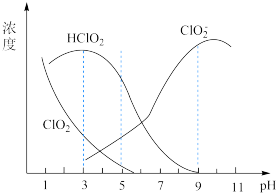
(3) 亚氯酸钠(NaClO2)在水溶液中可生成ClO2、HClO2、ClO 、Cl-等,其中HClO2和ClO2都具有漂白作用。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则使用该漂白剂的适宜pH
、Cl-等,其中HClO2和ClO2都具有漂白作用。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则使用该漂白剂的适宜pH________ (填“大于”“ 等于”或“小于”)3。
(4) 为了测定NaClO2·3H2O的纯度,取上述合成产品10.00 g溶于水配成1000 mL溶液,取出20.00 mL溶液于锥形瓶中,再加入足量硫酸酸化的KI溶液,充分反应后加入2~3滴淀粉溶液,用0.2640 mol·L-1Na2S2O3标准溶液滴定,共用去Na2S2O3标准溶液20.00 mL,通过计算确定该产品纯度是否合格?(合格纯度在90%以上)(写出计算过程)__________
提示: 2Na2S2O3+I2===Na2S4O6+2NaI。

回答下列问题:
(1) 写出“反应”步骤中生成ClO2的化学方程式:
(2) “电解”所用食盐水由粗盐水精制而成,精制时为除去Mg2+和Ca2+,要加入的试剂分别为

(3) 亚氯酸钠(NaClO2)在水溶液中可生成ClO2、HClO2、ClO
 、Cl-等,其中HClO2和ClO2都具有漂白作用。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则使用该漂白剂的适宜pH
、Cl-等,其中HClO2和ClO2都具有漂白作用。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则使用该漂白剂的适宜pH(4) 为了测定NaClO2·3H2O的纯度,取上述合成产品10.00 g溶于水配成1000 mL溶液,取出20.00 mL溶液于锥形瓶中,再加入足量硫酸酸化的KI溶液,充分反应后加入2~3滴淀粉溶液,用0.2640 mol·L-1Na2S2O3标准溶液滴定,共用去Na2S2O3标准溶液20.00 mL,通过计算确定该产品纯度是否合格?(合格纯度在90%以上)(写出计算过程)
提示: 2Na2S2O3+I2===Na2S4O6+2NaI。
您最近一年使用:0次
名校
解题方法
10 . 实验室有一包白色固体,可能含有硫酸铵、硫酸氢铵中的一种或两种,为确定其成分,现称取24.70g的白色固体溶于适量水中,然后滴加4mol·L-1的氢氧化钠溶液50.00mL,加热(此温度下铵盐不分解)充分反应使氨气全部逸出,测得氨气在标况下的体积为2.24L,则下列表述正确的是
| A.白色固体一定只含有硫酸铵 |
| B.若氢氧化钠溶液足量,则生成氨气的体积应为6.72L(标况) |
| C.从上述数据能求算出白色固体中(NH4)2SO4、NH4HSO4的物质的量之比为1∶2 |
| D.将某白色固体加热分解,若产生的气体不能使湿润的红色石蕊试纸变蓝,则该固体中一定不含铵盐 |
您最近一年使用:0次
2017-03-06更新
|
360次组卷
|
2卷引用:2016-2017学年江苏省连云港市高二学业水平模拟测试化学试卷