名校
解题方法
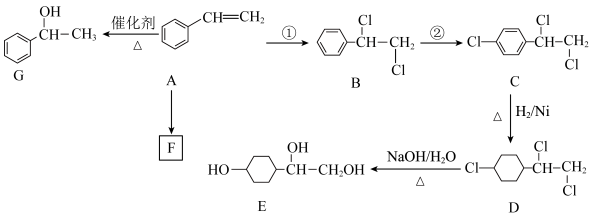
1 . 苯乙烯(A)是一种重要化工原料,以苯乙烯为原料可以制备一系列化工产品,如图示。
(1)E中所含官能团的名称是_______ 。F是高分子化合物,A→F的反应类型是_______ 。
(2)第②步反应所需的试剂_______ (填化学式)。
(3)H是G的同分异构体,其中属于酚类的H有_______ 种,任写一种符合核磁共振氢谱有4组峰且峰面积之比为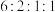 的H的结构简式
的H的结构简式_______ 。
(4)下列关于D→E的反应相关描述不正确的有_______。(填标号)
(5)以2-甲基丙烯为原料,参考上述信息,写出合成2-甲基-2-羟基丙醛(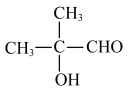 )的合成路线
)的合成路线_______ 。
(1)E中所含官能团的名称是
(2)第②步反应所需的试剂
(3)H是G的同分异构体,其中属于酚类的H有
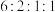 的H的结构简式
的H的结构简式(4)下列关于D→E的反应相关描述不正确的有_______。(填标号)
A.反应过程中,有 键的断裂和形成 键的断裂和形成 |
B.水分子中的键角小于 |
| C.化合物D和化合物E分子中均含有3个手性碳原子 |
D.化合物E分子中存在由 轨道“头碰头”形成的 轨道“头碰头”形成的 键 键 |
(5)以2-甲基丙烯为原料,参考上述信息,写出合成2-甲基-2-羟基丙醛(
 )的合成路线
)的合成路线
您最近一年使用:0次
名校
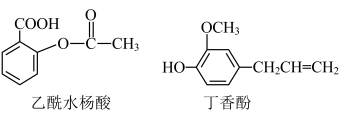
2 . Ⅰ.乙酰水杨酸是解热镇痛药阿司匹林的主要成分,丁香酚具有抗菌和降血压等作用,它们的结构简式如下:______ ,不饱和度为______ 。
(2)丁香酚分子中含有的官能团名称是______ 。
(3)分子式为 的芳香族化合物中,苯环上连接与丁香酚相同的3个基团的有机化合物有
的芳香族化合物中,苯环上连接与丁香酚相同的3个基团的有机化合物有______ 种,其中羟基和甲氧基(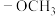 )位于对位的有机化合物的结构简式为
)位于对位的有机化合物的结构简式为______ 。
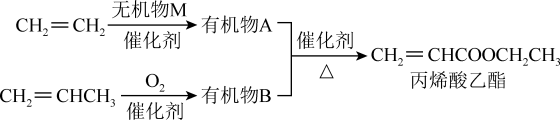
Ⅱ.丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成:______ 。
(5)A与B反应生成丙烯酸乙酯的化学方程式是______ 。
(6)久置的丙烯酸乙酯自身会发生聚合反应,所得聚合物具有较好的弹性,可用于生产织物和皮革处理剂。请写出上述聚合过程的化学方程式______ 。
(2)丁香酚分子中含有的官能团名称是
(3)分子式为
 的芳香族化合物中,苯环上连接与丁香酚相同的3个基团的有机化合物有
的芳香族化合物中,苯环上连接与丁香酚相同的3个基团的有机化合物有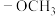 )位于对位的有机化合物的结构简式为
)位于对位的有机化合物的结构简式为Ⅱ.丙烯酸乙酯天然存在于菠萝等水果中,是一种食品用合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成:
(5)A与B反应生成丙烯酸乙酯的化学方程式是
(6)久置的丙烯酸乙酯自身会发生聚合反应,所得聚合物具有较好的弹性,可用于生产织物和皮革处理剂。请写出上述聚合过程的化学方程式
您最近一年使用:0次
名校
3 .  是制造芯片的新型半导体材料。回答下列问题:
是制造芯片的新型半导体材料。回答下列问题:
(1)镓为第四周期元素,基态 原子的价层电子轨道表示式为:
原子的价层电子轨道表示式为:_________________________ 。
(2) 的电负性由强到弱的顺序为
的电负性由强到弱的顺序为_________________________ (元素符号表示,下同);
 的第一电离能由大到小的顺序
的第一电离能由大到小的顺序_____________________________ 。
(3)芯片制造中用到光刻胶,可由甲基丙烯酸甲酯(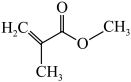 )、马来酸酐(
)、马来酸酐(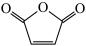 )等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为
)等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为_________________ ,马来酸酐分子中, 键和
键和 键个数比为
键个数比为_________________ 。
(4)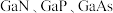 的结构类似于金刚石,熔点如表所示:
的结构类似于金刚石,熔点如表所示:
试分析三者熔点变化的原因:_________________________ 。
(5) 的晶胞结构如图所示(白球是
的晶胞结构如图所示(白球是 ,黑球是
,黑球是 )。
)。
图甲中,与 原子紧邻的
原子紧邻的 原子有
原子有_________ 个,若 晶体密度为
晶体密度为 ,相对分子质量为
,相对分子质量为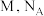 表示阿伏加德罗常数,则晶胞中距离最近的两个
表示阿伏加德罗常数,则晶胞中距离最近的两个 原子间距离为
原子间距离为_____________  。(用含
。(用含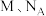 和
和 的代数式表示)
的代数式表示)
 是制造芯片的新型半导体材料。回答下列问题:
是制造芯片的新型半导体材料。回答下列问题:(1)镓为第四周期元素,基态
 原子的价层电子轨道表示式为:
原子的价层电子轨道表示式为:(2)
 的电负性由强到弱的顺序为
的电负性由强到弱的顺序为 的第一电离能由大到小的顺序
的第一电离能由大到小的顺序(3)芯片制造中用到光刻胶,可由甲基丙烯酸甲酯(
 )、马来酸酐(
)、马来酸酐( )等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为
)等通过加聚反应制得。甲基丙烯酸甲酯中碳原子的轨道杂化类型为 键和
键和 键个数比为
键个数比为(4)
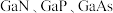 的结构类似于金刚石,熔点如表所示:
的结构类似于金刚石,熔点如表所示:| 物质 |  | 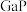 |  |
熔点/ | 1700 | 1480 | 1238 |
(5)
 的晶胞结构如图所示(白球是
的晶胞结构如图所示(白球是 ,黑球是
,黑球是 )。
)。图甲中,与
 原子紧邻的
原子紧邻的 原子有
原子有 晶体密度为
晶体密度为 ,相对分子质量为
,相对分子质量为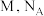 表示阿伏加德罗常数,则晶胞中距离最近的两个
表示阿伏加德罗常数,则晶胞中距离最近的两个 原子间距离为
原子间距离为 。(用含
。(用含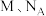 和
和 的代数式表示)
的代数式表示)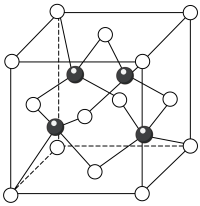
您最近一年使用:0次
名校
4 . 下列关于分子性质的解释错误的是
A. 比 比 稳定是由于水分子间可以形成氢键 稳定是由于水分子间可以形成氢键 |
B. 易溶于苯、 易溶于苯、 难溶于水,都可用“相似相溶”原理解释 难溶于水,都可用“相似相溶”原理解释 |
| C.分子晶体中一定存在分子间作用力,不一定存在共价键 |
D.乳酸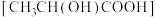 分子中含有一个手性碳原子 分子中含有一个手性碳原子 |
您最近一年使用:0次
5 . 下面的排序不正确的是
A.晶体熔点由低到高: |
B.熔点由高到低: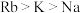 |
| C.硬度由大到小:金刚石>碳化硅>晶体硅 |
D.在 晶体中,与 晶体中,与 等距离且最近的 等距离且最近的 有12个 有12个 |
您最近一年使用:0次
6 . 下列各项叙述中,正确的是
A. 基态原子的未成对电子数依次增多 基态原子的未成对电子数依次增多 |
B.基态原子的价层电子排布为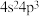 的元素,位于第四周期ⅤA族,是 的元素,位于第四周期ⅤA族,是 区元素 区元素 |
C. 和 和 轨道的形状均为哑铃形,能量也相等 轨道的形状均为哑铃形,能量也相等 |
D.硼原子核外电子由 ,原子释放能量 ,原子释放能量 |
您最近一年使用:0次
名校
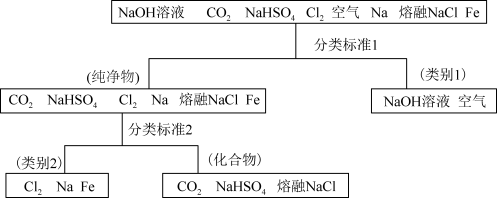
7 . 图所示为利用分类法对一组物质进行的分类。回答下列问题  属于
属于___________  填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与 反应的化学方程式
反应的化学方程式___________ ,依据该反应,可以说明
___________  填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。
(2)上述物质中属于电解质的是___________ 。
(3)某学生完成钠与水反应的实验,实验过程如图 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述不正确 的是___________。 填序号
填序号
(4)工业上常用 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为___________ 。
(5)向 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为___________ 。
 属于
属于 填“酸性”或“碱性”
填“酸性”或“碱性” 氧化物,书写
氧化物,书写 与
与 反应的化学方程式
反应的化学方程式
 填“属于”或“不属于”
填“属于”或“不属于” 碱性氧化物。
碱性氧化物。(2)上述物质中属于电解质的是
(3)某学生完成钠与水反应的实验,实验过程如图
 、
、 、
、 所示,下列有关实验现象及结论的叙述
所示,下列有关实验现象及结论的叙述 填序号
填序号
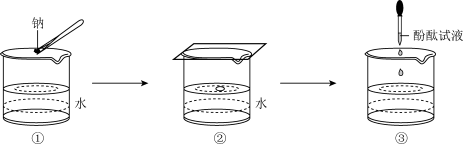
A.图 中钠熔成小球,说明钠与水反应放热且钠的熔点低 中钠熔成小球,说明钠与水反应放热且钠的熔点低 |
B.图 中钠四处游动并嘶嘶作响,说明反应产生了气体 中钠四处游动并嘶嘶作响,说明反应产生了气体 |
C.图 中滴加酚酞试液后溶液变红,说明有碱性物质生成 中滴加酚酞试液后溶液变红,说明有碱性物质生成 |
D.钠与水反应的离子方程式是: 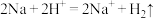 |
(4)工业上常用
 与
与 溶液反应制取消毒液,该反应的化学方程式为
溶液反应制取消毒液,该反应的化学方程式为(5)向
 溶液中加入NaOH溶液,对应的离子方程式为
溶液中加入NaOH溶液,对应的离子方程式为
您最近一年使用:0次
名校
8 . 氨既是一种重要的化工产品,又是一种重要的化工原料。图为合成氨以及氨氧化制硝酸的流程示意图:_______ ;反应开始后停止加热,发现反应更加剧烈,由此可知该反应是_______ (填“放热”或“吸热”)反应。
(2)可利用浓盐酸检验氨气管道是否泄漏,若泄漏,可观察到的现象_______ ,该反应方程式是_______ 。
(3)写出氧化炉中的化学反应方程式_______ 。
(4)工业生产中为了盛装大量浓硝酸,可选择_______ 作为罐体材料。
(5)为避免硝酸生产中的氮氧化物污染环境,人们开发了溶液吸收尾气处理方法。例如:尾气处理装置中含有少量的 ,通入空气,用具有碱性的
,通入空气,用具有碱性的 溶液等吸收尾气,产生不污染环境的气体和
溶液等吸收尾气,产生不污染环境的气体和 ,写出该反应的化学方程式
,写出该反应的化学方程式_______ 。
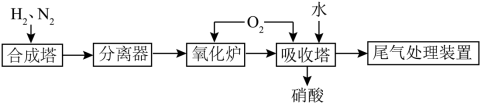
(2)可利用浓盐酸检验氨气管道是否泄漏,若泄漏,可观察到的现象
(3)写出氧化炉中的化学反应方程式
(4)工业生产中为了盛装大量浓硝酸,可选择_______ 作为罐体材料。
| A.铁 | B.铜 | C.铝 | D.铂 |
 ,通入空气,用具有碱性的
,通入空气,用具有碱性的 溶液等吸收尾气,产生不污染环境的气体和
溶液等吸收尾气,产生不污染环境的气体和 ,写出该反应的化学方程式
,写出该反应的化学方程式
您最近一年使用:0次
名校
9 . 设 为阿伏加德罗常数的值,则下列说法正确的是
为阿伏加德罗常数的值,则下列说法正确的是
 为阿伏加德罗常数的值,则下列说法正确的是
为阿伏加德罗常数的值,则下列说法正确的是A.2 mol  和足量 和足量 充分反应,生成2mol 充分反应,生成2mol  |
| B.在常温常压下,1.7gNH3含有的原子数为0.4NA |
| C.在加热下,5.6g铁粉与足量的硝酸完全反应,转移的电子为0.2mol |
D.0.1 mol/L的 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
名校
10 . 下列解释事实的方程式中,书写不正确 的是
A.氢氧化钠溶液试剂瓶不用玻璃塞的原因:SiO2+2OH-= +H2O +H2O |
B.硫在纯氧中点燃发出蓝紫色火焰:2S+3O2 2SO3 2SO3 |
C.过量SO2和NaOH溶液反应:SO2+OH- =  |
D.Cu和稀硝酸反应:3Cu+8H++2 =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
您最近一年使用:0次



