解题方法
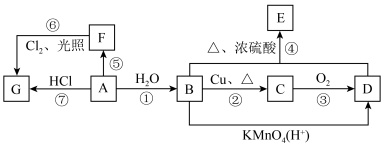
1 . 已知A是常用来衡量一个国家石油化工发展水平的标志性物质,A、B、C、D、E、F、G均为有机物,它们之间有如图转化关系。
(1)C的结构简式为___________ 。
(2)写出下列编号对应反应的化学方程式,并注明反应类型:
①___________ ,___________ 反应。
②___________ ,___________ 反应。
(3)有机物 的结构简式如图,回答下列问题。
的结构简式如图,回答下列问题。 中的官能团名称为
中的官能团名称为___________ 。
② 与足量的
与足量的 反应,生成
反应,生成
___________  ,与足量
,与足量 溶液反应生成产物的结构简式为
溶液反应生成产物的结构简式为___________ 。
(4)有机玻璃是一种高分子聚合物,单体是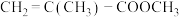 ,写出合成有机玻璃的化学方程式:
,写出合成有机玻璃的化学方程式:___________ 。
(1)C的结构简式为
(2)写出下列编号对应反应的化学方程式,并注明反应类型:
①
②
(3)有机物
 的结构简式如图,回答下列问题。
的结构简式如图,回答下列问题。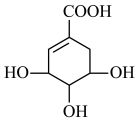
 中的官能团名称为
中的官能团名称为②
 与足量的
与足量的 反应,生成
反应,生成
 ,与足量
,与足量 溶液反应生成产物的结构简式为
溶液反应生成产物的结构简式为(4)有机玻璃是一种高分子聚合物,单体是
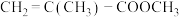 ,写出合成有机玻璃的化学方程式:
,写出合成有机玻璃的化学方程式:
您最近一年使用:0次
解题方法
2 . 随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
I.以 和
和 为原料合成尿素
为原料合成尿素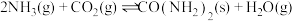
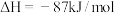 。
。
(1)有利于提高 平衡转化率的措施是___________(填序号)。
平衡转化率的措施是___________(填序号)。
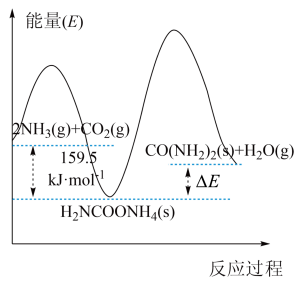
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图所示:
第一步: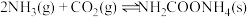

第二步: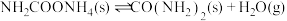


___________  。
。
②决定该反应速率是___________ 反应(填“第一步”或“第二步”),理由是___________ 。
Ⅱ.以和催化重整制备合成气: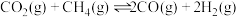 。
。
(3)在密闭容器中通入物质的量均为 的
的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应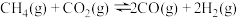 ,
, 的平衡转化率随温度、压强的变化关系如图所示。
的平衡转化率随温度、压强的变化关系如图所示。___________ (填序号)。
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率: D.同时断裂
D.同时断裂 键和
键和 键
键
②由图可知,压强
___________  (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同); 点速率
点速率
___________ 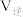 。
。
③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则
,则 点对应温度下的
点对应温度下的
___________ (用含 的代数式表示)。
的代数式表示)。
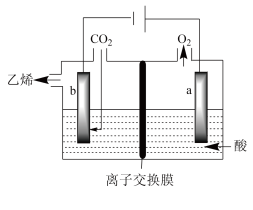
Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:___________ 。
I.以
 和
和 为原料合成尿素
为原料合成尿素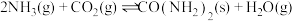
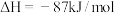 。
。(1)有利于提高
 平衡转化率的措施是___________(填序号)。
平衡转化率的措施是___________(填序号)。| A.高温低压 | B.低温高压 | C.高温高压 | D.低温低压 |
(2)研究发现,合成尿素反应分两步完成,其能量变化如下图所示:
第一步:
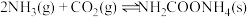

第二步:
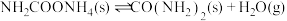


 。
。②决定该反应速率是
Ⅱ.以和催化重整制备合成气:
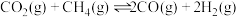 。
。(3)在密闭容器中通入物质的量均为
 的
的 和
和 ,在一定条件下发生反应
,在一定条件下发生反应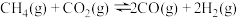 ,
, 的平衡转化率随温度、压强的变化关系如图所示。
的平衡转化率随温度、压强的变化关系如图所示。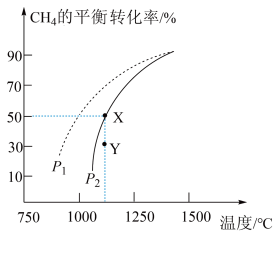
A.容器中混合气体的密度保持不变 B.容器内混合气体的压强保持不变
C.反应速率:
 D.同时断裂
D.同时断裂 键和
键和 键
键②由图可知,压强

 (填“>”“<”或“=”,下同);
(填“>”“<”或“=”,下同); 点速率
点速率
 。
。③已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ,则
,则 点对应温度下的
点对应温度下的
 的代数式表示)。
的代数式表示)。Ⅲ.电化学法还原二氧化碳制乙烯
在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示:
您最近一年使用:0次
解题方法
3 . 优氯净[二氯异氰尿酸钠 ]为白色固体,难溶于冷水,是最为广谱、高效、安全的氧化杀菌消毒剂。实验室利用
]为白色固体,难溶于冷水,是最为广谱、高效、安全的氧化杀菌消毒剂。实验室利用 溶液和氰尿酸[化学式为
溶液和氰尿酸[化学式为 制备优氯净[二氯异氰尿酸钠
制备优氯净[二氯异氰尿酸钠 ],实验装置如图所示(夹持装置略去)。
],实验装置如图所示(夹持装置略去)。
回答下列问题:
(1)仪器 的名称为
的名称为___________ ,装置A中的药品可以是___________ (填一种化学式)。
(2)实验发现装置 中
中 溶液的利用率较低,改进方法是
溶液的利用率较低,改进方法是___________ 。
(3)①当装置B内出现___________ 现象时,打开装置B的活塞加入氰尿酸 溶液,在反应过程中不断通入
溶液,在反应过程中不断通入 。
。
②实验过程中 的温度必须保持为
的温度必须保持为 ,
, 值控制在
值控制在 的范围,则该实验的控温方式是
的范围,则该实验的控温方式是___________ 。
③在装置 中用
中用 溶液吸收多余
溶液吸收多余 ,防止大气污染。写出该反应的离子方程式
,防止大气污染。写出该反应的离子方程式___________ 。
(4)反应结束后装置B中的浊液经过滤、___________ (填“温水”或“冷水”)洗涤、干燥得粗产品。
(5)通过下列实验,可以测定优氯净样品中有效氯的含量(样品中有效氯 )。
)。
反应原理: 、
、 、
、 。
。
实验步骤:准确称取 样品,用容量瓶配成
样品,用容量瓶配成 溶液;取
溶液;取 上述溶液于锥形瓶中,加入适量稀硫酸和过量
上述溶液于锥形瓶中,加入适量稀硫酸和过量 溶液,充分反应。生成的
溶液,充分反应。生成的 恰好消耗
恰好消耗 标准溶液。则该样品中有效氯的百分含量为
标准溶液。则该样品中有效氯的百分含量为___________  (保留三位有效数字)。
(保留三位有效数字)。
 ]为白色固体,难溶于冷水,是最为广谱、高效、安全的氧化杀菌消毒剂。实验室利用
]为白色固体,难溶于冷水,是最为广谱、高效、安全的氧化杀菌消毒剂。实验室利用 溶液和氰尿酸[化学式为
溶液和氰尿酸[化学式为 制备优氯净[二氯异氰尿酸钠
制备优氯净[二氯异氰尿酸钠 ],实验装置如图所示(夹持装置略去)。
],实验装置如图所示(夹持装置略去)。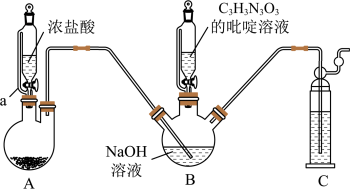

回答下列问题:
(1)仪器
 的名称为
的名称为(2)实验发现装置
 中
中 溶液的利用率较低,改进方法是
溶液的利用率较低,改进方法是(3)①当装置B内出现
 溶液,在反应过程中不断通入
溶液,在反应过程中不断通入 。
。②实验过程中
 的温度必须保持为
的温度必须保持为 ,
, 值控制在
值控制在 的范围,则该实验的控温方式是
的范围,则该实验的控温方式是③在装置
 中用
中用 溶液吸收多余
溶液吸收多余 ,防止大气污染。写出该反应的离子方程式
,防止大气污染。写出该反应的离子方程式(4)反应结束后装置B中的浊液经过滤、
(5)通过下列实验,可以测定优氯净样品中有效氯的含量(样品中有效氯
 )。
)。反应原理:
 、
、 、
、 。
。实验步骤:准确称取
 样品,用容量瓶配成
样品,用容量瓶配成 溶液;取
溶液;取 上述溶液于锥形瓶中,加入适量稀硫酸和过量
上述溶液于锥形瓶中,加入适量稀硫酸和过量 溶液,充分反应。生成的
溶液,充分反应。生成的 恰好消耗
恰好消耗 标准溶液。则该样品中有效氯的百分含量为
标准溶液。则该样品中有效氯的百分含量为 (保留三位有效数字)。
(保留三位有效数字)。
您最近一年使用:0次
4 . 下列应用与盐类水解无关的是
| A.用纯碱去油污时,加热可以增强去污效果 | B.用醋酸除去茶壶里的水垢 |
| C.草木灰与铵盐不能混合使用 | D.饱和氯化铁溶液滴入沸水中制备胶体 |
您最近一年使用:0次
5 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 和 和 的混合气体中所含氮原子数为 的混合气体中所含氮原子数为 |
B. 熔融的 熔融的 中含有 中含有 个阳离子 个阳离子 |
C.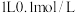 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
D. 的 的 溶液中含有 溶液中含有 的数目为 的数目为 |
您最近一年使用:0次
解题方法
6 . 下列实验过程能达到目的,且现象和结论正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向试管中加入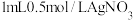 溶液,滴加 溶液,滴加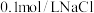 溶液 溶液 ,产生白色沉淀,再滴加2滴 ,产生白色沉淀,再滴加2滴 溶液,沉淀由白色变为黄色 溶液,沉淀由白色变为黄色 |  |
| B | 在两支试管中均加 溶液,分别滴入2滴 溶液,分别滴入2滴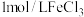 溶液和 溶液和 溶液,加 溶液,加 溶液的试管产生气泡速率更快 溶液的试管产生气泡速率更快 |  的催化效果强于 的催化效果强于 |
| C | 用 计分别测定浓度均为 计分别测定浓度均为 的 的 和 和 的 的 , , 的 的 更大 更大 | 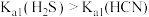 |
| D | 将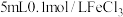 溶液与 溶液与 溶液混合于试管中充分反应后,滴加几滴 溶液混合于试管中充分反应后,滴加几滴 溶液,振荡,溶液变为血红色 溶液,振荡,溶液变为血红色 |  与 与 的反应有一定的限度 的反应有一定的限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 下列关于 的说法正确的是
的说法正确的是
 的说法正确的是
的说法正确的是A. 可用于漂白食品 可用于漂白食品 | B. 能与酸反应属于碱性氧化物 能与酸反应属于碱性氧化物 |
C. 中阴阳离子的个数比为 中阴阳离子的个数比为 | D. 可作潜水艇的供氧剂 可作潜水艇的供氧剂 |
您最近一年使用:0次
解题方法
8 . 下列化学用语表示正确的是
A.次氯酸分子电子式: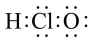 |
B. 的结构示意图为 的结构示意图为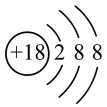 |
C.质子数为6、中子数为8的原子: |
D. 既可以表示甲烷分子,也可以表示四氯化碳分子 既可以表示甲烷分子,也可以表示四氯化碳分子 |
您最近一年使用:0次
9 . 化学与生产、生活密切相关,下列说法正确的是
| A.煤炭燃烧过程中添加“固硫”装置,可减少二氧化碳的排放 |
| B.铝制品表面有致密的氧化膜保护层,所以可长时间盛放酸(或碱)性物质 |
| C.明矾和臭氧都可用于净水,均利用了其氧化性 |
| D.预制菜进入校园,为让汤底更加浓郁、颜色更佳、口感更好,可适当使用食品添加剂 |
您最近一年使用:0次
10 . 下列有关说法正确的是
| A.断裂化学键的过程不一定发生化学变化 | B.原电池是将电能转化为化学能的装置 |
| C.电解质溶液导电的过程是物理变化 | D.纯水的pH一定等于7 |
您最近一年使用:0次



