1 . 化学与社会、生活密切相关。下列叙述正确的是
| A.二氧化硅可用于制作光感电池 |
| B.漂白粉在空气中久置变质,是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C.绿色化学要求从源头上消除或减少生产活动对环境的污染 |
| D.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 |
您最近一年使用:0次
2 . 实验室以含钴废料(主要成分是CoO、Co2O3,含少量Fe2O3、Al2O3等杂质)为原料制备CoCO3的流程如图所示。
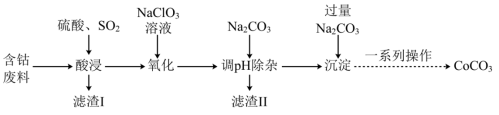
已知:①“酸浸”后过滤得到的滤液中含有Co2+、Fe2+、Al3+等。
②有关沉淀数据如表(完全沉淀时金属离子浓度≤1×10-5mol/L):
回答下列问题:
(1)基态钴原子的价层电子排布式为_______ ,在“酸浸”之前,先要对含钴废料进行粉碎处理,其目的是_______ 。
(2)“酸浸”时需通入SO2,其中SO2作______ (填“氧化剂”或“还原剂”),由于“酸浸”时,溶液中会产生Fe3+,写出SO2与Fe3+反应的离子方程式:______ 。
(3)“氧化”流程中,氧化剂与还原剂的物质的量之比为______ 。
(4)常温下,若浸取液中c(Co2+)=0.1mol/L,则“调pH除杂”时需调节溶液pH的范围为______ 至______ 。(加入NaClO3和Na2CO3时,溶液的体积变化忽略)
(5)“滤渣II”的主要成分为______ 。
(6)“一系列操作”为过滤、洗涤、干燥,其中过滤所需要的硅酸盐材质的仪器有_______ 。
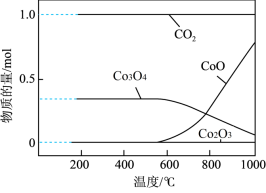
(7)将得到的CoCO3固体在空气中加热,反应温度对反应产物的影响如图所示,则500~1000℃时,发生主要反应的化学方程式为_______ 。

已知:①“酸浸”后过滤得到的滤液中含有Co2+、Fe2+、Al3+等。
②有关沉淀数据如表(完全沉淀时金属离子浓度≤1×10-5mol/L):
| 沉淀 | Al(OH)3 | Fe(OH)3 | Co(OH)2 |
| 恰好完全沉淀时的pH | 5.2 | 2.8 | 9.4 |
(1)基态钴原子的价层电子排布式为
(2)“酸浸”时需通入SO2,其中SO2作
(3)“氧化”流程中,氧化剂与还原剂的物质的量之比为
(4)常温下,若浸取液中c(Co2+)=0.1mol/L,则“调pH除杂”时需调节溶液pH的范围为
(5)“滤渣II”的主要成分为
(6)“一系列操作”为过滤、洗涤、干燥,其中过滤所需要的硅酸盐材质的仪器有
(7)将得到的CoCO3固体在空气中加热,反应温度对反应产物的影响如图所示,则500~1000℃时,发生主要反应的化学方程式为

您最近一年使用:0次
3 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 证明氧化性Cl2>Br2>I2 | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 |
| B | 比较水和乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
| C | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 能正确表示下列反应的离子方程式为
A.过量铁粉加入稀硝酸中:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
C.用Na2SO3溶液吸收少量Cl2:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3•H2O +OH-=NH3•H2O |
您最近一年使用:0次
5 . 设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.2L0.5mol/L亚硫酸溶液中含有的H+数为2NA |
| B.23gNa与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA |
| C.标准状况下,22.4LCHCl3中含有氯原子数目为3NA |
| D.28gC2H4分子中含有的σ键数目为4NA |
您最近一年使用:0次
解题方法
6 . 已知有如图所示物质间的相互转化,已知A是一种金属单质。
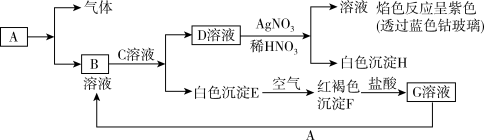
试回答:
(1)按要求作答:B物质的化学式:___________ ,C物质的电子式___________ 。
(2)写出由E转变成F的化学方程式:___________ 。
(3)写出下列反应的离子方程式:D溶液与AgNO3反应:___________ ;向G溶液中加入A:___________ 。
(4)焰色试验是___________ 变化。填(“物理”或“化学”)

试回答:
(1)按要求作答:B物质的化学式:
(2)写出由E转变成F的化学方程式:
(3)写出下列反应的离子方程式:D溶液与AgNO3反应:
(4)焰色试验是
您最近一年使用:0次
7 .  表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A.标准状况下,22.4LH2O含有的分子数为 |
B.常温常压下, 个 个 分子占有的体积为22.4L 分子占有的体积为22.4L |
C.5.6 g金属铁与足量稀硫酸反应转移的电子数为0.2 |
D.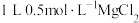 溶液中,含 溶液中,含 个数为2 个数为2 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.Na跟水反应所得产物既有电解质又有非电解质 |
| B.加入还原剂才可完成NaCl→Na的转化 |
C.过氧化钠的电子式为 |
| D.Na2CO3溶液显碱性,Na2CO3属于盐类 |
您最近一年使用:0次
9 . 下列4支试管中,等质量的铁与足量盐酸反应生成H2的反应速率最大的是
| 试管 | 盐酸浓度 | 温度 | 铁的状态 |
| A | 1mol·L-1 | 10℃ | 块状 |
| B | 1mol·L-1 | 10℃ | 粉末状 |
| C | 3mol·L-1 | 20℃ | 块状 |
| D | 3mol·L-1 | 20℃ | 粉末状 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-30更新
|
223次组卷
|
2卷引用:云南省保山市腾冲市第八中学2020-2021学年高一下学期期末考试化学试题
解题方法
10 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:

(1)写出工业上由食盐制备
 的离子方程式:
的离子方程式:(2)步骤Ⅰ中已获得
 ,步骤Ⅱ中又将
,步骤Ⅱ中又将 转化为
转化为 和
和 ,其目的是
,其目的是(3)步骤Ⅱ中通入热空气吹出
 ,利用了
,利用了 的___________(填标号)。
的___________(填标号)。| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(4)步骤Ⅱ中用纯碱溶液吸收
 ,该反应的化学方程式为
,该反应的化学方程式为(5)从理论上考虑,下列物质也能吸收
 的是___________(填标号)。
的是___________(填标号)。A. | B.NaCl溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(6)查阅资料知,
 的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
您最近一年使用:0次



