解题方法
1 . 第L能层所含的能级数,最多容纳的电子数分别为
| A.2,2 | B.2,8 | C.2,16 | D.4,32 |
您最近一年使用:0次
解题方法
2 . 2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)下图是_______ 装置,能量转化是,_____ 能转化为_____ 能。______ 极,发生_____ (填“氧化”或“还原”)反应。
(3)Cu棒,上发生的电极反应是______ 。
(4)溶液中H⁺向______ (填“Zn”或“Cu”)电极定向移动。
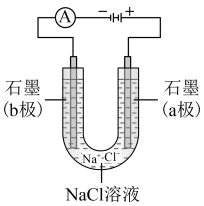
(5)下图是_____ 装置,a极是该电池的_______ 极,b极是该电池的_____ 极。
(1)下图是
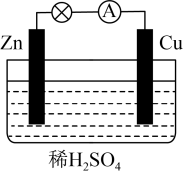
(3)Cu棒,上发生的电极反应是
(4)溶液中H⁺向
(5)下图是
您最近一年使用:0次
解题方法
3 . 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下图是元素周期表的一部分。______ (金属或非金属)元素;元素b在元素周期表中的位置为______ 。
(2)元素c的原子结构示意图_______ ;元素f的元素符号为______ ;元素c和f的原子半径大小关系为c____ f(>或<)
(3)元素d和元素g形成的盐的电子式为_______ 。
(4)第一电离能a___ d(>或<),非金属性c___ f(>或<)。
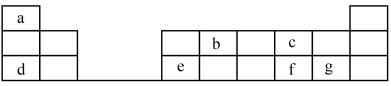
(2)元素c的原子结构示意图
(3)元素d和元素g形成的盐的电子式为
(4)第一电离能a
您最近一年使用:0次
4 . 按要求回答下列问题:
(1)消毒液的组成元素中,基态O原子的电子排布式是______ ,基态Cl原子未成对电子数为_____ 个。
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为_______ (填元素符号),氧元素和氮元素的非金属性的大小顺序为________ (填元素符号)
(3)某元素原子的最外层电子构型为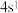 ,元素周期表的位置第
,元素周期表的位置第____ 周期,第_____ 族,它属于____ 区元素。
(1)消毒液的组成元素中,基态O原子的电子排布式是
(2)与氧元素相邻的氮元素的第一电离能的大小顺序为
(3)某元素原子的最外层电子构型为
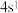 ,元素周期表的位置第
,元素周期表的位置第
您最近一年使用:0次
5 . 反应;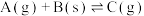
 ,在其他条件不变时,改变其中一个条件,则生成
,在其他条件不变时,改变其中一个条件,则生成 的速率(填“增大”、“不变”、“减小”):
的速率(填“增大”、“不变”、“减小”):
(1)升温_______ 。
(2)使用催化剂_______ 。
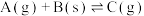
 ,在其他条件不变时,改变其中一个条件,则生成
,在其他条件不变时,改变其中一个条件,则生成 的速率(填“增大”、“不变”、“减小”):
的速率(填“增大”、“不变”、“减小”):(1)升温
(2)使用催化剂
您最近一年使用:0次
6 . 下列能层的能量由低到高的顺序是
| A.K、L、Q、O | B.P、Q、N、L | C.K、L、M、N | D.M、K、P、Q |
您最近一年使用:0次
解题方法
7 . 电解原理在化学工业中有广泛应用。下图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:___________ (填写“阳极”或“阴极”)。
(2)若X、Y都是惰性电极,a是饱和食盐水,Y极上的电极反应式为___________ 。
(3)若X、Y都是惰性电极,a是CuCl2溶液,X极的电极反应式为___________ 。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是___________ 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的的方案是___________。 填字母编号
填字母编号

(2)若X、Y都是惰性电极,a是饱和食盐水,Y极上的电极反应式为
(3)若X、Y都是惰性电极,a是CuCl2溶液,X极的电极反应式为
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的的方案是___________。
 填字母编号
填字母编号
| 方案 | X | Y |  溶液 溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 |  |
| C | 铁 | 银 | 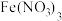 |
| D | 铁 | 银 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
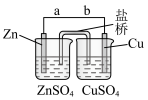
8 . 某学生利用下面实验装置探究盐桥式原电池的工作原理。
(1)锌电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ ;铜电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ 。
(2)导线中电子流向由___________ 流向___________ (用a、b表示)。
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为___________ ;
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
(5)反应一段时间后右侧烧杯中Cu2+浓度是___________ (填增大,减小或不变)。
(1)锌电极为电池的
(2)导线中电子流向由
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
| A.NaOH | B.Zn | C.Fe | D.H2SO4 |
(5)反应一段时间后右侧烧杯中Cu2+浓度是
您最近一年使用:0次
9 . 现有含AgBr的饱和溶液:
(1)AgBr的沉淀溶解平衡方程式:___________ ,Ksp的表达式是___________ ;
(2)加入固体AgNO3,则c(Ag+)___________ (填“变大”、“变小”或“不变”,下同);
(3)加入更多的AgBr固体,则c(Ag+)___________ ;
(1)AgBr的沉淀溶解平衡方程式:
(2)加入固体AgNO3,则c(Ag+)
(3)加入更多的AgBr固体,则c(Ag+)
您最近一年使用:0次
10 . 回答下列问题:
(1)FeCl3的水溶液呈___________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示);实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水将其稀释到所需的浓度,以___________ (填“促进”或“抑制”)其水解。
(2)将FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。
(1)FeCl3的水溶液呈
(2)将FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是
您最近一年使用:0次



