名校
解题方法
1 . 胆矾(CuSO4·5H2O)的结构示意图如下所示。下列说法不正确 的是

A.基态Cu2+的价层电子轨道表示式是  |
| B.H2O中氧原子的VSEPR的价层电子对数是4 |
C.SO 中的O-S-O的键角小于H2O中的H-O-H的键角 中的O-S-O的键角小于H2O中的H-O-H的键角 |
D.胆矾中的H2O与Cu2+、H2O与SO 的作用力分别为配位键和氢键 的作用力分别为配位键和氢键 |
您最近一年使用:0次
23-24高二下·北京·期末
2 . 铁的多种化合物均为磁性材料,氮化铁(FexNy)是其中一种,某FexNy的制备需铁、氮气、丙酮和乙醇参与。
(1)Fe在元素周期表中的位置___________ 。
(2)丙酮(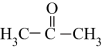 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是___________ ,1mol丙酮分子中含有σ键的数目为___________ mol。
(3)乙醇的晶体类型为___________ ,乙醇分子中C、O、H三种元素中电负性最大的元素是___________ 。
(4)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是___________ 。
(1)Fe在元素周期表中的位置
(2)丙酮(
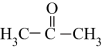 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(3)乙醇的晶体类型为
(4)乙醇的沸点(78.3℃)高于丙酮的沸点(56.5℃),原因是
您最近一年使用:0次
23-24高二下·北京·期末
解题方法
3 . 非金属氟化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态F原子核外电子的运动状态有___________ 种。
(2)O、F、Cl电负性最小的是___________ ;HClO的电子式为___________ ;OF2的沸点低于Cl2O,原因是___________ 。
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为___________ 。XeF2与水反应时放出氧气和氙气,氟以化合态留在溶液中,该反应的化学方程式为___________ 。
(1)基态F原子核外电子的运动状态有
(2)O、F、Cl电负性最小的是
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
您最近一年使用:0次
23-24高二下·北京·期末
解题方法
4 . 有机化合物M的合成路线如下图所示,下列说法不正确的是
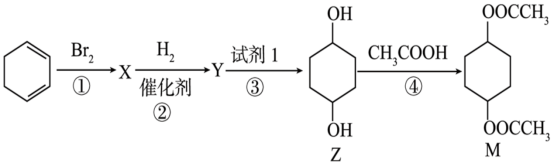
A.反应①还可能生成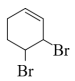 |
B.Y的分子式为 |
C.若用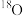 标记Z中的O原子,则M中一定含有 标记Z中的O原子,则M中一定含有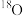 |
| D.试剂1为NaOH醇溶液 |
您最近一年使用:0次
5 . 下列化学用语不正确 的是
A.氮分子的电子式:  |
B.基态 原子的价电子轨道表示式: 原子的价电子轨道表示式: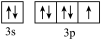 |
C.基态 的价电子排布式: 的价电子排布式: |
D. 分子的空间结构模型: 分子的空间结构模型: |
您最近一年使用:0次
6 . 某烃与H2反应后能生成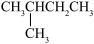 ,则该烃不可能是
,则该烃不可能是
A.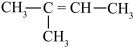 | B.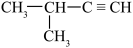 |
C.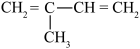 | D.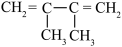 |
您最近一年使用:0次
2024-04-27更新
|
320次组卷
|
10卷引用:北京市西城区2021-2022学年高二下学期期末化学试题
北京市西城区2021-2022学年高二下学期期末化学试题北京市第三十五中学2022-2023学年高二下学期期中考试化学试题北京师范大学第二附属中学2023-2024学年高二下学期期中考试化学试题北京市宣武外国语实验学校2023-2024学年高二下学期期中考试化学试题北京市铁路第二中学2023-2024学年高二下学期期中考试化学试题北京市顺义区第一中学2023-2024学年高二下学期期中考试化学试题名校期中好题汇编-烃(选择题)2.2.1 烯烃 随堂练习(已下线)清单05 烃(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)四川省华蓥中学2022-2023学年高一下学期5月月考化学试题
7 . 氮化硼晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
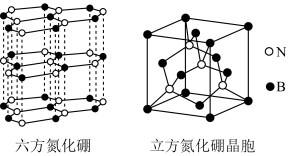
| A.六方氮化硼与立方氮化硼互为同素异形体 |
B.立方相氮化硼含有 键和 键和 键,所以硬度大 键,所以硬度大 |
C.六方、立方相氮化硼晶体的化学式均为BN,硼原子的杂化类型分别为 、 、 |
| D.两种晶体中既有极性键又有非极性键 |
您最近一年使用:0次
8 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是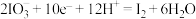 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
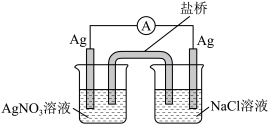
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
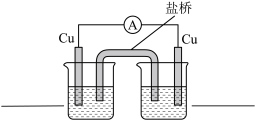
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
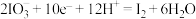 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近一年使用:0次
解题方法
9 . 氟在已知元素中电负性最大、非金属性最强,其单质在1886年才被首次分离出来。
(1)基态F原子的核外电子排布式为___________ 。基态F原子的电子有___________ 种空间运动状态。
(2)氟氧化物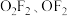 的结构已经确定。
的结构已经确定。
①依据上表数据推测 键的稳定性:
键的稳定性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
② 中
中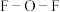 的键角小于
的键角小于 中
中 的键角,解释原因:
的键角,解释原因:___________ 。
(3) 是一种有特殊性质的氢化物。
是一种有特殊性质的氢化物。
①已知:氢键 中三原子在一条直线上时,作用力最强。测定结果表明,
中三原子在一条直线上时,作用力最强。测定结果表明,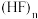 固体中
固体中 分子排列成锯齿形。画出含2个
分子排列成锯齿形。画出含2个 的重复单元结构:
的重复单元结构:___________ 。
② 中加入
中加入 可以解离出
可以解离出 和具有正四面体形结构的阴离子,写出该过程的离子方程式:
和具有正四面体形结构的阴离子,写出该过程的离子方程式:___________ 。
(4)工业上用蒬石(主要成分 )制备
)制备 。
。 晶体的一种立方晶胞如图所示。
晶体的一种立方晶胞如图所示。 晶体中距离
晶体中距离 最近的
最近的 有
有___________ 个。
②晶体中 与
与 的最近距离为
的最近距离为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。该晶体的密度
。该晶体的密度
___________  (列出计算式)。
(列出计算式)。
(1)基态F原子的核外电子排布式为
(2)氟氧化物
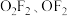 的结构已经确定。
的结构已经确定。 |  | |
 键长/pm 键长/pm | 121 | 148 |
 键的稳定性:
键的稳定性:
 (填“>”或“<”)。
(填“>”或“<”)。②
 中
中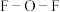 的键角小于
的键角小于 中
中 的键角,解释原因:
的键角,解释原因:(3)
 是一种有特殊性质的氢化物。
是一种有特殊性质的氢化物。①已知:氢键
 中三原子在一条直线上时,作用力最强。测定结果表明,
中三原子在一条直线上时,作用力最强。测定结果表明,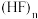 固体中
固体中 分子排列成锯齿形。画出含2个
分子排列成锯齿形。画出含2个 的重复单元结构:
的重复单元结构:②
 中加入
中加入 可以解离出
可以解离出 和具有正四面体形结构的阴离子,写出该过程的离子方程式:
和具有正四面体形结构的阴离子,写出该过程的离子方程式:(4)工业上用蒬石(主要成分
 )制备
)制备 。
。 晶体的一种立方晶胞如图所示。
晶体的一种立方晶胞如图所示。
 晶体中距离
晶体中距离 最近的
最近的 有
有②晶体中
 与
与 的最近距离为
的最近距离为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。该晶体的密度
。该晶体的密度
 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
10 .  在实验研究和化学工业中应用广泛,有多种制备方法。
在实验研究和化学工业中应用广泛,有多种制备方法。
Ⅰ.利用 溶液吸收
溶液吸收 制备
制备 溶液
溶液
(1)写出该制备方法的离子方程式___________ 。
(2) 时,
时, 与
与 反应后的溶液中,
反应后的溶液中, 价含
价含 微粒(
微粒( 和
和 )物质的量分数随
)物质的量分数随 变化如图1所示:
变化如图1所示:
Ⅱ.利用工业废碱渣(主要成分 )吸收硫酸厂尾气中的
)吸收硫酸厂尾气中的 制备无水
制备无水 的成本低,优势明显。其流程如下:
的成本低,优势明显。其流程如下: )显碱性的原因
)显碱性的原因___________ 。
(4)图2为吸收塔中 溶液与
溶液与 反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是
反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是___________ 。___________ 。
(6)为了降低由中和器所得溶液中 的溶解度,从而提高结晶产率,中和器中加入的
的溶解度,从而提高结晶产率,中和器中加入的 是过量的。
是过量的。
①请结合化学反应原理解释 过量的原因
过量的原因___________ 。
②结晶时应选择的最佳操作是___________ (选填字母)。
a.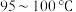 加热蒸发,直至蒸干
加热蒸发,直至蒸干
b.维持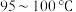 蒸发浓缩至有大量晶体析出,趁热过滤
蒸发浓缩至有大量晶体析出,趁热过滤
c.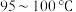 加热浓缩,冷却至室温结晶,过滤
加热浓缩,冷却至室温结晶,过滤
(7)为检验 成品中是否含少量
成品中是否含少量 ,需选用的试剂是
,需选用的试剂是___________ 。
 在实验研究和化学工业中应用广泛,有多种制备方法。
在实验研究和化学工业中应用广泛,有多种制备方法。Ⅰ.利用
 溶液吸收
溶液吸收 制备
制备 溶液
溶液(1)写出该制备方法的离子方程式
(2)
 时,
时, 与
与 反应后的溶液中,
反应后的溶液中, 价含
价含 微粒(
微粒( 和
和 )物质的量分数随
)物质的量分数随 变化如图1所示:
变化如图1所示: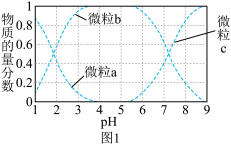
A.曲线 表示 表示 物质的量分数随溶液 物质的量分数随溶液 变化的曲线 变化的曲线 |
B. 的溶液中: 的溶液中: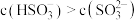 |
C. 的溶液中: 的溶液中: |
D. 的 的 溶液中存在: 溶液中存在: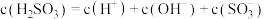 |
Ⅱ.利用工业废碱渣(主要成分
 )吸收硫酸厂尾气中的
)吸收硫酸厂尾气中的 制备无水
制备无水 的成本低,优势明显。其流程如下:
的成本低,优势明显。其流程如下: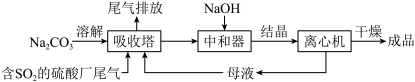
 )显碱性的原因
)显碱性的原因(4)图2为吸收塔中
 溶液与
溶液与 反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是
反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是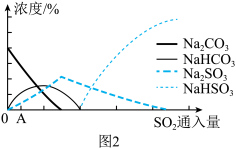
| 资料显示: Ⅰ.  在 在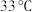 时溶解度最大,将其饱和溶液加热至 时溶解度最大,将其饱和溶液加热至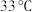 以上时,由于溶解度降低会析出无水 以上时,由于溶解度降低会析出无水 ,冷却至 ,冷却至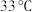 以下时析出 以下时析出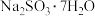 ; ;Ⅱ.无水  在空气中不易被氧化, 在空气中不易被氧化,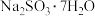 在空气中易被氧化。 在空气中易被氧化。 |
(6)为了降低由中和器所得溶液中
 的溶解度,从而提高结晶产率,中和器中加入的
的溶解度,从而提高结晶产率,中和器中加入的 是过量的。
是过量的。①请结合化学反应原理解释
 过量的原因
过量的原因②结晶时应选择的最佳操作是
a.
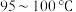 加热蒸发,直至蒸干
加热蒸发,直至蒸干b.维持
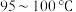 蒸发浓缩至有大量晶体析出,趁热过滤
蒸发浓缩至有大量晶体析出,趁热过滤c.
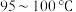 加热浓缩,冷却至室温结晶,过滤
加热浓缩,冷却至室温结晶,过滤(7)为检验
 成品中是否含少量
成品中是否含少量 ,需选用的试剂是
,需选用的试剂是
您最近一年使用:0次



