解题方法
1 . 化学在生产和日常生活中有着重要的应用,下表中用途与其性质或原理对应关系错误的是
| 选项 | 用途 | 性质或原理 |
| A | 硬铝是制造飞机和宇宙飞船的理想材料 | 硬铝密度小、强度高具有较强的抗腐蚀能力 |
| B | 抗击新冠疫情时,84消毒液、75%酒精都可作为环境消毒剂 | 二者都有较强的氧化性 |
| C | 工业上常用绿矾(FeSO4•7H2O)处理废水中含有的重铬酸根离子(Cr2O ) ) | Fe2+具有还原性 |
| D | 用小苏打治疗胃酸过多 | NaHCO3可中和胃酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下列含氮物质的性质与用途具有对应关系的是
| A.N2难溶于水,可用作粮食保护气 |
| B.NH3具有还原性,液氨可作制冷剂 |
| C.HNO3具有挥发性,可用于制造化肥 |
| D.NH4Cl溶液呈酸性,可用于去除铁锈 |
您最近一年使用:0次
2023-04-14更新
|
235次组卷
|
3卷引用:上海市静安区2022-2023学年高三下学期二模变式题(选择题6-10)
(已下线)上海市静安区2022-2023学年高三下学期二模变式题(选择题6-10)上海市静安区2022-2023学年高三下学期二模测试化学试题宁夏银川市第二中学2023-2024学年高三上学期统练四 化学试题
名校
3 . 氧化物在生产、生活中有广泛应用。下列氧化物的性质与用途具有对应关系的是
A. 熔点高,可用于工业制备金属铝 熔点高,可用于工业制备金属铝 |
B. 易溶于水,可用于自来水消毒 易溶于水,可用于自来水消毒 |
C. 具有漂白、防腐、抗氧化,可用于葡萄酒保存 具有漂白、防腐、抗氧化,可用于葡萄酒保存 |
D. 具有强氧化性,可用作呼吸面具供氧剂 具有强氧化性,可用作呼吸面具供氧剂 |
您最近一年使用:0次
名校
4 . 下列有关物质性质与用途具有对应关系的是
| A.浓硫酸具有强氧化性,可用于干燥CO2 |
| B.FeCl3溶液呈酸性,可用于腐蚀电路板上的Cu |
| C.石墨具有导电性,可用于制铅笔芯 |
| D.Al2O3熔点高,可用作耐高温材料 |
您最近一年使用:0次
2021-03-18更新
|
301次组卷
|
5卷引用:三轮冲刺卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)
(已下线)三轮冲刺卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)上海市青浦高级中学2021届高三下学期3月月考化学试题上海市吴淞中学2021-2022学年高二上学期第一次月考化学试题江苏省南京市中华中学2021-2022学年高一下学期期末考试化学试题河北省石家庄市第一中学2022-2023高二上学期9月开学考试化学试题
5 . 下列有关物质的性质与用途具有对应关系的是
| A.铝的金属活泼性强,可用于制作铝金属制品 |
| B.氧化铝熔点高,可用作电解冶炼铝的原料 |
| C.氢氧化铝受热分解,可用于中和过多的胃酸 |
| D.明矾溶于水并水解形成胶体,可用于净水 |
您最近一年使用:0次
2020-07-11更新
|
7085次组卷
|
47卷引用:第5章 金属及其化合物(章末复习)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)
(已下线)第5章 金属及其化合物(章末复习)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)专题05 元素及其化合物-2020年高考真题和模拟题化学分项汇编(已下线)第5单元 常见的金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)第12讲 镁、铝、铜及其化合物 金属冶炼(精讲)——2021年高考化学一轮复习讲练测(已下线)小题必刷14 铝及其化合物——2021年高考化学一轮复习小题必刷(通用版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练上海市崇明区2021届高三下学期二模化学试题(已下线)课时16 铝及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向03 物质的组成、性质和分类-备战2022年高考化学一轮复习考点微专题(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第8讲 金属材料(不锈钢、铝合金、合金)(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第三单元 金属及其化合物(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点15 铝及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第08讲 金属材料(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题08 元素及其化合物(练)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题09 常见金属元素的性质及应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)第三章 金属及其化合物 第15讲 金属材料 金属冶炼(已下线)题型33 铝及其化合物的性质(已下线)专题05 元素化合物性质(已下线)第5讲 金属材料与金属的冶炼(已下线)考点11 镁、铝及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题1-52020年江苏卷化学高考试题四川省成都市双流棠湖中学2021届高三上学期开学考试理综化学试题黑龙江省哈尔滨市第九中学2021届高三上学期开学考试化学试题河南省三门峡市第一高级中学2021届高三8月开学考试化学试题江西师范大学附属中学2020-2021学年高一上学期12月考试化学试题(已下线)练习12 从铝土矿到铝合金-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)河南省豫南九校2020-2021学年高一上学期第三次联考化学试题江西省赣州市第十四中学2022届高三上学期第二次月考化学试题北京市北京中国人民大学附属中学2022届高三10月检测化学试卷(已下线)2020年江苏卷化学高考真题变式题1-10黑龙江省鹤岗市第一中学2021-2022学年高二下学期期末考试化学试题第三章 铁金属材料 综合拔高练甘肃省武威第十八中学2022-2023学年高三上学期第一次诊断化学试题江西省赣州市赣县第三中学2022-2023学年高三上学期(奥赛班)强化训练化学试题河南省濮阳市第一高级中学2022-2023学年高三上学期第三次质量检测考试化学试题内蒙古巴彦淖尔市临河区第三中学2021~2022学年高三上学期期中考试化学试题北京市昌平区第二中学2022-2023 学年高三上学期期中考试化学试题陕西省西安市周至县第六中学2023-2024学年高三上学期11月期中化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷江苏省扬州大学附属中学2023-2024学年高二下学期 3月月考化学试卷广东省河源市龙川县第一中学2023-2024学年高二下学期期中考试化学试题
6 . 下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将硫酸滴入装有亚硫酸钠固体的培养皿。
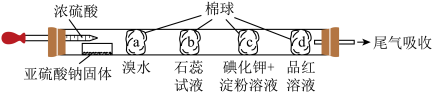
关于此实验的“现象”、“解释或结论”以及对应关系均正确的是

关于此实验的“现象”、“解释或结论”以及对应关系均正确的是
| 选项 | 现象 | 解释或结论 |
| A | a处黄色褪去 | 二氧化硫具有漂白性 |
| B | b处变为红色 | 二氧化硫与水反应生成酸性物质 |
| C | c处变为蓝色 | 二氧化硫具有一定的氧化性 |
| D | d处红色先褪去后恢复 | 二氧化硫具有漂白性且漂白性不稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
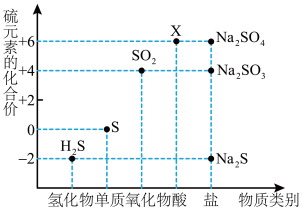
(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有_______ (填化学式)。
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目______ 。
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设 NA为阿伏加德罗常数的值。下列说法正确的是
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
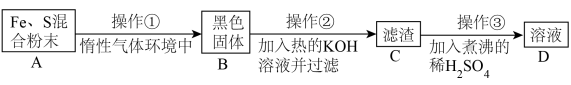
请回答以下问题:
(7)操作②的作用是_______ ,也可改用_______ 。
(8)混合粉末 A 中硫粉过量的原因是_______ 。
(9)下列溶液中通入SO2一定不会产生沉淀的是
(10)区别浓H2SO4和稀H2SO4,既简单又可靠的方法是

(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
| A.1mol 铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4LSO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 molNa2O2与足量H2O反应,转移的电子数为NA |
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:

请回答以下问题:
(7)操作②的作用是
(8)混合粉末 A 中硫粉过量的原因是
(9)下列溶液中通入SO2一定不会产生沉淀的是
| A.Ba(OH)2 | B.澄清石灰水 | C.Na2S | D.BaCl2 |
| A.各取少许溶液分别放入铜片 | B.分别与石蕊试液作用 |
| C.用玻璃棒各蘸少许液涂在纸上 | D.观察溶液的颜色 |
您最近一年使用:0次
名校
解题方法
8 . 第三代铝锂合金被用于国产大飞机的外壳,其用途与下列性质无关的是
| A.密度小 | B.耐腐蚀 | C.能导热 | D.强度大 |
您最近一年使用:0次
2023-04-05更新
|
207次组卷
|
4卷引用:专题01 化学与STSE
(已下线)专题01 化学与STSE上海市浦东新区2022-2023学年高三下学期4月模拟质量调研化学试题上海市浦东新区2023届高三下学期二模考试化学试题(已下线)上海市华东师范大学第二附属中学2022-2023学年高一下学期期中考试化学试题
9 . 海洋元素“溴”的单质及其化合物的用途广泛。
(1)Br原子的最外层电子排布式为_______ ,其中未成对电子的电子云形状为_______ 。
(2)能作为溴、碘元素原子得电子能力递变规律的判断依据是_______ (填序号)。
a.IBr中溴为﹣1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)从原子结构角度解释氯的非金属性强于溴的原因:_______ 。
(4)Br2和碱金属单质形成的MBr熔点如表:
NaBr的电子式_______ ,MBr熔点呈现表中趋势的原因是_______ 。
(5)海水提溴过程中,先向酸化的浓缩海水中通入_______ ,将其中的Br—氧化,再用“空气吹出法”吹出Br2,并用纯碱吸收:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),则吸收1mol Br2,转移电子_______ mol,反应中氧化产物为_______ 。
(6)随后用硫酸酸化吸收液,得到Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得Br2的质量减少,可能原因是_______ 。
(1)Br原子的最外层电子排布式为
(2)能作为溴、碘元素原子得电子能力递变规律的判断依据是
a.IBr中溴为﹣1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)从原子结构角度解释氯的非金属性强于溴的原因:
(4)Br2和碱金属单质形成的MBr熔点如表:
| MBr | NaBr | KBr | RbBr | CsBr |
| 熔点/℃ | 747 | 734 | 693 | 636 |
(5)海水提溴过程中,先向酸化的浓缩海水中通入
(6)随后用硫酸酸化吸收液,得到Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得Br2的质量减少,可能原因是
您最近一年使用:0次
解题方法
10 . 下列物质性质与用途不相应的是
A. 是一种红棕色粉末,可用作涂料 是一种红棕色粉末,可用作涂料 |
| B.液氮的沸点较低,可为超导材料提供低温环境 |
| C.石墨具有良好的润滑性,可用作电池电极材料 |
D. 与水混合成糊状后会很快凝固,可用作石膏绷带 与水混合成糊状后会很快凝固,可用作石膏绷带 |
您最近一年使用:0次



