解题方法
1 . 氟及其化合物用途非常广泛,自然界中氟多以化合态形式存在,形成的化合物有:N2F2、HBF4、 等。回答下列问题:
等。回答下列问题:
(1)氟元素基态原子最高能级电子的电子云形状为___________ ,下列为氟原子激发态的电子排布式的是___________ (填序号)。
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为___________ 。
②N2F2结构式为___________ ,其分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性___________ (填“增强”或“减弱”), 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的___________ (填“长”或“短”)。___________ ,设NA为阿伏加德罗常数的值则该晶体的密度为___________  (列出计算式)。
(列出计算式)。
 等。回答下列问题:
等。回答下列问题:(1)氟元素基态原子最高能级电子的电子云形状为
A.1s22s22p43s1 B.1s22s22p6 C.1s22s22p5 D.1s22s12p6
(2)F与N可形成化合物N2F2,分子中各原子均满足8电子稳定结构。
①分子中氮原子的杂化方式为
②N2F2结构式为
 键与
键与 键的数目之比为
键的数目之比为(3)氟硼酸(HBF4,属于强酸)可由HF和BF3化合生成,常用于替代浓硫酸作铅蓄电池的电解质溶液,从化学键形成角度分析HF与BF3能化合的原因
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物
 ,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,
,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比, 的导电性
的导电性 中C-C键的键长比石墨中C-C键的
中C-C键的键长比石墨中C-C键的
 (列出计算式)。
(列出计算式)。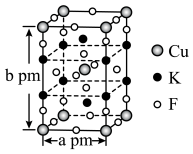
您最近一年使用:0次
解题方法
2 . 贵金属银有广泛用途。工业上用银锰精矿(主要含 、MnS、
、MnS、 等)制备银,同时获得二氧化锰的流程如下。
等)制备银,同时获得二氧化锰的流程如下。
(1)“浸锰”步骤中产生的浸锰液主要含有 ,生成气体的主要成分为
,生成气体的主要成分为_______ ;用惰性电极电解浸锰液制 ,写出电解总反应的化学方程式
,写出电解总反应的化学方程式_______ 。
(2)已知“浸铁”步骤中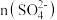 保持不变,反应中n(氧化剂):n(还原剂)=
保持不变,反应中n(氧化剂):n(还原剂)=_______ ;浸铁滤饼的主要成分为S和_______ 。
(3)“浸银”时发生反应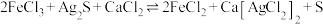 ,其中
,其中 在溶液中是一种稳定配合物。加入
在溶液中是一种稳定配合物。加入 的作用是
的作用是_______ ;结合离子方程式,从平衡角度分析选用氯化物浓溶液的原因是_______ 。
(4)“沉银”步骤中,生成单质银的离子反应方程式为_______ ,沉银液经处理可再利用,方法是向沉银液中通入_______ (写化学式),通过一步转化后循环再用。
 、MnS、
、MnS、 等)制备银,同时获得二氧化锰的流程如下。
等)制备银,同时获得二氧化锰的流程如下。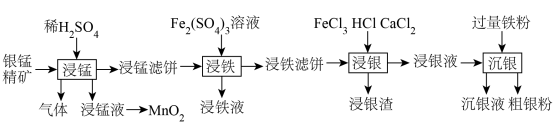
(1)“浸锰”步骤中产生的浸锰液主要含有
 ,生成气体的主要成分为
,生成气体的主要成分为 ,写出电解总反应的化学方程式
,写出电解总反应的化学方程式(2)已知“浸铁”步骤中
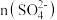 保持不变,反应中n(氧化剂):n(还原剂)=
保持不变,反应中n(氧化剂):n(还原剂)=(3)“浸银”时发生反应
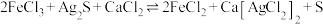 ,其中
,其中 在溶液中是一种稳定配合物。加入
在溶液中是一种稳定配合物。加入 的作用是
的作用是(4)“沉银”步骤中,生成单质银的离子反应方程式为
您最近一年使用:0次
3 . 钛被视为继铁、铝之后的第三金属,钛和钛的化合物在航天、化工、建筑、医疗中都有着广泛的用途。回答下列问题:
(1)基态钛原子核外电子有___________ 种空间运动状态,根据价电子排布图判断下列钛原子或离子电离一个电子所需能量最高的是___________ 。
A.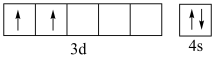 B.
B.
C. D.
D.
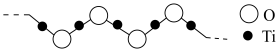
(2)硫酸氧钛是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为 。则该阳离子的化学式为
。则该阳离子的化学式为___________ 。 的VSEPR模型名称是
的VSEPR模型名称是___________ 。
(3)钣的配合物有多种。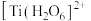 、
、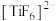 、
、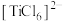 的配体中所含原子电负性由大到小的顺序是
的配体中所含原子电负性由大到小的顺序是___________ ,其中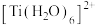 中
中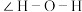
___________ (填写“大于”、“于”或“等于”)单个水分子中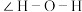 。
。
(4)有一种氮化钛晶体的晶胞与 晶胞相似,该晶体的晶胞参数为
晶胞相似,该晶体的晶胞参数为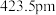 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为___________  。用
。用 掺杂
掺杂 后,其晶胞结构如图所示,距离
后,其晶胞结构如图所示,距离 最近的
最近的 有
有___________ 个。( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

(1)基态钛原子核外电子有
A.
 B.
B.
C.
 D.
D.
(2)硫酸氧钛是一种优良的催化剂,其阳离子为如图所示链状聚合形式的离子,聚合度为
 。则该阳离子的化学式为
。则该阳离子的化学式为 的VSEPR模型名称是
的VSEPR模型名称是
(3)钣的配合物有多种。
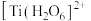 、
、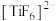 、
、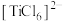 的配体中所含原子电负性由大到小的顺序是
的配体中所含原子电负性由大到小的顺序是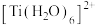 中
中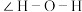
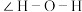 。
。(4)有一种氮化钛晶体的晶胞与
 晶胞相似,该晶体的晶胞参数为
晶胞相似,该晶体的晶胞参数为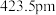 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为 。用
。用 掺杂
掺杂 后,其晶胞结构如图所示,距离
后,其晶胞结构如图所示,距离 最近的
最近的 有
有 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
4 . 氨的用途十分广泛,是制造硝酸和氮肥的重要原料。
(1)工业合成氨中,合成塔中每产生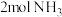 ,放出92.2kJ热量。
,放出92.2kJ热量。

1mol N-H键断裂吸收的能量约等于___________ kJ
(2)一定条件下,在恒温恒容的密闭容器中加入等物质的量 和
和 发生反应生成
发生反应生成 下列状态能说明反应达到平衡的是___________(填标号)。
下列状态能说明反应达到平衡的是___________(填标号)。
(3)以氨为原料生产尿素的方程式为 。
。
①为进一步提高 的平衡转化率,下列措施能达到目的的是
的平衡转化率,下列措施能达到目的的是___________ (填标号)。
A.增大 的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
②尿素的合成分两步进行:
a.
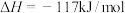
b.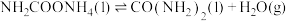

第一步反应速率快,可判断活化能较大的是___________ (填“第一步”或“第二步”)。
③某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的 和
和 发生反应:
发生反应: ,反应过程中混合气体中
,反应过程中混合气体中 的体积分数如下图所示。
的体积分数如下图所示。
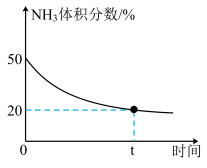
实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数
___________ (已知:分压=总压×体积分数)。
(4)中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。a、b、c、d均为Pt电极。
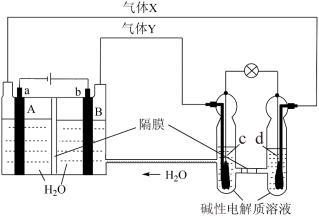
气体X为___________ ,A区pH___________ (填“变大”或“变小”或“不变”)图中右管中的 通过隔膜向
通过隔膜向___________ 电极移动(填“c”或“d”),c是___________ 极,电极上的电极反应为___________ 。
(1)工业合成氨中,合成塔中每产生
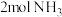 ,放出92.2kJ热量。
,放出92.2kJ热量。
1mol N-H键断裂吸收的能量约等于
(2)一定条件下,在恒温恒容的密闭容器中加入等物质的量
 和
和 发生反应生成
发生反应生成 下列状态能说明反应达到平衡的是___________(填标号)。
下列状态能说明反应达到平衡的是___________(填标号)。| A.容器内压强不变 | B. 的体积分数不变 的体积分数不变 |
| C.气体的密度不再改变 | D. |
(3)以氨为原料生产尿素的方程式为
 。
。①为进一步提高
 的平衡转化率,下列措施能达到目的的是
的平衡转化率,下列措施能达到目的的是A.增大
 的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂
的浓度 B.增大压强 C.及时转移生成的尿素 D.使用更高效的催化剂②尿素的合成分两步进行:
a.

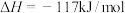
b.
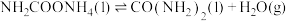

第一步反应速率快,可判断活化能较大的是
③某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的
 和
和 发生反应:
发生反应: ,反应过程中混合气体中
,反应过程中混合气体中 的体积分数如下图所示。
的体积分数如下图所示。
实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数

(4)中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。a、b、c、d均为Pt电极。

气体X为
 通过隔膜向
通过隔膜向
您最近一年使用:0次
解题方法
5 . α-甲基苯乙烯(AMS)在有机合成中用途广泛,如图是用苯为原料合成AMS并进一步制备香料龙葵醛的路线:_______ ;B中含氧官能团的名称为_______ 。
(2)写出反应③的方程式_______ 。
(3)检验龙葵醛中官能团可选择的试剂是_______ 。
(4)写出由B制备龙葵醛的化学反应方程式_______ 。
(5)AMS 可以自身聚合,写出该高聚物的结构简式:_______ 。
(6)B在一定条件下也可以直接制备AMS,反应所需条件为_______ 。
(7)写出符合下列条件的A的一种同分异构体的结构简式_______ 。
i.分子中含有3个甲基 ii.苯环上的一取代物只有1种
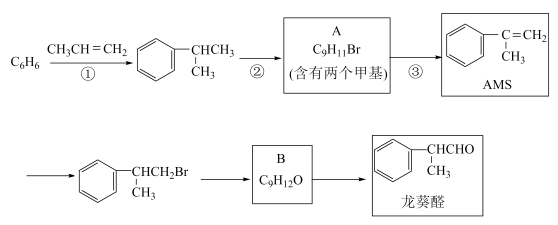
(2)写出反应③的方程式
(3)检验龙葵醛中官能团可选择的试剂是
(4)写出由B制备龙葵醛的化学反应方程式
(5)AMS 可以自身聚合,写出该高聚物的结构简式:
(6)B在一定条件下也可以直接制备AMS,反应所需条件为
(7)写出符合下列条件的A的一种同分异构体的结构简式
i.分子中含有3个甲基 ii.苯环上的一取代物只有1种
您最近一年使用:0次
名校
6 . 甲醇是一种基本的有机化工原料,用途十分广泛。应用 催化加氢规模化生产甲醇是综合利用
催化加氢规模化生产甲醇是综合利用 ,实现“碳达峰”的有效措施之一、我国科学家研究发现二氧化碳电催化还原制甲醇的反应
,实现“碳达峰”的有效措施之一、我国科学家研究发现二氧化碳电催化还原制甲醇的反应
 ,需通过以下两步实现:
,需通过以下两步实现:
I.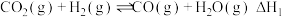
II.
反应过程中各物质的相对能量变化情况如图所示。
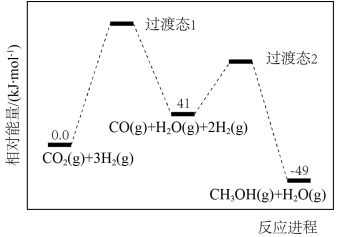
(1)
___________ ,稳定性:过渡态1___________ 过渡态2(填“大于”“小于”或“等于”)
(2)为探究该反应 ,进行如下实验:在一恒温、体积为
,进行如下实验:在一恒温、体积为 密闭容器中,充入
密闭容器中,充入 和
和 ,进行该反应(不考虑其它副反应)。
,进行该反应(不考虑其它副反应)。 时测得
时测得 和
和 的体积分数之比为
的体积分数之比为 且比值不再随时间变化。回答下列问题:
且比值不再随时间变化。回答下列问题:
①反应开始到平衡,
___________ 。
②该温度下的平衡常数
___________  (保留三位有效数字)。
(保留三位有效数字)。
③若上述反应过程中不断升高反应温度,下列图像正确的是___________ 。
A.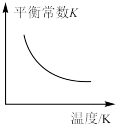 B.
B. C.
C.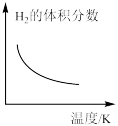 D.
D.
(3)基于催化剂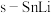 的
的 电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为
电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为___________ ,若电池工作 电极的质量变化为
电极的质量变化为 ,则理论上消耗
,则理论上消耗 的物质的量为
的物质的量为___________ 。

 催化加氢规模化生产甲醇是综合利用
催化加氢规模化生产甲醇是综合利用 ,实现“碳达峰”的有效措施之一、我国科学家研究发现二氧化碳电催化还原制甲醇的反应
,实现“碳达峰”的有效措施之一、我国科学家研究发现二氧化碳电催化还原制甲醇的反应 ,需通过以下两步实现:
,需通过以下两步实现:I.
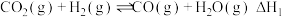
II.

反应过程中各物质的相对能量变化情况如图所示。

(1)

(2)为探究该反应
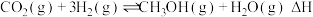 ,进行如下实验:在一恒温、体积为
,进行如下实验:在一恒温、体积为 密闭容器中,充入
密闭容器中,充入 和
和 ,进行该反应(不考虑其它副反应)。
,进行该反应(不考虑其它副反应)。 时测得
时测得 和
和 的体积分数之比为
的体积分数之比为 且比值不再随时间变化。回答下列问题:
且比值不再随时间变化。回答下列问题:①反应开始到平衡,

②该温度下的平衡常数

 (保留三位有效数字)。
(保留三位有效数字)。③若上述反应过程中不断升高反应温度,下列图像正确的是
A.
 B.
B. C.
C. D.
D.
(3)基于催化剂
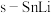 的
的 电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为
电催化制备甲酸盐同时释放电能的装置如图所示,该电池充电时,阳极的电极反应式为 电极的质量变化为
电极的质量变化为 ,则理论上消耗
,则理论上消耗 的物质的量为
的物质的量为
您最近一年使用:0次
2023-11-06更新
|
230次组卷
|
4卷引用:T28-原理综合题
名校
7 . 近年来甲醇用途日益广泛,越来越引起商家的关注。工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2 L密闭容器内,n(CO)和n(H2)按1:2 充入。在400 ℃时发生反应CO(g)+2H2(g) CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:
(1)图甲中表示CH3OH的变化的曲线是_______ (填序号)。
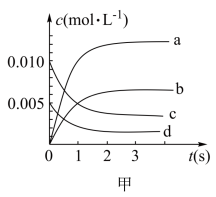
(2)此反应在前2s,H2 的反应速率是_______
(3)下列措施不能提高反应速率的有_______(填序号)。
(4)下列叙述能说明反应达到平衡状态的是_______ (填序号)。
a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1 mol CH3OH的同时有2 mol H-H键断裂
(5)CO(g)+2H2(g) CH3OH(g),此反应的平衡常数的表达式为:
CH3OH(g),此反应的平衡常数的表达式为:_____
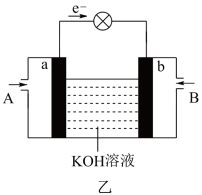
(6)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图乙所示,图中CH3OH从_______ (填“A”或“B”)处通入。
 CH3OH(g),体系中n(CO)随时间的变化如表:
CH3OH(g),体系中n(CO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |

(2)此反应在前2s,H2 的反应速率是
(3)下列措施不能提高反应速率的有_______(填序号)。
| A.升高温度 |
| B.加入催化剂 |
| C.增大压强 |
| D.及时分离出CH3OH |
a.CO和H2的浓度保持不变
b.v(H2)=2v(CO)
c.CO的物质的量分数保持不变
d.容器内气体密度保持不变
e.每生成1 mol CH3OH的同时有2 mol H-H键断裂
(5)CO(g)+2H2(g)
 CH3OH(g),此反应的平衡常数的表达式为:
CH3OH(g),此反应的平衡常数的表达式为:(6)CH3OH与O2的反应可将化学能转化为电能,其工作原理如图乙所示,图中CH3OH从

您最近一年使用:0次
2023·全国·模拟预测
名校
解题方法
8 . MnSO4·H2O是一种浅粉色晶体,易溶于水,不溶于乙醇,是饲料中常用的添加剂,也是电解制备锰及其他锰盐的原料,工业用途广泛。某同学设计如图甲所示实验装置制备硫酸锰。
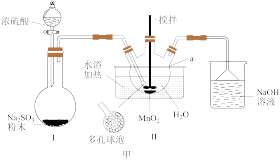
回答下列问题:
(1)仪器a的名称是_____ 。连接好实验仪器,装药品之前需进行的操作是______ 。
(2)装置Ⅱ中发生反应的化学方程式为_____ ;装置Ⅱ中水浴温度控制在80℃左右,温度过高时反应速率可能减慢的原因是______ 。
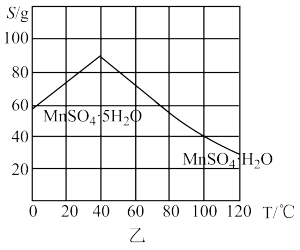
(3)结合图乙,分析反应后从溶液中获得MnSO4·H2O晶体的操作为_____ 、酒精洗涤、低温干燥。
(4)测定饲料中硫酸锰的含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应而消除其影响。然后加入指示剂,用硫酸亚铁铵[Fe(NH4)2(SO4)2]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关反应的离子方程式如下:
①2Mn2++NO +4PO
+4PO +2H+=2[Mn(PO4)2]3-+NO
+2H+=2[Mn(PO4)2]3-+NO +H2O;
+H2O;
②NH +NO
+NO =N2↓+2H2O;
=N2↓+2H2O;
③[Mn(PO4)2]3-+Fe2+=Mn2++[Fe(PO4)2]3-。
取ag饲料,消耗浓度为cmol•L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO4·H2O的质量分数为_____ %(用含a、c、V的式子表示)。若实验时未用标准溶液润洗滴定管,会导致测定结果_____ (填“偏大”“偏小”或“无影响”)。
(5)用惰性电极电解MnSO4酸性溶液可制得MnO2,请写出电解法制备MnO2时的阳极反应式:_____ 。

回答下列问题:
(1)仪器a的名称是
(2)装置Ⅱ中发生反应的化学方程式为
(3)结合图乙,分析反应后从溶液中获得MnSO4·H2O晶体的操作为

(4)测定饲料中硫酸锰的含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应而消除其影响。然后加入指示剂,用硫酸亚铁铵[Fe(NH4)2(SO4)2]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关反应的离子方程式如下:
①2Mn2++NO
 +4PO
+4PO +2H+=2[Mn(PO4)2]3-+NO
+2H+=2[Mn(PO4)2]3-+NO +H2O;
+H2O;②NH
 +NO
+NO =N2↓+2H2O;
=N2↓+2H2O;③[Mn(PO4)2]3-+Fe2+=Mn2++[Fe(PO4)2]3-。
取ag饲料,消耗浓度为cmol•L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO4·H2O的质量分数为
(5)用惰性电极电解MnSO4酸性溶液可制得MnO2,请写出电解法制备MnO2时的阳极反应式:
您最近一年使用:0次
2023-04-11更新
|
300次组卷
|
4卷引用:T26-实验综合题
(已下线)T26-实验综合题(已下线)化学押题卷(一)重庆市乌江新高考协作体2023-2024学年高三上学期第一次联合调研抽测(一模)化学试题河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题
名校
解题方法
9 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示:
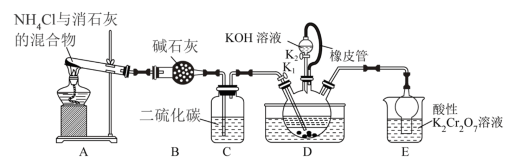
已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;②三颈烧瓶内盛放:CS2、水和催化剂。③CS2+3NH3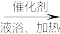 NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解。
NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解。
回答下列问题:
(1)装置A中反应的化学方程式是__ 。
(2)装置C的作用是__ 。
(3))制备KSCN溶液:熄灭A处的酒精灯,关闭K1,保持三颈烧瓶内液温105℃一段时间,然后打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN (发生复分解反应)的化学方程式:__ 。
(4)装置E的作用为吸收尾气(发生氧化还原反应),产生防止污染环境的气体是__ 。
(5)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压__ 、___ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
(6)测定晶体中KSCN的含量:称取10.0g样品。配成1000mL溶液量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液18.00mL。[已知:滴定时发生的反应:SCN-+Ag+=AgSCN↓(白色)。滴定过程的指示剂a为__ 。

已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;②三颈烧瓶内盛放:CS2、水和催化剂。③CS2+3NH3
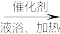 NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解。
NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解。回答下列问题:
(1)装置A中反应的化学方程式是
(2)装置C的作用是
(3))制备KSCN溶液:熄灭A处的酒精灯,关闭K1,保持三颈烧瓶内液温105℃一段时间,然后打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN (发生复分解反应)的化学方程式:
(4)装置E的作用为吸收尾气(发生氧化还原反应),产生防止污染环境的气体是
(5)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压
(6)测定晶体中KSCN的含量:称取10.0g样品。配成1000mL溶液量取20.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液18.00mL。[已知:滴定时发生的反应:SCN-+Ag+=AgSCN↓(白色)。滴定过程的指示剂a为
您最近一年使用:0次
10 . 关于合金的叙述,不正确的是
| A.合金的熔沸点一般比组成它们的各成分金属要高 |
| B.合金的硬度可以比原金属更高,化学性质也可能和原成分金属不同 |
| C.非金属和金属之间也可以形成合金 |
| D.合金的用途比纯金属的用途更广 |
您最近一年使用:0次
2018-03-26更新
|
1886次组卷
|
6卷引用:【全国百强校】四川省南充市阆中中学2020届高三化学选择题专项训练(30)
【全国百强校】四川省南充市阆中中学2020届高三化学选择题专项训练(30)(已下线)《2018-2019学年同步单元双基双测AB卷》 第三单元 金属及其化合物单元测试 B卷2017年普通高等学校招生统一考试化学(上海卷)人教版(2019)高一必修第一册 第三章素养检测(已下线)【浙江新东方】绍兴qw81西藏拉萨市第二高级中学2022-2023学年高一上学期期末考试化学试题



