名校
1 . 瑞舒伐他汀钙是治疗高血脂的常用药物,其中间体H的合成路线如下。
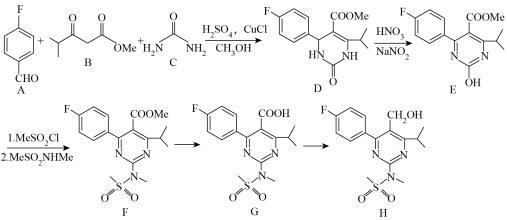
注:Me表示甲基
回答下列问题:
(1)D的分子式为___________ ,B中含有的官能团名称是___________ 。
(2)A+B+C→D的化学方程式是___________ 。
(3)E→F的反应类型为___________ 。实验室中完成F→G中官能团是转化需要的反应条件是___________ 。
(4)实现反应G→H,需要加入的反应试剂必须具有的性质是___________ 。
(5)X是A的一种同系物,X的相对分子质量比A大14,符合条件的X有___________ 种。
(6)用甲苯和适当的无机试剂(任选)合成对溴苯甲醛的流程如下:

①其中M和N的名称分别是___________ 、___________ 。
②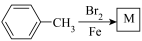 步骤中主要副产物的结构简式是
步骤中主要副产物的结构简式是___________ 。

注:Me表示甲基
回答下列问题:
(1)D的分子式为
(2)A+B+C→D的化学方程式是
(3)E→F的反应类型为
(4)实现反应G→H,需要加入的反应试剂必须具有的性质是
(5)X是A的一种同系物,X的相对分子质量比A大14,符合条件的X有
(6)用甲苯和适当的无机试剂(任选)合成对溴苯甲醛的流程如下:

①其中M和N的名称分别是
②
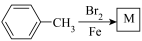 步骤中主要副产物的结构简式是
步骤中主要副产物的结构简式是
您最近一年使用:0次
名校
解题方法
2 . 由下列实验方案、现象得出的结论正确的是
| 实验方案 | 现象 | 结论 | |
| A | 向溴水中加入植物油,振荡后静置 | 水层颜色变浅 | 植物油可用于萃取溴水中的溴 |
| B | 向 溶液中加入乙醇 溶液中加入乙醇 | 析出深蓝色固体 |  在乙醇中溶解度小 在乙醇中溶解度小 |
| C | 用毛皮摩擦过的带电橡胶靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2为四面体结构 |
| D | 将氯气通入盛有鲜花的集气瓶中 | 鲜花褪色 | 氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-29更新
|
578次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题
名校
解题方法
3 . 有机电化学合成是一种有前景的绿色合成技术,利用电化学合成1,2-二氯乙烷的装置如图所示。若该装置工作时中间室NaCl溶液的浓度不变,电解时阴极生成气体的速率为xmol·h-1,下列说法错误的是
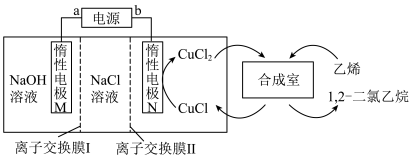

| A.惰性电极M为阴极 |
| B.离子交换膜Ⅰ为阳离子交换膜,离子交换膜Ⅱ为阴离子交换膜 |
C.合成室内发生的反应为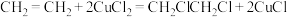 |
| D.中间室补充NaCl的速率为x mol⋅h-1 |
您最近一年使用:0次
名校
解题方法
4 . 化学与生产、生活、科技息息相关。下列说法错误的是
| A.臭氧是替代氯气的净水剂,为弱极性分子,在水中的溶解度小于在四氯化碳中的溶解度 |
| B.聚四氟乙烯树脂可用于制印刷电路板的底板,聚四氟乙烯是有机高分子材料 |
| C.通过清洁煤技术可减少煤燃烧造成的污染,有利于促进碳中和 |
| D.“北斗三星”采用星载氢原子钟,通过电子跃迁产生的电磁波校准时钟 |
您最近一年使用:0次
名校
解题方法
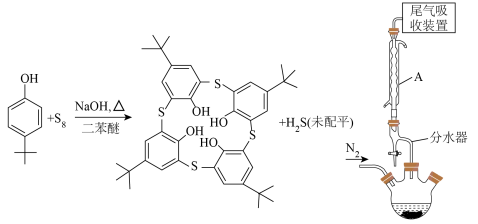
5 . 自分子识别兴起以来,冠醚、杯酚烃等的合成引起了研究者的广泛关注。硫代杯[4]芳烃已被应用于许多方面,如监测和分离一些阳离子、阴离子等。合成对叔丁基硫代杯[4]芳烃(M=720.0g⋅mol-1)的原理表示如下:
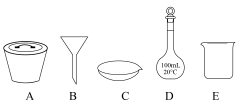
利用如图所示装置(加热、搅拌、夹持等装置省略),将60.00g对叔丁基苯酚、25.60gS8、8g氢氧化钠和40mL二苯醚加入500mL三颈烧瓶中,在N2气氛下磁力加热搅拌,逐步升温到230℃,温度保持在230℃反应4小时。停止加热并冷却至100℃以下后,加入40mL 6mol·L-1的盐酸和400mL乙醇的混合溶液,搅拌,抽滤,用乙醇和蒸馏水交替洗涤固体,得到粗产物。将粗产物在氯仿/乙醇中重结晶,得到30.24g纯化的对叔丁基硫代杯[4]芳烃。回答下列问题:
(1)仪器A的名称是___________ ,其作用是___________ 。
(2)对叔丁基邻苯二酚(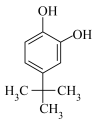 )的沸点小于2-叔丁基对苯二酚(
)的沸点小于2-叔丁基对苯二酚(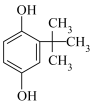 )的原因是
)的原因是___________ 。
(3)加热过程中要不断通入氮气,目的是___________ 。
(4)停止加热后,向反应器中加入盐酸和乙醇混合溶液的目的是___________ 。
(5)实验过程中会产生一种有毒气体,尾气吸收装置中应用___________ (填试剂名称)将该气体除去。
(6)在重结晶过程中,需要用到如图所示仪器中的___________ (填字母)___________ (计算结果精确到0.1%)。
利用如图所示装置(加热、搅拌、夹持等装置省略),将60.00g对叔丁基苯酚、25.60gS8、8g氢氧化钠和40mL二苯醚加入500mL三颈烧瓶中,在N2气氛下磁力加热搅拌,逐步升温到230℃,温度保持在230℃反应4小时。停止加热并冷却至100℃以下后,加入40mL 6mol·L-1的盐酸和400mL乙醇的混合溶液,搅拌,抽滤,用乙醇和蒸馏水交替洗涤固体,得到粗产物。将粗产物在氯仿/乙醇中重结晶,得到30.24g纯化的对叔丁基硫代杯[4]芳烃。回答下列问题:
(1)仪器A的名称是
(2)对叔丁基邻苯二酚(
 )的沸点小于2-叔丁基对苯二酚(
)的沸点小于2-叔丁基对苯二酚( )的原因是
)的原因是(3)加热过程中要不断通入氮气,目的是
(4)停止加热后,向反应器中加入盐酸和乙醇混合溶液的目的是
(5)实验过程中会产生一种有毒气体,尾气吸收装置中应用
(6)在重结晶过程中,需要用到如图所示仪器中的
您最近一年使用:0次
2024-03-10更新
|
621次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题
名校
解题方法
6 . 2023年2月17日NanoToday上报道的纳米酶是一种神奇的纳米材料,它具备天然酶的属性,能在温和条件下高效催化酶的底物,产生与天然酶相同的反应产物,并可作为酶的替代品调节细胞代谢,用于疾病的诊断和治疗。纳米酶分散到水中形成的分散系为胶体,其本质特征是
| A.能形成丁达尔效应 | B.粒子直径为1~100nm |
| C.可以透过滤纸 | D.可以透过半透膜 |
您最近一年使用:0次
名校
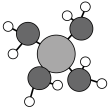
7 . 硅材料在生活中占有重要地位。Si(NH2)4(结构如图所示)受热分解可生成Si3N4和NH3。Si3N4是一种优良的耐高温结构陶瓷。下列有关说法错误的是

| A.电负性N>Si |
| B.Si3N4属于分子晶体 |
| C.基态Si和N原子的未成对电子数之比为2:3 |
| D.Si(NH2)4中的Si、N原子轨道的杂化类型相同 |
您最近一年使用:0次
2024-01-11更新
|
214次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高二下学期开学考试化学试题
解题方法
8 .  是合成荧光粉、光导体等的重要原料,
是合成荧光粉、光导体等的重要原料, 的开发与利用是科学界研究的热点。回答下列问题:
的开发与利用是科学界研究的热点。回答下列问题:
(1)已知: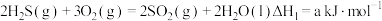 ,
,  ,则空气氧化脱除
,则空气氧化脱除 反应
反应 的
的
___________  。
。
(2)工业上可通过羰基硫(COS)与水蒸气在一定条件下反应制备 ,反应的原理为
,反应的原理为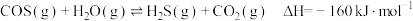 。
。
①T℃时,采用适当的催化剂在密闭容器中将等物质的量的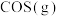 和
和 混合发生反应,已知该条件下该反应的平衡常数
混合发生反应,已知该条件下该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数可能为
的物质的量分数可能为___________ (填字母)
A.0.52 B.0.40 C.0.30 D.0.20
②图甲表示在两个相同的密闭容器中,反应物起始浓度相同,在相同质量不同型号的催化剂催化下,反应相同时间段时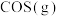 的转化率与温度的关系,则
的转化率与温度的关系,则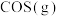 的平衡转化率
的平衡转化率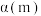
___________ 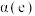 (填“
(填“ ”“
”“ ”或“
”或“ ”);q点时,
”);q点时,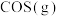 转化率出现突变的原因可能是
转化率出现突变的原因可能是___________ 。

③一定条件下进行该反应,测得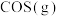 的平衡转化率与起始投料比
的平衡转化率与起始投料比 的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
___________ ,图中与c点的反应温度相同的点有___________ (填字母),若图中a、e两点对应的反应温度分别为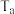 和
和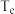 ,则
,则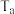
___________ 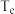 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。

(3)如图所示,质子固体电解质膜 燃料电池可对
燃料电池可对 废气进行资源化利用。
废气进行资源化利用。

电极a的电极反应式为___________ 。
 是合成荧光粉、光导体等的重要原料,
是合成荧光粉、光导体等的重要原料, 的开发与利用是科学界研究的热点。回答下列问题:
的开发与利用是科学界研究的热点。回答下列问题:(1)已知:
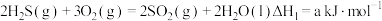 ,
,  ,则空气氧化脱除
,则空气氧化脱除 反应
反应 的
的
 。
。(2)工业上可通过羰基硫(COS)与水蒸气在一定条件下反应制备
 ,反应的原理为
,反应的原理为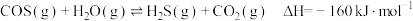 。
。①T℃时,采用适当的催化剂在密闭容器中将等物质的量的
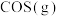 和
和 混合发生反应,已知该条件下该反应的平衡常数
混合发生反应,已知该条件下该反应的平衡常数 ,则平衡时体系中
,则平衡时体系中 的物质的量分数可能为
的物质的量分数可能为A.0.52 B.0.40 C.0.30 D.0.20
②图甲表示在两个相同的密闭容器中,反应物起始浓度相同,在相同质量不同型号的催化剂催化下,反应相同时间段时
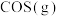 的转化率与温度的关系,则
的转化率与温度的关系,则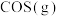 的平衡转化率
的平衡转化率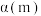
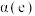 (填“
(填“ ”“
”“ ”或“
”或“ ”);q点时,
”);q点时,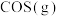 转化率出现突变的原因可能是
转化率出现突变的原因可能是
③一定条件下进行该反应,测得
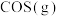 的平衡转化率与起始投料比
的平衡转化率与起始投料比 的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
的关系如图所示,图中各点对应的反应温度可能相同,也可能不相同,图中c点时反应的平衡常数
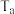 和
和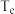 ,则
,则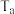
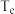 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(3)如图所示,质子固体电解质膜
 燃料电池可对
燃料电池可对 废气进行资源化利用。
废气进行资源化利用。
电极a的电极反应式为
您最近一年使用:0次
名校
解题方法
9 . X、Y、Z、W、Q为五种原子序数逐渐递增的短周期主族元素,五种元素分别位于三个周期,只有Z是金属元素且与X同族,W、Q相邻,常温时,测得 、Q简单氢化物的水溶液pH分别为11、1,以下有关说法正确的是
、Q简单氢化物的水溶液pH分别为11、1,以下有关说法正确的是
 、Q简单氢化物的水溶液pH分别为11、1,以下有关说法正确的是
、Q简单氢化物的水溶液pH分别为11、1,以下有关说法正确的是A.第一电离能: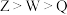 | B.简单氢化物的稳定性: |
C.氧化物对应的水化物酸性: | D.工业上可通过电解ZQ的水溶液来获得Z的单质 |
您最近一年使用:0次
2023-10-11更新
|
169次组卷
|
2卷引用:山西省九师联盟2022-2023学年高三上学期开学考试理综化学试题
解题方法
10 . 连花清瘟胶囊(颗粒)被批准可用于新冠病毒肺炎轻型、普通型引起的发热、咳嗽、乏力,其主要成分绿原酸转化为氢化绿原酸的反应如图所示。下列说法错误的是


| A.氢化绿原酸分子中含有3种含氧官能团 |
B.绿原酸可与 溶液反应产生 溶液反应产生 |
| C.一定量的氢化绿原酸分别与足量Na、NaOH溶液反应,消耗Na与NaOH物质的量之比为5:2 |
D.1mol绿原酸最多可与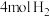 发生加成反应生成氢化绿原酸 发生加成反应生成氢化绿原酸 |
您最近一年使用:0次



