1 . 汽油不仅是一种燃料,也是一种重要的化工原料。汽油通过裂解可以得到乙烯、丙烯等气态物质,乙烯、丙烯可进一步合成丙烯酸乙酯。有关物质转化关系如下:
(1)丙烯酸乙酯的分子式是_______ 。
(2)有机物B中含氧官能团的名称是_______ 。
(3)久置的丙烯酸乙酯自身也会发生聚合反应,所得聚合物具有较好的弹性,可用于生产织物和皮革处理剂。该聚合反应的化学方程式是_______ 。
(4)下列说法正确的是_______。
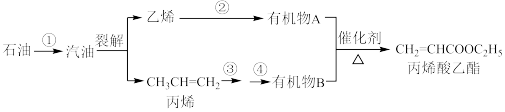
(1)丙烯酸乙酯的分子式是
(2)有机物B中含氧官能团的名称是
(3)久置的丙烯酸乙酯自身也会发生聚合反应,所得聚合物具有较好的弹性,可用于生产织物和皮革处理剂。该聚合反应的化学方程式是
(4)下列说法正确的是_______。
| A.步骤①是石油的分馏,属于化学变化 |
| B.步骤②的反应类型是加成反应 |
| C.相同质量的乙烯、丙烯完全燃烧,消耗的氧气质量相等 |
D.仅用 溶液无法鉴别有机物A、B和丙烯酸乙酯 溶液无法鉴别有机物A、B和丙烯酸乙酯 |
您最近一年使用:0次
2 . 请回答:
(1)①氮气的电子式是_______ ,②乙醛的结构简式是_______ 。
(2)过氧化钠与水反应的化学方程式是_______ 。
(3)乙烯在空气中燃烧,可观察到的现象是_______ 。
(1)①氮气的电子式是
(2)过氧化钠与水反应的化学方程式是
(3)乙烯在空气中燃烧,可观察到的现象是
您最近一年使用:0次
名校
3 . Ⅰ、体育比赛中当运动员肌肉挫伤或扭伤时,队医常用药剂氯乙烷(CH3CH2Cl)(沸点为12.27 ℃)对受伤部位进行局部冷却麻醉处理,工业上制取氯乙烷有两种方案:
a.CH3CH3+Cl2 CH3CH2Cl+HCl b.CH2=CH2+HCl
CH3CH2Cl+HCl b.CH2=CH2+HCl CH3—CH2Cl
CH3—CH2Cl
(1)你认为制备氯乙烷的最好方案为___________ (填“a”或“b”)。
Ⅱ、乙醇和乙酸是生活中常见的有机物。
(2)如图所示为乙醇的___________ (“空间充填”或“球棍”)模型。
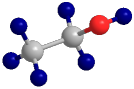
(3)乙醇中所含有的官能团的名称为___________ ,乙酸属于___________ (填“电解质”或“非电解质”)。
(4)用结构简式补全如图所示装置中乙醇和乙酸反应的化学方程式:CH3CH2OH+CH3COOH
___________ +H2O,该反应的类型为___________ 反应(填“取代”或“加成”),右侧小试管中应装有___________ 溶液(填“饱和Na2CO3”或“饱和NaOH”)。

a.CH3CH3+Cl2
 CH3CH2Cl+HCl b.CH2=CH2+HCl
CH3CH2Cl+HCl b.CH2=CH2+HCl CH3—CH2Cl
CH3—CH2Cl(1)你认为制备氯乙烷的最好方案为
Ⅱ、乙醇和乙酸是生活中常见的有机物。
(2)如图所示为乙醇的

(3)乙醇中所含有的官能团的名称为
(4)用结构简式补全如图所示装置中乙醇和乙酸反应的化学方程式:CH3CH2OH+CH3COOH


您最近一年使用:0次
名校
4 . 按要求填空或计算,(1)(2)小题为判断题。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。___________ (填“×”或“√”)
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。___________ (填“×”或“√”)
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性。
(4)Na与水反应,增大水的用量:反应速率___________ (选填“加快”、“减慢”、“不变”)。
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=___________ mol·L-1·min-1。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(4)Na与水反应,增大水的用量:反应速率
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=
您最近一年使用:0次
名校
5 . Ⅰ.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为_____ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=______ mol·L-1。
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C______ 具有(填“氧化性”或“还原性”)。
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为_____ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_____ 。
A.O2 B.FeCl2 C.KCl D.KMnO4
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KCl D.KMnO4
您最近一年使用:0次
2024-02-14更新
|
65次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高一上学期模拟预测化学试题
解题方法
6 . Na、Mg、Al、Fe、Cu、Zn是中学常见的金属率质,其合金在生活中有广泛应用。回答下列问题:
(1)实验室保存在煤油中的金属是___________ 。在潮湿空气中久置会生成绿色锈的金属是___________ 。
(2)铝合金广泛用于门窗,其耐腐蚀的主要原因是___________ 。
(3)一包钠铝合金与水恰好完全反应,收集到8960mLH₂(标准状况)。则这包合金中钠的物质的量为___________ ,铝的质量为___________ 。写出上述过程中涉及的两个反应的离子方程式:___________ 、___________ 。
(4)现有10g两种金属组成的合金与足量的稀硫酸反应产生11.2LH₂(标准状况)。则合金组成可能是___________(填字母)。
(5)等质量的镁、铝、锌与足量相同浓度的盐酸反应,产生H₂体积与时间关系如图所示。根据图像推知a、b、c曲线代表的金属依次是___________ (填元素符号)。
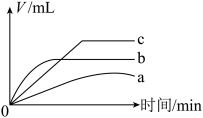
(1)实验室保存在煤油中的金属是
(2)铝合金广泛用于门窗,其耐腐蚀的主要原因是
(3)一包钠铝合金与水恰好完全反应,收集到8960mLH₂(标准状况)。则这包合金中钠的物质的量为
(4)现有10g两种金属组成的合金与足量的稀硫酸反应产生11.2LH₂(标准状况)。则合金组成可能是___________(填字母)。
| A.Mg和Cu | B.Al和Fe | C.Mg和Zn | D.Al和Cu |

您最近一年使用:0次
14-15高一上·福建泉州·阶段练习
名校
7 . 有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、KCl 等混合组成,为了检验它们所含的物质,做了以下实验.
①将固体溶于水,搅拌后得到无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,将沉淀置于稀硝酸中,发现沉淀全部溶解.
(1)试判断:固体混合物中肯定含有______ ,肯定没有_______ ,可能含有____ .
(2)对可能有的物质,可采用______ 来检验,如果含有该物质,其现象是_____________________ .
①将固体溶于水,搅拌后得到无色透明溶液;②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;③过滤,将沉淀置于稀硝酸中,发现沉淀全部溶解.
(1)试判断:固体混合物中肯定含有
(2)对可能有的物质,可采用
您最近一年使用:0次
解题方法
8 . 某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下系列实验,实验结果记录如下:
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)______ (填“相同”或“不同”)。
(2)对实验3完成下列填空:
①Al为______ 极,电极反应式为______ 。
②石墨为______ 极,电极反应式为______ 。
③电池总反应式为______
(3)实验4中Al作______ 极,理由是______ 。
(4)解释实验5中电流计偏向Al的原因______ 。
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
| 5 | Al、Cu | 浓硝酸 | 偏向Al |
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)
(2)对实验3完成下列填空:
①Al为
②石墨为
③电池总反应式为
(3)实验4中Al作
(4)解释实验5中电流计偏向Al的原因
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有
您最近一年使用:0次
2020-08-21更新
|
400次组卷
|
3卷引用:北京市人大附中朝阳学校2019~2020年高一下学期阶段练习化学试题(选考班)
北京市人大附中朝阳学校2019~2020年高一下学期阶段练习化学试题(选考班)贵州省贵阳市白云区第二高级中学2021-2022学年高一下学期期中考试化学试题(已下线)第18讲 原电池 化学电源(练)-2023年高考化学一轮复习讲练测(全国通用)
名校
9 . 一定温度下,在容积为VL的密闭容器中进行反应:n N(g) m M(g),M、N的物质的量随时间的变化曲线如图所示:
m M(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中n:m=_________ 。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为________ 。
(3)在a、b、c点中,表示正反应速率大于逆反应速率的点有:__________ 。
(4)下列叙述中能说明上述反应达到平衡状态的是_______ ( 填选项字母)
A.反应中M与N的物质的量之比为1:1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗n mol N,同时生成m mol M
 m M(g),M、N的物质的量随时间的变化曲线如图所示:
m M(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中n:m=
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为
(3)在a、b、c点中,表示正反应速率大于逆反应速率的点有:
(4)下列叙述中能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1:1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗n mol N,同时生成m mol M
您最近一年使用:0次
2020-08-17更新
|
443次组卷
|
3卷引用:河北省石家庄市第二中学2019-2020高一下学期期末考试模拟(四)化学试题
河北省石家庄市第二中学2019-2020高一下学期期末考试模拟(四)化学试题(已下线)第02章 化学反应的方向、限度与速率(A卷基础强化卷)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)章末检测卷(二)化学反应的方向、限度与速率
10 . 钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:_____________
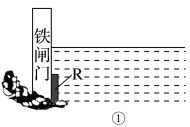
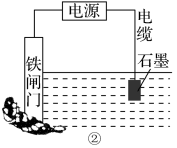
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用________ 。
A.铜 B.钠 C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的__________ 极。
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如图所示:
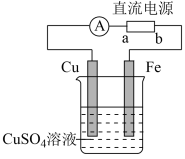
①电镀装置图的“直流电源”中,______  填“a”或“b”
填“a”或“b” 是正极。Fe电极反应式为
是正极。Fe电极反应式为_________ ;
②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为________ 。
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:______ 。


(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的正极电极反应式为:
(2)为了降低某水库的铁闸门被腐蚀的速率,可以采用图①所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(3)图②所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
(4)钢铁的防护除了用电化学保护方法之外,在钢铁制品表面镀铜也可以有效地防止其腐蚀,电镀的装置如图所示:

①电镀装置图的“直流电源”中,
 填“a”或“b”
填“a”或“b” 是正极。Fe电极反应式为
是正极。Fe电极反应式为②接通电源前,装置图中的铜、铁两个电极质量相等,电镀完成后,将两个电极取出,用水小心冲洗干净、烘干,然后称量,二者质量之差为5.12g,由此计算电镀过程中电路中通过电子的物质的量为
③上述铁镀件破损后,铁更容易被腐蚀。请简要说明镀铜铁镀件破损后,铁更容易被腐蚀的原因:
您最近一年使用:0次



