1 . 为了测定镁铝合金中各成分金属的含量,可采取以下两种方法:
(1)将8g镁铝合金样品投入足量的氢氧化钠溶液中充分反应后,过滤,得滤渣4.4g,则合金样品中铝的质量分数为_______ 。
(2)在标准状况下进行甲、乙、丙三组实验:各取200mL同浓度的盐酸,加入不同质量的同一种镁铝合金粉末,产生气体,有关数据记录如下:
则盐酸的物质的量浓度为____ (保留三位有效数字),合金中镁铝的物质的量之比____ 。
(1)将8g镁铝合金样品投入足量的氢氧化钠溶液中充分反应后,过滤,得滤渣4.4g,则合金样品中铝的质量分数为
(2)在标准状况下进行甲、乙、丙三组实验:各取200mL同浓度的盐酸,加入不同质量的同一种镁铝合金粉末,产生气体,有关数据记录如下:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 2.55 | 3.85 | 4.59 |
| 生成气体体积/L | 2.80 | 3.36 | 3.36 |
则盐酸的物质的量浓度为
您最近一年使用:0次
解题方法
2 . 测定冶金级高纯硅中铁元素的含量:将mg样品用氢氟酸和硝酸溶解处理,配成V mL溶液,用羟胺(NH2OH,难电离)将Fe3+还原为Fe2+后,加入邻二氮菲,形成橙红色物质。利用吸光度法测得吸光度为0.500(吸光度与Fe2+浓度的关系曲线如图所示)。
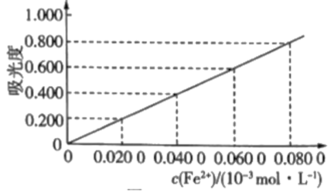
(1)酸性条件下,羟胺将Fe3+还原为Fe2+,同时产生一种无污染气体,该反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数表达式为___________ (用字母表示)。

(1)酸性条件下,羟胺将Fe3+还原为Fe2+,同时产生一种无污染气体,该反应的离子方程式为
(2)样品中铁元素的质量分数表达式为
您最近一年使用:0次
名校
解题方法
3 . 三聚氰胺最早被李比希于1834年合成,它有毒,不可用于食品加工或食品添加剂。经李比希法分析得知,三聚氰胺分子中,氮元素的含量高达66.67%,氢元素的质量分数为4.76%,其余为碳元素。它的相对分子质量大于100,但小于150。试回答下列问题:
(1)分子式中原子个数比N(C)∶N(H)∶N(N)=_____________ 。
(2)三聚氰胺分子中碳原子数为_____________ ,理由是(写出计算式)_____________ 。
(3)三聚氰胺的分子式为_____________ 。
(4)若核磁共振氢谱显示只有1个吸收峰,红外光谱表征有1个由碳氮两种元素组成的六元杂环。则三聚氰胺的结构简式为______ 。
(1)分子式中原子个数比N(C)∶N(H)∶N(N)=
(2)三聚氰胺分子中碳原子数为
(3)三聚氰胺的分子式为
(4)若核磁共振氢谱显示只有1个吸收峰,红外光谱表征有1个由碳氮两种元素组成的六元杂环。则三聚氰胺的结构简式为
您最近一年使用:0次
2020-07-30更新
|
546次组卷
|
4卷引用:课后-1.2.2 有机化合物分子式和分子结构的确定-人教2019选择性必修3
解题方法
4 . 奶粉中蛋白质含量的国家标准是:每100g婴幼儿奶粉中含蛋白质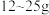 。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取
。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取 该奶粉样品进行反应后,生成的
该奶粉样品进行反应后,生成的 和
和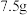 质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于
质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于________ (填“合格”或“不合格”)奶粉。
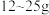 。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取
。其测定方法是:奶粉经水解产生氨基酸,再经过其他反应生成氨,由氨计算出氮,再由氮求出蛋白质的含量(蛋白质的含氮量按16%计算)。某市质检局对市场中某个品牌的婴幼儿奶粉进行检验,取 该奶粉样品进行反应后,生成的
该奶粉样品进行反应后,生成的 和
和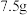 质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于
质量分数为19.6%的稀硫酸能恰好完全反应生成正盐,该品牌的婴幼儿奶粉属于
您最近一年使用:0次
解题方法
5 . 现有一块部分被氧化为氧化钠的钠块,其质量为10.8g,将它投入一定量的水中完全反应,最终得到含16g溶质的氢氧化钠溶液,回答下列问题:
(1)反应中生成的氢气为______ mol。
(2)钠的质量为______ g。
(3)被氧化的钠的质量为______ g。
(4)氧化钠的质量分数为______ (保留三位有效数字)。
(1)反应中生成的氢气为
(2)钠的质量为
(3)被氧化的钠的质量为
(4)氧化钠的质量分数为
您最近一年使用:0次
2022-12-09更新
|
251次组卷
|
3卷引用:作业(二十) 物质的量在化学方程式计算中的应用
作业(二十) 物质的量在化学方程式计算中的应用云南省大理市黄冈实验中学2021-2022学年高一上学期12月月考化学试题(已下线)【定心卷】3.2.2 物质的量在化学方程式计算中的应用随堂练习-人教版2023-2024学年必修第一册
解题方法
6 . 质量分数为25%的浓氨水,密度是0.91g•cm-3。用等体积水稀释,所得氨水的质量分数是多少____ ?若稀释后的氨水密度是0.95g•cm-3,试计算它的物质的量浓度____ 。
您最近一年使用:0次
解题方法
7 . 某研究小组通过以下方法测定某铁矿石样品(主要成分为 )中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
)中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数___________ 。(假设杂质不与盐酸反应)
 )中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
)中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
您最近一年使用:0次
8 . 蛋白质在一定条件下与浓硫酸反应可转化为硫酸铵,后者在浓氢氧化钠溶液和水蒸气作用下,其中的氮元素可转化为氨放出。现用30.0mL牛奶进行上述实验,将牛奶中蛋白质里的氮元素完全转化成氨,再用50.0mL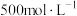 硫酸溶液吸收放出的氨,剩余的酸用38.0mL
硫酸溶液吸收放出的氨,剩余的酸用38.0mL 氢氧化钠溶液可恰好完全中和。
氢氧化钠溶液可恰好完全中和。
(1)30.0mL牛奶中共含有_______ 克氮?
(2)如果牛奶中蛋白质含氮16%(质量分数),则牛奶中蛋白质的质量分数是______ ?(已知牛奶的密度是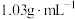 )
)
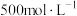 硫酸溶液吸收放出的氨,剩余的酸用38.0mL
硫酸溶液吸收放出的氨,剩余的酸用38.0mL 氢氧化钠溶液可恰好完全中和。
氢氧化钠溶液可恰好完全中和。(1)30.0mL牛奶中共含有
(2)如果牛奶中蛋白质含氮16%(质量分数),则牛奶中蛋白质的质量分数是
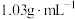 )
)
您最近一年使用:0次
解题方法
9 . 碳酸钠和碳酸氢钠是用途广泛的化合物。在实验室中,充分加热碳酸钠和碳酸氢钠的混合物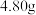 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为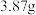 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数_______ 。
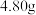 ,完全反应后称得剩余固体质量为
,完全反应后称得剩余固体质量为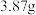 ,求混合物中碳酸氢钠的质量分数
,求混合物中碳酸氢钠的质量分数
您最近一年使用:0次
解题方法
10 . 利用碘量法测定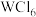 产品纯度,实验如下:
产品纯度,实验如下:
①称量:将足量CS2(易挥发)加入干燥的称量瓶中,盖紧称重为m1g;开盖并计时1分钟,盖紧称重为m2g;再开盖加入待测样品并计时1分钟,盖紧称重为m3g,则样品质量为_______ g(不考虑空气中水蒸气的干扰)。
②滴定:先将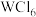 转化为可溶的
转化为可溶的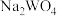 ,通过
,通过 离子交换柱发生反应:
离子交换柱发生反应: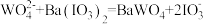 ;交换结束后,向所得含
;交换结束后,向所得含 的溶液中加入适量酸化的KI溶液,发生反应:
的溶液中加入适量酸化的KI溶液,发生反应: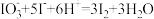 ;反应完全后,用
;反应完全后,用 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。滴定达终点时消耗
。滴定达终点时消耗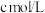 的
的 溶液VmL,则样品中
溶液VmL,则样品中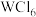 (摩尔质量为Mg/mol)的质量分数为
(摩尔质量为Mg/mol)的质量分数为_______ 。称量时,若加入待测样品后,开盖时间超过1分钟,则滴定时消耗 溶液的体积将
溶液的体积将_______ (填“偏大”“偏小”或“不变”),样品中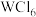 质量分数的测定值将
质量分数的测定值将_______ (填“偏大”“偏小”或“不变”)。
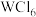 产品纯度,实验如下:
产品纯度,实验如下:①称量:将足量CS2(易挥发)加入干燥的称量瓶中,盖紧称重为m1g;开盖并计时1分钟,盖紧称重为m2g;再开盖加入待测样品并计时1分钟,盖紧称重为m3g,则样品质量为
②滴定:先将
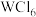 转化为可溶的
转化为可溶的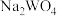 ,通过
,通过 离子交换柱发生反应:
离子交换柱发生反应: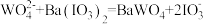 ;交换结束后,向所得含
;交换结束后,向所得含 的溶液中加入适量酸化的KI溶液,发生反应:
的溶液中加入适量酸化的KI溶液,发生反应: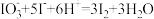 ;反应完全后,用
;反应完全后,用 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: 。滴定达终点时消耗
。滴定达终点时消耗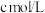 的
的 溶液VmL,则样品中
溶液VmL,则样品中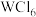 (摩尔质量为Mg/mol)的质量分数为
(摩尔质量为Mg/mol)的质量分数为 溶液的体积将
溶液的体积将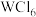 质量分数的测定值将
质量分数的测定值将
您最近一年使用:0次



