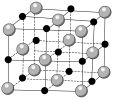
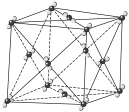
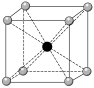
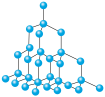
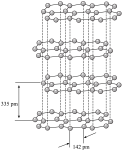
1 . 下图表示一些晶体中的某些结构,它们分别是NaCl、干冰、CsCl、金刚石、石墨晶体结构中的某一种的某一部分。
(1)代表金刚石的是___________ (填字母,下同),金刚石属于___________ 晶体,其中每个碳原子采取___________ 杂化轨道形成共价键三维骨架结构。
(2)代表石墨的是___________ ,石墨属于混合型晶体。石墨晶体是层状结构,其中每个正六边形占有碳原子数平均为___________ 个。层间没有化学键相连,是靠___________ 维系的。
(3)代表NaCl晶体的是___________ ,每个Cl―紧邻着___________ 个Na+。每个晶胞中有___________ 个Na+。
(4)代表CsCl晶体的是___________ ,它属于___________ 晶体。每个Cs+紧邻着___________ 个Cl―。
(5)代表干冰的是___________ ,它属于___________ 晶体,每个CO2分子与___________ 个CO2分子紧邻。
|
|
|
| A | B | C |
|
| |
| D | E |
(1)代表金刚石的是
(2)代表石墨的是
(3)代表NaCl晶体的是
(4)代表CsCl晶体的是
(5)代表干冰的是
您最近一年使用:0次
2 . 下列化学用语表示不正确 的是
A.Mg2+的结构示意图: |
B.基态氧原子的轨道表示式: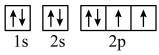 |
| C.S2-的电子排布式:1s22s22p63s23p4 |
| D.基态铬原子(24Cr)的 |
您最近一年使用:0次
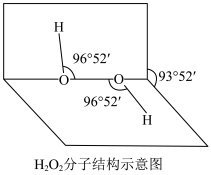
3 . H2O2是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。H2O2的电子式是___________ ,结构式是___________ 。含有___________ 键和___________ 键的___________ 分子(填“极性”或“非极性”)。H2O2能与水混溶,却不溶于CCl4。请予以解释:___________ 。
您最近一年使用:0次
解题方法
4 . 电负性与电离能是两种定量描述元素原子得失电子能力的参数,请根据下列数据回答问题。
(1)非金属性:S___________ (填“>”、“=”或“<”)F。
(2)依据电负性数值,上述元素中最容易形成离子键的是___________ 和___________ 。
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为___________ ,通过分析电负性的变化规律,确定Y元素电负性的取值范围是___________ 。
(4)由电负性数据推断:化合物PBr3中P的化合价为___________ 。已知PBr3与水反应是非氧化还原反应,写出PBr3与水反应的化学方程式___________ 。
| 元素符号 | Li | Be | C | O | F | Na | Al | P | S | Br |
| 电负性 | 1.0 | 1.5 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 2.2 | 2.5 | 2.8 |
(2)依据电负性数值,上述元素中最容易形成离子键的是
(3)已知某主族元素Y,其基态原子核外有2个电子层,3个未成对电子,Y元素基态原子的轨道表示式为
(4)由电负性数据推断:化合物PBr3中P的化合价为
您最近一年使用:0次
5 . 碳化硅(SiC)的一种晶体具有类似金刚石的结构,其中碳原子与硅原子的位置是交替的,在下列三种晶体中,它们的熔点从高到低的顺序是
①金刚石 ②晶体硅 ③碳化硅
①金刚石 ②晶体硅 ③碳化硅
| A.①③② | B.②③① | C.③①② | D.②①③ |
您最近一年使用:0次
解题方法
6 . 请按要求完成填空:
(1)完成下表中的空白:
(2)配合物[Cu(NH3)4]SO4的中心离子是___________ 、配体是___________ 、配位原子是___________ 、配位数是___________ 。
(1)完成下表中的空白:
| 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | VSEPR模型 | 空间结构 |
| CO2 | ① | ② | ③ | ④ |
SO | ⑤ | ⑥ | ⑦ | ⑧ |
您最近一年使用:0次
7 . 如图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列说法不正确 的是
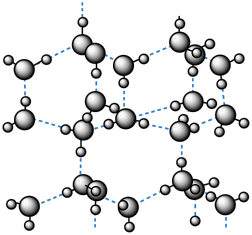
| A.水分子间存在O―H···O作用力 |
| B.冰中1个水分子通过氢键与4个水分子相连,冰中水分子与氢键的数目之比为1:4 |
| C.冰融化要破坏范德华力和氢键 |
| D.液态水结成冰时的体积变大与氢键具有方向性有关 |
您最近一年使用:0次
解题方法
8 . 下列说法中,正确的是
| A.σ键由原子轨道“头碰头”形成 | B.π键由原子轨道“头碰头”形成 |
| C.π键电子云形状为轴对称 | D.共价三键由两个σ键和一个π键构成 |
您最近一年使用:0次
解题方法
9 . 单质碘的熔、沸点较低,其原因是
| A.碘的非金属性强 | B.碘分子中键能较小 |
| C.固态碘单质中碘分子间以范德华力结合 | D.I-I共价键的键长较长 |
您最近一年使用:0次
解题方法
10 . 下列说法中,不正确 的是
| A.键长和键角决定分子的空间结构 |
| B.两个原子之间形成共价键时,最多有一个σ键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.键长与键能是衡量分子稳定性的两个参数 |
您最近一年使用:0次