1 . 按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物:

| A | B |
|
|
| 步骤① | 步骤② |
| C | D |
|
|
| 步骤③ | 步骤④ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
88次组卷
|
17卷引用:福建省泉州第一中学2022-2023学年高三上学期期中考试化学试题
福建省泉州第一中学2022-2023学年高三上学期期中考试化学试题山东省枣庄市滕州市第一中学2022-2023学年高三上学期10月考试化学试题上海市华东师范大学附属东昌中学2022-2023学年高一上学期12月阶段考化学试题山东省济南市历城区第一中学2020届高三12月检测化学试题江西省南昌市进贤县第一中学2020-2021学年高二下学期第二次月考化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一上学期10月学业质量检测化学试题上海市晋元高级中学2021-2022学年高一上学期期中考试化学试题上海交通大学附属中学2021-2022学年高一上学期期中测试化学试题(已下线)专题34 基本实验仪器和基本操作(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练广东省深圳市盐田高级中学2022-2023学年高二下学期第一次月考化学试题 广东省珠海市斗门区第一中学2022-2023学年高二下学期期中考试化学试题江西省宜春市宜丰中学2022-2023学年高二下学期3月月考化学试题(已下线)第02讲 研究有机化合物的一般方法-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)广东省深圳市盐田高级中学2023-2024学年高二下学期4月月考化学试题重庆市松树桥中学校2023-2024学年高二下学期期中考试化学试题浙江省杭州市学军中学2023-2024学年高三下学期5月阶段性考试安徽省蚌埠第二中学2023-2024学年高二下学期5月期中考试化学试题
2 . 一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是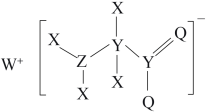
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近一年使用:0次
2024-04-08更新
|
97次组卷
|
14卷引用:福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题
福建省三明市五县2021-2022学年高二下学期联合质检考试(期中)化学试题厦门外国语学校2021-2022学年高二下学期期中考试化学试题湖北省黄冈市麻城市第二中学2021-2022学年高二下学期3月月考化学试题 吉林省吉林第一中学2022-2023学年高二上学期11月月考化学试题福建省龙岩市一级校联盟2022-2023学年高二下学期4月期中考试化学试题福建省三明第一中学2022-2023学年高二下学期期中考试化学试题福建省厦门市湖滨中学2022-2023学年高二下学期期中考试化学试题云南省大理州实验中学2021-2022学年高二下学期化学期中考试题山东省德州市2020-2021学年高二下学期期末考试化学试题陕西省武功县普集高级中学2022-2023学年高二下学期第一次月考化学试题广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题2024届高考化学考点剖析精创专题卷——专题七 物质结构 元素周期律四川省达州市万源中学2023-2024学年高二下学期4月月考化学试题河南省郑州市十校2023-2024学年高二下学期期中联考化学试卷
11-12高二下·甘肃天水·阶段练习
名校
解题方法
3 . 碳化硅的一种晶体(SiC)具有类似金刚石的结构,其中碳原子和硅原子的位置是交替的。下列三种晶体:①金刚石②晶体硅③碳化硅中,它们的熔点由高到低的顺序是
| A.①③② | B.②③① | C.③①② | D.②①③ |
您最近一年使用:0次
2024-04-02更新
|
238次组卷
|
17卷引用:福建省莆田第十五中学2021-2022学年高二下学期期中考试化学试题
福建省莆田第十五中学2021-2022学年高二下学期期中考试化学试题2014-2015福建省漳浦县三校高二下学期期中化学试卷福建省莆田第二十五中学2019-2020学年高二下学期返校考试化学试题宁夏青铜峡市宁朔中学2021-2022学年高二3月月考化学试题云南省蒙自一中2021-2022学年高二下学期3月份考试化学试题(已下线)2011-2012学年甘肃省甘谷一中高二下学期第二次月考化学试卷(已下线)2012-2013学年吉林省龙井市三中高二下学期期中考试化学试卷2015-2016学年山西阳泉十五中高三第一次阶段考试化学试卷河北省馆陶县第一中学2016-2017学年高二下学期期中考试化学试题人教版2017-2018学年高二化学选修三同步训练:3.2 分子晶体与原子晶体(第2课时)贵州省遵义市正安县第一中学2018-2019学年高二上学期期中考试化学试题江苏省泗阳县众兴中学2020-2021学年高二上学期10月月考化学试题江苏省泗阳县实验高级中学2021-2022学年高二上学期第一次质量调研化学试题(已下线)第三章章节专项提升河南省焦作市2022-2023学年第四中学高二下学期期中考试 化学试卷(已下线)3.2.2 共价晶体课堂例题(已下线)单项选择题1-5
名校
解题方法
4 . 现有下列物质:①生石灰;② 固体;③
固体;③ 溶液;④单质铁;⑤
溶液;④单质铁;⑤ ;⑥熔融
;⑥熔融 ;⑦石墨;⑧蔗糖晶体;⑨
;⑦石墨;⑧蔗糖晶体;⑨ 固体;⑩
固体;⑩ 固体;⑪漂白粉。请填空:
固体;⑪漂白粉。请填空:
(1)上述状态下可导电的物质是________ (填标号,下同),属于电解质的是________ 。
(2)上述物质中属于碱性氧化物的是________ (填化学式),原因为_________ (请用化学方程式说明)。
(3)⑥的电离方程式为________ ,⑩溶于水时的电离方程式为________ 。
(4)②的水溶液与④反应的离子方程式为________ ,②与⑨的水溶液混合后,溶液恰好呈中性,发生反应的离子方程式为__________ 。
(5)写出⑪在空气中变质的化学方程式___________ 。
 固体;③
固体;③ 溶液;④单质铁;⑤
溶液;④单质铁;⑤ ;⑥熔融
;⑥熔融 ;⑦石墨;⑧蔗糖晶体;⑨
;⑦石墨;⑧蔗糖晶体;⑨ 固体;⑩
固体;⑩ 固体;⑪漂白粉。请填空:
固体;⑪漂白粉。请填空:(1)上述状态下可导电的物质是
(2)上述物质中属于碱性氧化物的是
(3)⑥的电离方程式为
(4)②的水溶液与④反应的离子方程式为
(5)写出⑪在空气中变质的化学方程式
您最近一年使用:0次
名校
5 . 反应H2S(g)+CO2(g) COS(s)+H2O(g)可用于制备有机化工原料COS。已知240℃时,其化学反应平衡常数K=1。
COS(s)+H2O(g)可用于制备有机化工原料COS。已知240℃时,其化学反应平衡常数K=1。
①一定温度下,设起始充入的(CO2):(H2S)=m相同时间内测得H2S转化率与m和温度(T)的关系如图甲所示。
②起始密闭容器中w[H2S(g)]和w[CO2(g)]、w[COS(g)]和w[H2O(g)]分别相等。在300℃、320℃时上述反应中,H2S(g)和COS(g)的体积分数(w)随时间(t)的变化关系如图。(从上到下依次为L1,L2,L3,L4)

下列说法错误的是
 COS(s)+H2O(g)可用于制备有机化工原料COS。已知240℃时,其化学反应平衡常数K=1。
COS(s)+H2O(g)可用于制备有机化工原料COS。已知240℃时,其化学反应平衡常数K=1。①一定温度下,设起始充入的(CO2):(H2S)=m相同时间内测得H2S转化率与m和温度(T)的关系如图甲所示。
②起始密闭容器中w[H2S(g)]和w[CO2(g)]、w[COS(g)]和w[H2O(g)]分别相等。在300℃、320℃时上述反应中,H2S(g)和COS(g)的体积分数(w)随时间(t)的变化关系如图。(从上到下依次为L1,L2,L3,L4)

下列说法错误的是
| A.该反应的△H<0 |
| B.m1>m2 |
| C.绝热恒容条件下发生反应。若反应起始,H2S与CO2按物质的量比1∶1、温度240℃下投入反应体系,则达平衡状态时,H2S的转化率小于50% |
| D.300℃时w[COS(g)]随时间变化的曲线为L1,320℃时w[H2S(g)]随时间变化的曲线为L3 |
您最近一年使用:0次
6 . 将电能转化为化学能在生活生产和科学研究中具有重要意义。某学习小组用石墨电极持续电解CuCl2溶液。
【实验探究】
(1)t1~t3,b极产生的气体有刺激性气味,用湿润的碘化钾淀粉试纸检验,试纸变蓝,气体是_______ 。
(2)t1时刻,a极析出铜的电极反应式为_______ 。
(3)从a极刮取白色沉淀(含少量红色固体),经检验含CuCl、Cu。
已知:Cu+ Cu+Cu2+,CuOH(黄色,不溶)→Cu2O(红色,不溶)
Cu+Cu2+,CuOH(黄色,不溶)→Cu2O(红色,不溶)
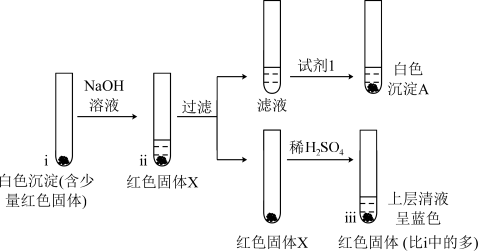
①白色沉淀A为AgCl,试剂1是_______ 。
②向试管i中加入NaOH溶液,生成的黄色沉淀很快转变为红色。解释该现象的化学方程式为_______ 。
③证实从a极刮取的白色沉淀中含有CuCl的理由是_______ 。
(4)针对CuCl沉淀是如何产生的,小组提出两种假设。
假设1:由电极反应产生:Cu2++Cl-+e-=CuCl↓。
假设2:除电极反应外,也可由氧化还原反应产生CuCl,请用离子方程式说明:_______ 。
(5)t1时a极未产生气体,而t3时a极产生气体。原因是_______ 。
【应用实践】
(6)镀铜工业中,电镀液以CuSO4、H2SO4为主,同时含Cl-和添加剂。过多的Cl-会使镀层出现白色胶状薄膜。电镀前向电镀液中加入适量Ag2SO4(微溶)固体能有效解决该问题,解释Ag2SO4的作用_______ ;若加入AgNO3,固体效果是否会更好,说明理由_______ 。
【实验探究】
| 实验 | 时刻 | 现象 |
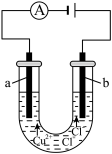 | t1 | a极析出红色固体;b极产生气体 |
| t2 | a极产生白色沉淀;a极附近溶液变为黄绿色;b极产生气体 | |
| … | …… | |
| t3 | a极产生气体;b极产生气体 |
(1)t1~t3,b极产生的气体有刺激性气味,用湿润的碘化钾淀粉试纸检验,试纸变蓝,气体是
(2)t1时刻,a极析出铜的电极反应式为
(3)从a极刮取白色沉淀(含少量红色固体),经检验含CuCl、Cu。
已知:Cu+
 Cu+Cu2+,CuOH(黄色,不溶)→Cu2O(红色,不溶)
Cu+Cu2+,CuOH(黄色,不溶)→Cu2O(红色,不溶)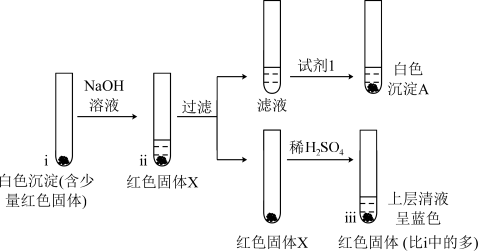
①白色沉淀A为AgCl,试剂1是
②向试管i中加入NaOH溶液,生成的黄色沉淀很快转变为红色。解释该现象的化学方程式为
③证实从a极刮取的白色沉淀中含有CuCl的理由是
(4)针对CuCl沉淀是如何产生的,小组提出两种假设。
假设1:由电极反应产生:Cu2++Cl-+e-=CuCl↓。
假设2:除电极反应外,也可由氧化还原反应产生CuCl,请用离子方程式说明:
(5)t1时a极未产生气体,而t3时a极产生气体。原因是
【应用实践】
(6)镀铜工业中,电镀液以CuSO4、H2SO4为主,同时含Cl-和添加剂。过多的Cl-会使镀层出现白色胶状薄膜。电镀前向电镀液中加入适量Ag2SO4(微溶)固体能有效解决该问题,解释Ag2SO4的作用
您最近一年使用:0次
7 . 香港城市大学支春义团队研发的Zn/富Co(Ⅲ)Co3O4电池(Co3O4的组成近似于Fe3O4)。如图采用ZnSO4和CoSO4,为电解质溶液,充、放电过程中a极发生CoO(s)与Co3O4(s)之间的转化,从而很好地克服了之前碱性锌─钴电池的缺陷。下列说法错误的是
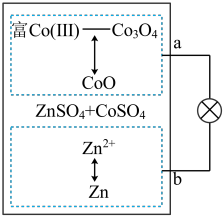

A.放电时,溶液中SO 移向b极 移向b极 |
| B.放电时,溶液中Co2+浓度增大 |
| C.若为碱性介质,会降低电极的可逆性 |
| D.充电时,外电路通过2mole-,理论上电解质溶液质量减少6g |
您最近一年使用:0次
名校
解题方法
8 . 过氧化氢在酸性环境中可氧化Br-,该过程由下列基元反应构成:
①H++H2O2→H3O (快)
(快)
②H3O +Br-→H2O+HOBr (快)活化能 Ea3
+Br-→H2O+HOBr (快)活化能 Ea3
③HOBr+H++Br-→H2O+Br2 (慢)活化能 Ea4
下列说法错误的是
①H++H2O2→H3O
 (快)
(快)②H3O
 +Br-→H2O+HOBr (快)活化能 Ea3
+Br-→H2O+HOBr (快)活化能 Ea3③HOBr+H++Br-→H2O+Br2 (慢)活化能 Ea4
下列说法错误的是
| A.Ea3<Ea4 | B.H+为该反应的催化剂 |
| C.整个反应的速率由反应③决定 | D.总反应为:H2O2+2H++2Br-=2H2O+Br2 |
您最近一年使用:0次
名校
9 . 下述反应可制备特种陶瓷的原料MgO:MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
 MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是
MgO(s)+CO2(g)+SO2(g) △H>0,该反应在某密闭容器中达到平衡时,下列分析正确的是| A.恒温时,增大压强平衡逆向移动,平衡常数减小 |
| B.容积不变时,升高温度,混合气体的平均相对分子质量减小 |
| C.恒温恒容时,分离出部分CO2气体可提高MgSO4的转化率 |
D.恒温恒容时,冲入CO气体,达到新平衡时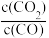 增大 增大 |
您最近一年使用:0次
名校
10 . 合成氨工业对国民经济和社会发展具有重要的意义。
(1) 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
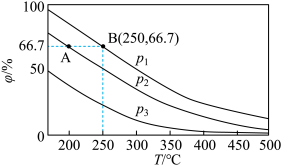
①其中,
___________  (填“>”或“<”),其原因是
(填“>”或“<”),其原因是___________ 。
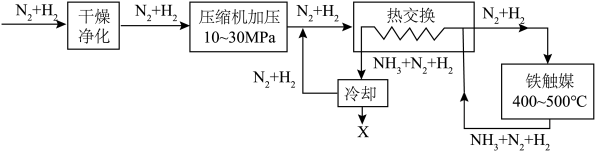
②A、B两点的反应速率: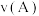
___________ 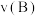 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③若在250℃、 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
___________  (保留一位小数)。
(保留一位小数)。
(2)工业合成氨生产流程示意图如下:
①X为___________ 。
②上述流程中,有利于提高原料利用率的措施是___________ (填标号)。
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:
 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议___________ 。
(1)
 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①其中,

 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是②A、B两点的反应速率:
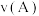
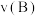 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③若在250℃、
 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
 (保留一位小数)。
(保留一位小数)。(2)工业合成氨生产流程示意图如下:

①X为
②上述流程中,有利于提高原料利用率的措施是
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:

 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议
您最近一年使用:0次







