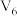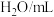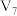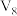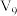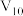解题方法
1 . 已知: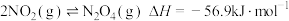 ,反应速率表达式为
,反应速率表达式为
 是反应速率常数,只与温度有关)。下列说法正确的是
是反应速率常数,只与温度有关)。下列说法正确的是
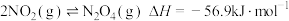 ,反应速率表达式为
,反应速率表达式为
 是反应速率常数,只与温度有关)。下列说法正确的是
是反应速率常数,只与温度有关)。下列说法正确的是| A.达到平衡后,充入NO2,v正增大,v逆减小 |
| B.达到平衡后,加入催化剂,v正和v逆都增大 |
| C.达到平衡后,升高温度,k正增大、k逆减小 |
| D.若恒温恒压条件下充入NO,则平衡不移动 |
您最近一年使用:0次
名校
2 . 某催化剂的M型、N型均可催化反应为2CO(g)+O2(g)⇌2CO2(g)。向容积相同的恒容密闭容器中分别充入等量的CO和O2,在相同时间段内,不同温度下测得CO的转化率(α)如图所示。由图推断下列说法正确的是
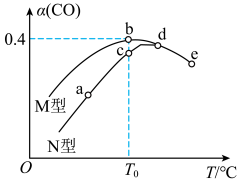

| A.a、b、c、d点均达到平衡状态 |
| B.该反应的平衡常数K(b)大于K(c) |
| C.b点反应物的有效碰撞几率最大 |
| D.图中五个点对应状态下,a点反应速率最慢 |
您最近一年使用:0次
2024-02-14更新
|
118次组卷
|
2卷引用:河南省济源高级中学2022-2023学年高二上学期10月月考 化学试题
名校
3 . 按要求回答下列问题
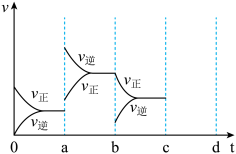
(1)在密闭容器中反应:2SO2+O2⇌2SO3 △H=-QkJmol∙L-1到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如图1所示,a→b过程中改变的条件可能是___________ ;b→c过程中改变的条件可能是___________ ;若增大压强时,将反应速率变化情况画在c~d处(d前已经达到化学平衡)___________ 。
(2)在一个容积固定的密闭容器中进行反应2X(g)+Y(g)⇌2Z(g),已知将2molX和1molY充入该容器,反应在绝热条件下进行达到平衡时,加入催化剂和未加催化剂的速率-时间图(v-t)如图所示,下列说法正确的有___________ (填序号)
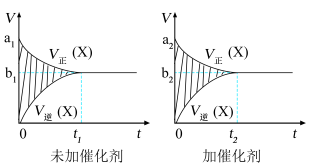
①a1>a2 ②b1>b2 ③t1>t2 ④两图阴影部分面积一样大 ⑤加催化剂的图阴影面积更大
(3)可逆反应CO(g)+H2(g)⇌H2O(g)+C(s),在500K下,向体积为2L的密闭刚性容器中充入1molCO和2molH2进行反应,经10min达到平衡。若初始压强为akPa,平衡时H2的转化率为25%。CO在10min内的平均速率为________ ;500K下,该反应的压强平衡常数为Kp=________ (用含a的式子表示);若平衡后向该容器中加入CO和H2O各0.5mol,平衡_________ (填“向左移动”“向右移动”或“不移动”)。
(1)在密闭容器中反应:2SO2+O2⇌2SO3 △H=-QkJmol∙L-1到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如图1所示,a→b过程中改变的条件可能是

(2)在一个容积固定的密闭容器中进行反应2X(g)+Y(g)⇌2Z(g),已知将2molX和1molY充入该容器,反应在绝热条件下进行达到平衡时,加入催化剂和未加催化剂的速率-时间图(v-t)如图所示,下列说法正确的有

①a1>a2 ②b1>b2 ③t1>t2 ④两图阴影部分面积一样大 ⑤加催化剂的图阴影面积更大
(3)可逆反应CO(g)+H2(g)⇌H2O(g)+C(s),在500K下,向体积为2L的密闭刚性容器中充入1molCO和2molH2进行反应,经10min达到平衡。若初始压强为akPa,平衡时H2的转化率为25%。CO在10min内的平均速率为
您最近一年使用:0次
名校
4 . 回答下列问题
(1)纯水在 时,
时, ,在此温度下,将
,在此温度下,将 的氢氧化钠溶液
的氢氧化钠溶液 与
与 的硫酸溶液
的硫酸溶液 混合(设混合后溶液体积为原两溶液体积之和)所得溶液的
混合(设混合后溶液体积为原两溶液体积之和)所得溶液的 ,则
,则
___________ .
(2)若某溶液中只存在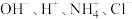 四种离子,且
四种离子,且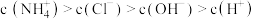 ,该溶液的溶质是
,该溶液的溶质是___________ .
(3)某同学在稀硫酸与锌反应制取氢气的实验中发现加入少量硫酸铜溶液可加快该反应中氢气的生成速率.为了进一步研究所加硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量 粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
请完成此实验设计,其中
___________ ,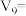
___________ .
(4)常温下,用 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 .若某次捕捉后得到
.若某次捕捉后得到 的溶液,则溶液中
的溶液,则溶液中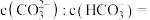
___________ [常温下,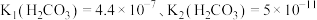 ].
].
(5)常温下,将 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在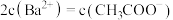 ,则该混合溶液中醋酸的电离常数
,则该混合溶液中醋酸的电离常数
___________ (用含a和b的代数式表示)
(1)纯水在
 时,
时, ,在此温度下,将
,在此温度下,将 的氢氧化钠溶液
的氢氧化钠溶液 与
与 的硫酸溶液
的硫酸溶液 混合(设混合后溶液体积为原两溶液体积之和)所得溶液的
混合(设混合后溶液体积为原两溶液体积之和)所得溶液的 ,则
,则
(2)若某溶液中只存在
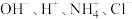 四种离子,且
四种离子,且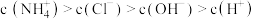 ,该溶液的溶质是
,该溶液的溶质是(3)某同学在稀硫酸与锌反应制取氢气的实验中发现加入少量硫酸铜溶液可加快该反应中氢气的生成速率.为了进一步研究所加硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量
 粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.
粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间.混合溶液组成 | A | B | C | D | E | F |
| 30 |
|
|
|
|
|
饱和 | 0 | 0.5 | 2.5 | 5 |
| 20 |
|
|
|
|
| 10 | 0 |

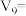
(4)常温下,用
 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 .若某次捕捉后得到
.若某次捕捉后得到 的溶液,则溶液中
的溶液,则溶液中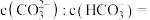
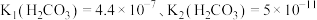 ].
].(5)常温下,将
 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在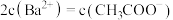 ,则该混合溶液中醋酸的电离常数
,则该混合溶液中醋酸的电离常数
您最近一年使用:0次
名校
5 . 填空。
(1)欲除去FeCl2溶液中的Fe3+,可向溶液中加少量___________ ,请用离子方程式表示除杂原理___________ 。
(2)下列属于氮的固定的是___________ (填序号)。
①工业合成氨
②雷雨天气N2与O2反应
③工业制硝酸的第一步反应:氨的催化氧化
写出上述反应①③的化学方程式:①___________ ,③___________ 。
(3)Fe2O3和铝粉常用于野外焊接钢轨,试写出其化学方程式:___________ 。
(4)检验 的离子方程式:
的离子方程式:___________ 。
(1)欲除去FeCl2溶液中的Fe3+,可向溶液中加少量
(2)下列属于氮的固定的是
①工业合成氨
②雷雨天气N2与O2反应
③工业制硝酸的第一步反应:氨的催化氧化
写出上述反应①③的化学方程式:①
(3)Fe2O3和铝粉常用于野外焊接钢轨,试写出其化学方程式:
(4)检验
 的离子方程式:
的离子方程式:
您最近一年使用:0次
名校
6 . 下列说法不正确的是
| A.附着在试管内壁的硫可用二硫化碳或热的NaOH溶液清洗 |
| B.Fe(OH)2容易被氧化,在空气中发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| C.Fe2O3常用于制造红色油漆和涂料 |
| D.NH3溶于水可以导电,故NH3属于电解质 |
您最近一年使用:0次
名校
解题方法
7 . 列有关焰色试验的叙述正确的是
| A.可以用稀盐酸清洗用过的铂丝或光洁无锈的铁丝 |
| B.焰色试验是元素的化学性质 |
| C.焰色试验时应将玻璃棒洗净后先在外焰上灼烧至与原来的火焰颜色相同,再蘸取待测物实验 |
| D.焰色通过蓝色的钴玻璃没有观察到黄色,则一定不含钠元素 |
您最近一年使用:0次
名校
8 . 下列实验操作中,正确的是
| A.钠要保存在煤油中,实验时剩余的钠要放到废液缸中 |
| B.等物质的量的①Na、②Na2O、③Na2O2、④NaOH投入到等体积且足量的水中,得到四种溶液溶质的质量分数相等 |
| C.取agNa2CO3和NaHCO3的固体混合物充分加热,质量减少bg,可测定出Na2CO3的质量分数 |
| D.Na2CO3是白色粉末,NaHCO3是细小的白色晶体,分别向Na2CO3和NaHCO3的固体中加入少量水,均伴有放热现象 |
您最近一年使用:0次
9 . 回答下列问题:
(1)以下合成材料制品中,属于塑料制品的是_______ ;属于橡胶制品的是_______ ;属于纤维制品的是_______ ;属于复合材料制品的是_______ 。
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子_______ (填“被氧化”或“被还原”),生成阳离子的过程;在海水中为防止钢铁巨轮被腐蚀,常在轮船水面下的船体上焊上_______ (填“锌块”或“铜块”)。
(1)以下合成材料制品中,属于塑料制品的是
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子
您最近一年使用:0次
解题方法
10 . 回答下列问题:
(1)正常雨水的pH为5.6,这是因为大气中二氧化碳溶于雨水的缘故。CO2与水反应生成H2CO3的化学方程式为_______ 。酸雨主要是由人为排放的 _______ 等气体转化为酸造成的。二氧化碳是污染气体吗?_______ (是或不是)。
(2)垃圾处理的常用方法有卫生填埋、焚烧和_______ (填“堆肥”或“排入大海”)。污水处理的主要方法之一是混凝法,_______ (填“食盐或“明矾”)是常用的混凝剂之一。
(3)生活中提倡垃圾分类回收,下列不属于可回收垃圾的是_______ 。
甲:旧报纸 乙:水果皮 丙:废金属
(1)正常雨水的pH为5.6,这是因为大气中二氧化碳溶于雨水的缘故。CO2与水反应生成H2CO3的化学方程式为
(2)垃圾处理的常用方法有卫生填埋、焚烧和
(3)生活中提倡垃圾分类回收,下列不属于可回收垃圾的是
甲:旧报纸 乙:水果皮 丙:废金属
您最近一年使用:0次

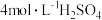 溶液/
溶液/




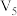
 溶液/
溶液/