1 . 实验室拟用如图装置模拟工业制硝酸的过程。下列说法正确的是


| A.五氧化二磷可用碱石灰代替 |
| B.向反应后盛水的装置中滴入紫色石蕊溶液,溶液变红 |
| C.装置E为安全瓶,其中L1可以为长导管,L2必须为短导管 |
| D.实验时须先通入一段时间空气后,再点燃酒精灯 |
您最近一年使用:0次
名校
解题方法
2 . 已知草酸镍晶体( )难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示:
)难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示: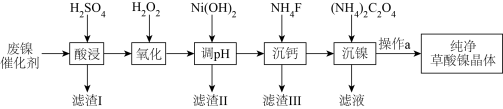
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
②Ksp(CaF2)=1.46 ③当某物质浓度小于1
③当某物质浓度小于1 时,视为完全沉淀
时,视为完全沉淀
回答下列问题:
(1)写出一种能提高“酸浸”速率的措施_______ 。滤渣Ⅰ的成分为 和
和_______ (填化学式)。
(2)“氧化”时反应的离子方程式为_______ 。
(3)“调 ”的范围为
”的范围为_______ ,用化学反应原理的相关知识简要说明滤渣Ⅱ的形成原因_______ 。
(4)“沉钙”过程中,当 沉淀完全时,溶液中
沉淀完全时,溶液中
_______  (列出计算式即可)。
(列出计算式即可)。
(5)“沉镍”时的离子方程式为_______ 。
(6)操作a包含过滤、用乙醇洗涤、110℃下烘干等步骤,其中用乙醇洗涤的目的是洗去杂质和_______ 。
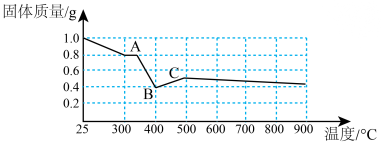
(7)某化学研究小组在文献中查阅到: 受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时, 晶体受热分解的化学方程式为
晶体受热分解的化学方程式为_______ 。
 )难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示:
)难溶于水,常用于制镍粉。工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍的流程如图所示:
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
 ③当某物质浓度小于1
③当某物质浓度小于1 时,视为完全沉淀
时,视为完全沉淀回答下列问题:
(1)写出一种能提高“酸浸”速率的措施
 和
和(2)“氧化”时反应的离子方程式为
(3)“调
 ”的范围为
”的范围为(4)“沉钙”过程中,当
 沉淀完全时,溶液中
沉淀完全时,溶液中
 (列出计算式即可)。
(列出计算式即可)。(5)“沉镍”时的离子方程式为
(6)操作a包含过滤、用乙醇洗涤、110℃下烘干等步骤,其中用乙醇洗涤的目的是洗去杂质和
(7)某化学研究小组在文献中查阅到:
 受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如图所示,写出加热到400℃时, 晶体受热分解的化学方程式为
晶体受热分解的化学方程式为
您最近一年使用:0次
名校
解题方法
3 . 完成下列内容。
(1)已知: 、
、 的燃烧热(
的燃烧热( )分别为
)分别为 和
和 ;
;
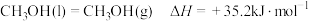 ;
;
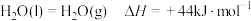 。
。
则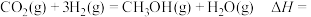
_______  。
。
(2)2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图所示)。其中吸附在Pd表面上的物种用*标注。该历程中最大能垒(活化能)为_______  ,该步骤的化学方程式为
,该步骤的化学方程式为_______ 。

(3)《科学美国人》评出的2016年十大创新技术之一是碳呼吸电池,电池原理如图所示。

多孔碳电极的电极反应式为_______ ,铝极反应为_______ ,随着反应的进行,碳呼吸电池中 浓度
浓度_______ (填“增大”“减小”或“不变”)。
(1)已知:
 、
、 的燃烧热(
的燃烧热( )分别为
)分别为 和
和 ;
;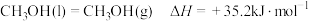 ;
;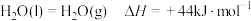 。
。则
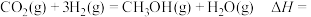
 。
。(2)2010年Sheth等得出乙炔在Pd表面选择加氢的反应机理(如图所示)。其中吸附在Pd表面上的物种用*标注。该历程中最大能垒(活化能)为
 ,该步骤的化学方程式为
,该步骤的化学方程式为
(3)《科学美国人》评出的2016年十大创新技术之一是碳呼吸电池,电池原理如图所示。

多孔碳电极的电极反应式为
 浓度
浓度
您最近一年使用:0次
名校
4 . 镧系金属铈(Ce)主要有+3、+4两种价态,地壳中常以氟碳铈矿( )存在。工业上利用氟碳铈矿提取
)存在。工业上利用氟碳铈矿提取 的一种工艺流程如图所示。下列有关说法错误的是
的一种工艺流程如图所示。下列有关说法错误的是

 )存在。工业上利用氟碳铈矿提取
)存在。工业上利用氟碳铈矿提取 的一种工艺流程如图所示。下列有关说法错误的是
的一种工艺流程如图所示。下列有关说法错误的是
A.加热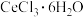 制备无水 制备无水 时,HCl的作用是抑制 时,HCl的作用是抑制 的水解 的水解 |
| B.在空气中焙烧氟碳铈矿时,发生的主要反应的氧化剂和还原剂的物质的量之比为1∶4 |
C.参与酸浸反应的 和 和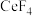 的物质的量之比为1∶3时,则需要 的物质的量之比为1∶3时,则需要 和HCl的物质的量之比也为1∶3 和HCl的物质的量之比也为1∶3 |
D.向 中加入KCl溶液的目的是将 中加入KCl溶液的目的是将 转化为 转化为 ,提高产率 ,提高产率 |
您最近一年使用:0次
名校
解题方法
5 . Ⅰ.甲醇是人们开发和利用的一种新能源已知:
①2H2(g)+O2(g)=2H2O(l) △H=-571.8 kJ/mol;
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。
(1)甲醇蒸气完全燃烧的热化学方程式为___________ 。
(2)反应②的能量变化如图所示,则△H2=___________ (用E1、E2的代数式表示)。
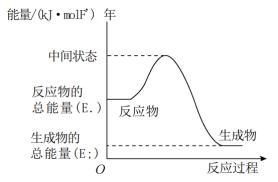
(3)请你分析H2(g)作为能源与甲醇蒸气作为能源相比的优点:___________ (写出两点即可)。
Ⅱ.碳的单质及其化合物是人类生产生活的主要能源物质。回答下列问题:
(4)有机物M经过太阳光照射可转化成N,转化过程如下:
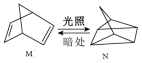 △H=+88.6 kJ/mol。则M、N相比,较稳定的是
△H=+88.6 kJ/mol。则M、N相比,较稳定的是___________ 。
(5)已知CH3OH(l)的燃烧热为-726.5 kJ/mol,CH3OH(l)+ O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a___________ (填“>”“<”或“=”)726.5。
(6)使Cl2和H2O(g)通过均热的碳层,生成HCl气体和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:___________ 。
①2H2(g)+O2(g)=2H2O(l) △H=-571.8 kJ/mol;
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ/mol。(1)甲醇蒸气完全燃烧的热化学方程式为
(2)反应②的能量变化如图所示,则△H2=

(3)请你分析H2(g)作为能源与甲醇蒸气作为能源相比的优点:
Ⅱ.碳的单质及其化合物是人类生产生活的主要能源物质。回答下列问题:
(4)有机物M经过太阳光照射可转化成N,转化过程如下:
 △H=+88.6 kJ/mol。则M、N相比,较稳定的是
△H=+88.6 kJ/mol。则M、N相比,较稳定的是(5)已知CH3OH(l)的燃烧热为-726.5 kJ/mol,CH3OH(l)+
 O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2(g) △H=-a kJ/mol,则a(6)使Cl2和H2O(g)通过均热的碳层,生成HCl气体和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
您最近一年使用:0次
名校
解题方法
6 . 硒(Se)与硫属于同一主族元素,含硒的几种物质存在如图所示的转化关系。下列说法错误的是


| A.图中只有反应④和⑤不属于氧化还原反应 |
B.反应②中可能有 生成 生成 |
C. 属于二元酸, 属于二元酸, 属于正盐 属于正盐 |
| D.反应⑥中氧化产物与还原产物的物质的量之比为8:1 |
您最近一年使用:0次
名校
7 . 化学在生产、生活中起着重要的作用,以下化学用语中正确的是
A.补铁剂通常需要与维C共同使用,是为了增强药品中 的效果 的效果 |
| B.侯氏制碱法中利用各个物质溶解度的不同,可直接过滤获得纯碱 |
| C.向冷的石灰乳中通入氯气,可制得漂白粉,有效成分为次氯酸钙 |
| D.不锈钢是最常见的一种合金钢,它的合金元素主要是锰和镍 |
您最近一年使用:0次
2022-10-13更新
|
525次组卷
|
4卷引用:甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题
名校
8 . 亚硝酸钙是白色粉末,易潮解,易溶于水,微溶于乙醇、乙醚。实验室用NO和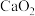 (淡黄色固体)制备无水亚硝酸钙的装置(夹持装置略)如图所示。
(淡黄色固体)制备无水亚硝酸钙的装置(夹持装置略)如图所示。

回答下列问题:
(1)实验开始先通 ,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a的名称为
,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a的名称为_______ ,B中盛放的试剂是_______ 。
(2)装置E中,酸性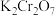 可将剩余的NO氧化为
可将剩余的NO氧化为 ,溶液逐渐由橙色变为绿色
,溶液逐渐由橙色变为绿色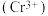 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(3)上述装置存在一处缺陷,会导致亚硝酸钙产率降低,改进的方法是_______ 。
(4)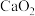 完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②……;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……
完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②……;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……
操作②是_______ 。
(5)测定所得亚硝酸钙中硝酸钙的含量。
实验原理: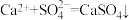 ;
;
 ;
;
 ;
;
 。
。
实验步骤:I.准确称取m g所得亚硝酸钙,置于150mL烧杯中,加入100mL蒸馏水和n g硫酸钠(足量),搅拌均匀,将溶液与沉淀全部移入250mL容量瓶,加入稀释至刻度,摇匀,干过滤;(忽略固体对溶液体积的影响)
II.取25.00mL滤液于500mL锥形瓶中,加入足量 饱和溶液,煮沸5min;
饱和溶液,煮沸5min;
III.冷却后用少量蒸馏水洗涤锥形瓶内壁,再加入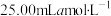 硫酸亚铁铵
硫酸亚铁铵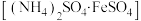 溶液,在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1∶1)。
溶液,在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1∶1)。
IV.加4滴指示剂,迅速用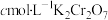 标准液滴定至终点,消耗
标准液滴定至终点,消耗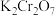 标准液V mL。
标准液V mL。
所得亚硝酸钙中硝酸钙的质量百分含量为_______ ;下列情况会导致硝酸钙的质量百分含量测量值偏大的是_______ (填标号)。
a.步骤I中,称量后样品发生了潮解
b.步骤II中,煮沸时间仅有3min
c.步骤III中量取的硫酸亚铁铵溶液的实际体积小于25.00mL
d.滴定终点时,发现尖嘴管内有气泡生成
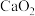 (淡黄色固体)制备无水亚硝酸钙的装置(夹持装置略)如图所示。
(淡黄色固体)制备无水亚硝酸钙的装置(夹持装置略)如图所示。
回答下列问题:
(1)实验开始先通
 ,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a的名称为
,一段时间后,向三颈烧瓶中滴加稀硝酸制取NO,B中产生大量气泡时,D处开始加热。仪器a的名称为(2)装置E中,酸性
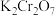 可将剩余的NO氧化为
可将剩余的NO氧化为 ,溶液逐渐由橙色变为绿色
,溶液逐渐由橙色变为绿色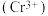 ,该反应的离子方程式为
,该反应的离子方程式为(3)上述装置存在一处缺陷,会导致亚硝酸钙产率降低,改进的方法是
(4)
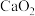 完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②……;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……
完全还原后,进行的操作是:①停止滴加稀硝酸,停止通电;②……;③冷却后,将所得产品完全转移到试剂瓶中密封保存;④……操作②是
(5)测定所得亚硝酸钙中硝酸钙的含量。
实验原理:
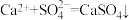 ;
; ;
; ;
; 。
。实验步骤:I.准确称取m g所得亚硝酸钙,置于150mL烧杯中,加入100mL蒸馏水和n g硫酸钠(足量),搅拌均匀,将溶液与沉淀全部移入250mL容量瓶,加入稀释至刻度,摇匀,干过滤;(忽略固体对溶液体积的影响)
II.取25.00mL滤液于500mL锥形瓶中,加入足量
 饱和溶液,煮沸5min;
饱和溶液,煮沸5min;III.冷却后用少量蒸馏水洗涤锥形瓶内壁,再加入
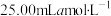 硫酸亚铁铵
硫酸亚铁铵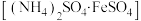 溶液,在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1∶1)。
溶液,在不断摇动下,沿瓶壁缓慢加入20mL硫酸(1∶1)。IV.加4滴指示剂,迅速用
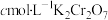 标准液滴定至终点,消耗
标准液滴定至终点,消耗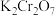 标准液V mL。
标准液V mL。所得亚硝酸钙中硝酸钙的质量百分含量为
a.步骤I中,称量后样品发生了潮解
b.步骤II中,煮沸时间仅有3min
c.步骤III中量取的硫酸亚铁铵溶液的实际体积小于25.00mL
d.滴定终点时,发现尖嘴管内有气泡生成
您最近一年使用:0次
2022-10-13更新
|
477次组卷
|
3卷引用:甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题
甘肃省兰州市西北师范大学附属中学2022-2023学年高三上学期期中考试化学试题河北衡水市部分中学2022-2023学年高三上学期10月考试化学试题(已下线)2022年河北省高考真题变式题(14-18)
9 . 2021年6月17日,神舟十二号载人飞行发射任务取得圆满成功,神舟十二号载人飞船首次实施绕飞空间站并与空间站径向交会。下列说法错误的是
| A.航天服材料中的玻璃纤维属于有机高分子材料 |
| B.返回器舱外表面使用的高温结构陶瓷是新型无机非金属材料 |
| C.中国空间站推进器的推进剂氙气属于稀有气体 |
| D.空间站太阳能电池板的主要材料是晶体硅 |
您最近一年使用:0次
10 . 2022年6月17日,中国第三艘航空母舰——“福建舰”正式下水,它是目前世界上最大的常规动力航母,配置了先进的电磁弹射和阻拦装置。下列说法错误的是
| A.电磁弹射技术可使舰载机快速起飞,电能属于二级能源 |
| B.氮化镓常用于雷达系统,其属于新型无机非金属材料 |
| C.低磁合金钢常用于舰体材料,其强度、熔点均高于纯铁 |
| D.航母燃料是重油,重油通过燃烧将化学能转变为热能、机械能等 |
您最近一年使用:0次
2022-09-29更新
|
1187次组卷
|
7卷引用:甘肃省武威第六中学 2022~2023学年高三上学期第二次阶段性考试化学试题



