2022高二上·安徽阜阳·竞赛
1 . 你知道什么是酸碱吗?
中学我们认识知道,酸是在水溶液中电离出的阳离子全部为氢离子的物质,碱是在水溶液中电离出的阴离子全部为氢氧根离子的物质。而事实上,酸碱的定义随着历史发展也在不断革新,历代化学家发表了不同的酸碱理论,目前较为广泛接受的有离子论,溶剂论,质子论,电子论和软硬酸碱理论,在此处针对溶剂论和质子论做简单介绍。
溶剂论是1905年富兰克林提出的一种按照纯溶剂是否能够自耦电离(例如水的自耦电离:2H2O H3O++OH-)出溶剂合质子来区分酸碱的一种理论,这个理论将溶液自耦电离出的具有溶液特征的阳离子称为酸,具有溶液特征的阴离子称为碱。例如:液态N2O4中发生自耦电离N2O4
H3O++OH-)出溶剂合质子来区分酸碱的一种理论,这个理论将溶液自耦电离出的具有溶液特征的阳离子称为酸,具有溶液特征的阴离子称为碱。例如:液态N2O4中发生自耦电离N2O4 NO++NO
NO++NO ,此时NO+即为该溶液的酸,NO
,此时NO+即为该溶液的酸,NO 即为该溶液的碱。
即为该溶液的碱。
据此回答第( 1 )题。
(1)①已知液氨会自耦电离,请类比水的自耦电离写出其自耦电离方程式:_______ ,其中,_______ 为液氨溶液的酸,_______ 为液氨溶液的碱。此时的酸碱中和反应可以写成(写出方程式):_______ 。
②写出氯气在液氨溶液中反应的离子方程式:_______ 。
质子论是1923年由布朗斯特和劳里提出的,其定义酸为可以给出质子的物种,碱定义为可以接受质子的物种,因此存在关系: ,如图的关系也称为“共轭酸碱对”,因此该理论又称为“共轭酸碱理论”。该理论下所有酸碱都是共轭的,满足弱酸共轭强碱,弱碱共轭强酸。其中的酸,碱可以是分子,也可以是阴离子,阳离子。同时,“盐”的定义被去除,因为组成盐的离子本身就可以分别看作酸和碱。
,如图的关系也称为“共轭酸碱对”,因此该理论又称为“共轭酸碱理论”。该理论下所有酸碱都是共轭的,满足弱酸共轭强碱,弱碱共轭强酸。其中的酸,碱可以是分子,也可以是阴离子,阳离子。同时,“盐”的定义被去除,因为组成盐的离子本身就可以分别看作酸和碱。
(2)①下列说法正确的是_______ 。
A.因为在水溶液中有 H2SO4 2H++SO
2H++SO ,因此 H2SO4 与 SO
,因此 H2SO4 与 SO 互为共轭酸碱对
互为共轭酸碱对
B.由于水可以发生自耦电离,则按照该理论,水既属于酸又属于碱
C.可以根据HNO3的性质推断NO 的酸性较弱
的酸性较弱
D.液氨对碳酸和盐酸是区分溶剂,可以便于区分酸性的强弱
②对于反应NH3+HCl=NH4Cl而言,_______ 是酸_______ 是碱。
③在溶液中,酸的强度是依靠其电离平衡常数 来判断的。
来判断的。  越大则证明电离程度越大,故酸性越强。
越大则证明电离程度越大,故酸性越强。
对于一种酸HA,其电离平衡常数为:HA H++A-,其中
H++A-,其中 ,与化学平衡常数类似,为离子浓度的化学计量数次幂的乘积比电解质的化学计量数次幂的乘积。
,与化学平衡常数类似,为离子浓度的化学计量数次幂的乘积比电解质的化学计量数次幂的乘积。
实验证明,盐酸,硝酸,硫酸,高氯酸的酸性是有差异的,可是在水溶液中无法区分酸性差异,其原因在于水溶液本身具有碱性,其溶剂化作用(质子在溶液中不是单独存在,而是结合溶剂分子生成溶剂合质子,这称为溶剂化作用)导致这四种酸在水溶液中的电离平衡趋势相同,从而无法断定酸性强弱,这类溶剂称为拉平溶剂。反之,若将这四种酸分别放入冰醋酸中,测得的平衡常数是不同的,即电离平衡趋势不同,这类溶剂称之为区分溶剂。据此回答问题:区分溶剂之所以能够区分不同强酸的酸碱性,原因在于其溶剂化作用_______ (填“较强”或“较弱”)。
中学我们认识知道,酸是在水溶液中电离出的阳离子全部为氢离子的物质,碱是在水溶液中电离出的阴离子全部为氢氧根离子的物质。而事实上,酸碱的定义随着历史发展也在不断革新,历代化学家发表了不同的酸碱理论,目前较为广泛接受的有离子论,溶剂论,质子论,电子论和软硬酸碱理论,在此处针对溶剂论和质子论做简单介绍。
溶剂论是1905年富兰克林提出的一种按照纯溶剂是否能够自耦电离(例如水的自耦电离:2H2O
 H3O++OH-)出溶剂合质子来区分酸碱的一种理论,这个理论将溶液自耦电离出的具有溶液特征的阳离子称为酸,具有溶液特征的阴离子称为碱。例如:液态N2O4中发生自耦电离N2O4
H3O++OH-)出溶剂合质子来区分酸碱的一种理论,这个理论将溶液自耦电离出的具有溶液特征的阳离子称为酸,具有溶液特征的阴离子称为碱。例如:液态N2O4中发生自耦电离N2O4 NO++NO
NO++NO ,此时NO+即为该溶液的酸,NO
,此时NO+即为该溶液的酸,NO 即为该溶液的碱。
即为该溶液的碱。据此回答第( 1 )题。
(1)①已知液氨会自耦电离,请类比水的自耦电离写出其自耦电离方程式:
②写出氯气在液氨溶液中反应的离子方程式:
质子论是1923年由布朗斯特和劳里提出的,其定义酸为可以给出质子的物种,碱定义为可以接受质子的物种,因此存在关系:
 ,如图的关系也称为“共轭酸碱对”,因此该理论又称为“共轭酸碱理论”。该理论下所有酸碱都是共轭的,满足弱酸共轭强碱,弱碱共轭强酸。其中的酸,碱可以是分子,也可以是阴离子,阳离子。同时,“盐”的定义被去除,因为组成盐的离子本身就可以分别看作酸和碱。
,如图的关系也称为“共轭酸碱对”,因此该理论又称为“共轭酸碱理论”。该理论下所有酸碱都是共轭的,满足弱酸共轭强碱,弱碱共轭强酸。其中的酸,碱可以是分子,也可以是阴离子,阳离子。同时,“盐”的定义被去除,因为组成盐的离子本身就可以分别看作酸和碱。(2)①下列说法正确的是
A.因为在水溶液中有 H2SO4
 2H++SO
2H++SO ,因此 H2SO4 与 SO
,因此 H2SO4 与 SO 互为共轭酸碱对
互为共轭酸碱对B.由于水可以发生自耦电离,则按照该理论,水既属于酸又属于碱
C.可以根据HNO3的性质推断NO
 的酸性较弱
的酸性较弱D.液氨对碳酸和盐酸是区分溶剂,可以便于区分酸性的强弱
②对于反应NH3+HCl=NH4Cl而言,
③在溶液中,酸的强度是依靠其电离平衡常数
 来判断的。
来判断的。  越大则证明电离程度越大,故酸性越强。
越大则证明电离程度越大,故酸性越强。对于一种酸HA,其电离平衡常数为:HA
 H++A-,其中
H++A-,其中 ,与化学平衡常数类似,为离子浓度的化学计量数次幂的乘积比电解质的化学计量数次幂的乘积。
,与化学平衡常数类似,为离子浓度的化学计量数次幂的乘积比电解质的化学计量数次幂的乘积。实验证明,盐酸,硝酸,硫酸,高氯酸的酸性是有差异的,可是在水溶液中无法区分酸性差异,其原因在于水溶液本身具有碱性,其溶剂化作用(质子在溶液中不是单独存在,而是结合溶剂分子生成溶剂合质子,这称为溶剂化作用)导致这四种酸在水溶液中的电离平衡趋势相同,从而无法断定酸性强弱,这类溶剂称为拉平溶剂。反之,若将这四种酸分别放入冰醋酸中,测得的平衡常数是不同的,即电离平衡趋势不同,这类溶剂称之为区分溶剂。据此回答问题:区分溶剂之所以能够区分不同强酸的酸碱性,原因在于其溶剂化作用
您最近一年使用:0次
2 . 风绪小组探究 的相关性质。
的相关性质。
(1)对于 和水反应放出氧气的现象,他们推测,可能和
和水反应放出氧气的现象,他们推测,可能和 有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是
有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是 在水中反应生成了
在水中反应生成了 ,后
,后 分解。通过查阅资料得知:
分解。通过查阅资料得知: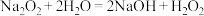 ,
,
①借助资料和实验,发现可以通过 溶于冷水制备少量的
溶于冷水制备少量的 。使用冷水的原因是
。使用冷水的原因是_______ 。
②为验证资料的真实性,他们向溶液中滴加适量的酸性 溶液,发现产生气泡,产生气泡的原因是(用方程式表示)
溶液,发现产生气泡,产生气泡的原因是(用方程式表示)_______ 。
(2)在有同学做实验时,还观察到了棕褐色沉淀,他们推测是 。猜测可能是
。猜测可能是 与
与 发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。
发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。
①先向沉淀中加入浓盐酸并加热,观察到有_______ 气体产生,发生反应_______ 。证明了猜想正确。
②后续得知,同学在制酸性 溶液时,加入的硫酸的量不一样。推测可能是
溶液时,加入的硫酸的量不一样。推测可能是 浓度不同造成的。于是,他们改用有
浓度不同造成的。于是,他们改用有 的
的 溶液滴入
溶液滴入 溶液中,仅观察到了
溶液中,仅观察到了_______ 沉淀,并证明是 ,反应方程式是
,反应方程式是_______ 。
(3) 在反应时,表现氧化性还是还原性,和
在反应时,表现氧化性还是还原性,和_______ 有关。
 的相关性质。
的相关性质。(1)对于
 和水反应放出氧气的现象,他们推测,可能和
和水反应放出氧气的现象,他们推测,可能和 有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是
有关。通过实验发现,用冷水时,该反应放出气体的速率相对慢,而换用热水相对快。从而推测可能是 在水中反应生成了
在水中反应生成了 ,后
,后 分解。通过查阅资料得知:
分解。通过查阅资料得知: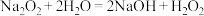 ,
,
①借助资料和实验,发现可以通过
 溶于冷水制备少量的
溶于冷水制备少量的 。使用冷水的原因是
。使用冷水的原因是②为验证资料的真实性,他们向溶液中滴加适量的酸性
 溶液,发现产生气泡,产生气泡的原因是(用方程式表示)
溶液,发现产生气泡,产生气泡的原因是(用方程式表示)(2)在有同学做实验时,还观察到了棕褐色沉淀,他们推测是
 。猜测可能是
。猜测可能是 与
与 发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。
发生了反应。为验证猜想以及探究实验现象不一样的原因,他们做了如下实验。①先向沉淀中加入浓盐酸并加热,观察到有
②后续得知,同学在制酸性
 溶液时,加入的硫酸的量不一样。推测可能是
溶液时,加入的硫酸的量不一样。推测可能是 浓度不同造成的。于是,他们改用有
浓度不同造成的。于是,他们改用有 的
的 溶液滴入
溶液滴入 溶液中,仅观察到了
溶液中,仅观察到了 ,反应方程式是
,反应方程式是(3)
 在反应时,表现氧化性还是还原性,和
在反应时,表现氧化性还是还原性,和
您最近一年使用:0次
解题方法
3 . 下列说法正确的是
| A.向丙烯醛溶液中滴加高锰酸钾溶液,发现紫红色褪去,可说明丙烯醛中含碳碳双键。 |
| B.向盛有氧化银固体的两支试管中分别滴加稀硝酸和氨水,发现氧化银溶解,说明氧化银是两性氧化物 |
C.将浓 溶液和少量溴苯混合后振荡,仍然有无色油状液体,说明常温下溴苯不易水解 溶液和少量溴苯混合后振荡,仍然有无色油状液体,说明常温下溴苯不易水解 |
| D.将酸性高锰酸钾溶液分别加入到苯和甲苯溶液中并振荡,可证明甲苯中的甲基可以活化苯环 |
您最近一年使用:0次
解题方法
4 . 氢溴酸是无色、易挥发的液体,在化工领域用途广泛。实验室模拟一种工业制备氢溴酸的主要流程如下:
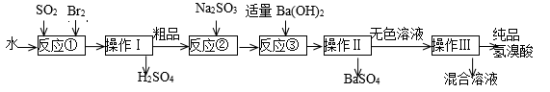
完成下列填空:
(1)写出反应①的离子方程式___________ 。该反应需要在冰水浴中进行,可能的原因是___________ 。
(2)操作I用到的玻璃仪器有蒸馏烧瓶、温度计、___________ 、接液管和锥形瓶。
(3)反应②中Na2SO3的目的是___________ 。
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由___________ 。
(5)工业氢溴酸往往呈淡黄色:①可能是因为像工业盐酸一样含Fe3+,②还可能是因为含___________ ,如何证明?___________ 。

完成下列填空:
(1)写出反应①的离子方程式
(2)操作I用到的玻璃仪器有蒸馏烧瓶、温度计、
(3)反应②中Na2SO3的目的是
(4)反应③中的Ba(OH)2溶液能否用BaCl2或者Ba(NO3)2溶液代替?说明理由
(5)工业氢溴酸往往呈淡黄色:①可能是因为像工业盐酸一样含Fe3+,②还可能是因为含
您最近一年使用:0次
名校
解题方法
5 . 亚硝酸钠(NaNO2)的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
已知:①NaNO2有强氧化性又有还原性;
②NO能被酸性KMnO4氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为NO2、NO和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的NaNO2。
反应原理为:2NO+Na2O2=2NaNO2

回答下列问题:
(1)乙装置的仪器名称是____ ,装置乙的作用是____ 。
(2)甲中滴入稀硝酸前需先通入N2,原因是____ 。
(3)甲装置中发生反应的离子方程式为____ 。
(4)反应过程中观察到丙中的现象为___ 。
(5)丁中酸性KMnO4的作用是____ 。
(6)设计实验证明丙装置有NaNO2生成____ (写出操作、试剂和现象)。
已知:①NaNO2有强氧化性又有还原性;
②NO能被酸性KMnO4氧化成硝酸根离子;
③亚硝酸是弱酸,很不稳定,易分解为NO2、NO和水。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的NaNO2。
反应原理为:2NO+Na2O2=2NaNO2

回答下列问题:
(1)乙装置的仪器名称是
(2)甲中滴入稀硝酸前需先通入N2,原因是
(3)甲装置中发生反应的离子方程式为
(4)反应过程中观察到丙中的现象为
(5)丁中酸性KMnO4的作用是
(6)设计实验证明丙装置有NaNO2生成
您最近一年使用:0次
2022-07-12更新
|
336次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
名校
解题方法
6 . 铜是生活中常见的金属,以铜为原料进行如下实验。回答下列问题:
Ⅰ.制备
(1)利用铜与浓硫酸制备 ,适宜的装置是
,适宜的装置是_______ (从A、B、C中选择),该装置内发生的化学方程式为_______ 。
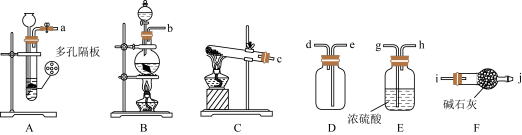
(2)收集干燥的 ,所需装置的接口连接顺序为:发生装置→
,所需装置的接口连接顺序为:发生装置→_______ (填小写字母)。
(3)反应后,发生装置中未观察到蓝色溶液,原因是_______ 。
Ⅱ.探究温度对铜与过氧化氢反应的影响
向10mL30%的 溶液中滴加1mL3mol/L硫酸,将光洁无锈的铜丝置于其中,铜丝表面产生气泡并逐渐变多,剩余溶液呈蓝色。经检验产生的气体为
溶液中滴加1mL3mol/L硫酸,将光洁无锈的铜丝置于其中,铜丝表面产生气泡并逐渐变多,剩余溶液呈蓝色。经检验产生的气体为 ,查阅资料发现是
,查阅资料发现是 催化
催化 分解的结果。
分解的结果。
(4)写出生成 的离子方程式
的离子方程式_______ 。
(5)学习小组提出猜想:升高温度, 催化能力增强,该小组设计如下实验验证猜想。
催化能力增强,该小组设计如下实验验证猜想。
①小组同学认为实验1~3的结果,不能证明猜想成立,理由是_______ 。
②为进一步验证猜想,完善实验4~6的方案(答案填在答题卡上)_______ 。小组同学结合实验1~6,判断猜想成立,依据是_______ 。
Ⅰ.制备

(1)利用铜与浓硫酸制备
 ,适宜的装置是
,适宜的装置是
(2)收集干燥的
 ,所需装置的接口连接顺序为:发生装置→
,所需装置的接口连接顺序为:发生装置→(3)反应后,发生装置中未观察到蓝色溶液,原因是
Ⅱ.探究温度对铜与过氧化氢反应的影响
向10mL30%的
 溶液中滴加1mL3mol/L硫酸,将光洁无锈的铜丝置于其中,铜丝表面产生气泡并逐渐变多,剩余溶液呈蓝色。经检验产生的气体为
溶液中滴加1mL3mol/L硫酸,将光洁无锈的铜丝置于其中,铜丝表面产生气泡并逐渐变多,剩余溶液呈蓝色。经检验产生的气体为 ,查阅资料发现是
,查阅资料发现是 催化
催化 分解的结果。
分解的结果。(4)写出生成
 的离子方程式
的离子方程式(5)学习小组提出猜想:升高温度,
 催化能力增强,该小组设计如下实验验证猜想。
催化能力增强,该小组设计如下实验验证猜想。| 实验序号 | 30%H2O2(mL) | 1mol/LCuSO4(mL) | 水(mL) | 水浴温度(℃) | 3min时生成O2的平均速率(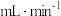 ) ) |
| 1 | 10 | 1 | 1 | 20 | 2.4 |
| 2 | 10 | 1 | 1 | 30 | 9 |
| 3 | 10 | 1 | 1 | 40 | 90 |
| 4 | 10 | 0 | 2 | 20 | A1 |
| 5 | A2 | ||||
| 6 | 10 | 0 | 2 | 40 | A3 |
②为进一步验证猜想,完善实验4~6的方案(答案填在答题卡上)
您最近一年使用:0次
2022-04-15更新
|
1537次组卷
|
9卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题广东省佛山市普通高中2022届高三教学质量检测(二)化学试题广东省佛山市2022届高三下学期4月第二次教学质量监测(二模)化学试题(已下线)押全国卷理综第26题 实验综合-备战2022年高考化学临考题号押题(全国卷)(已下线)押广东卷化学第17题 化学实验综合题-备战2022年高考化学临考题号押题(广东卷)(已下线)微专题24 氯气、氨气、二氧化硫的实验室制备与应用-备战2023年高考化学一轮复习考点微专题甘肃省兰州市外国语高级中学2022-2023学年高三上学期第二次考试化学试题湖南省湘潭市第一中学2023届高三上学期第五次月考化学试题广东省广州市玉岩中学2024届高三上学期10月月考化学试题
解题方法
7 . 在恒容密闭容器中发生反应:3CO(g)+Fe2O3(s) 3CO2(g)+2Fe(s),下列说法不正确的是
3CO2(g)+2Fe(s),下列说法不正确的是
 3CO2(g)+2Fe(s),下列说法不正确的是
3CO2(g)+2Fe(s),下列说法不正确的是| A.增加块状Fe2O3的量,反应速率增大 |
| B.降低温度,反应速率减慢 |
| C.使用催化剂,反应速率增大 |
| D.充入CO,反应速率增大 |
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
8 . 随着当今社会的发展,科技正在不断改变我们的生活方式,而我们所使用的支付方式也开始向着数字化的方向转变,支付宝正是其中的一个例子。而随着第19届亚运会的接近,支付宝的“蚂蚁森林”中也出现了“亚运碳中和”的选项,为国家的“双碳”目标做出自己的贡献。下列有关“碳中和”“碳达峰”的说法正确的是
| A.碳中和一般是指国家、企业、产品、活动或个人在一定时间内直接或间接产生的二氧化碳或温室气体排放总量,通过植树造林、节能减排等形式,达到绝对的“零排放”。 |
| B.“双碳”中的碳指的就是石油、煤炭、木材等由碳元素构成的自然资源,“碳”的耗用导致全球变暖的元凶“二氧化碳” 制造得多,所以我们认为“二氧化碳”也是大气污染物。 |
| C.2018年10月,支付宝蚂蚁森林种树模式被正式纳入国家义务植树体系。截至20年9月,已经有超5.5亿用户参与蚂蚁森林,种植了超过两亿棵树,这有利于实现“碳中和”。 |
| D.“低碳”“碳足迹”等词汇近年来成为国内外的热门用语。这里的“碳”的指向和“碳中和”“碳达峰”中的“碳”指向相同,都是指石油、煤炭、木材等由碳元素构成的自然资源。 |
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
9 . 瑞典Linkoping(林雪平)大学研究出一款超级电池Power Paper,又称“纸电池”,该电池打破四项世界纪录,因拥有极其轻薄的厚度,并具有极佳的延展性和稳固性,反复经过多次折叠依然能保持良好状态。电池虽小,但其容量为26800毫安,约为iPhone电池容量的十倍,以保障手机具有持久的续航。而根据微软公布的消息,这是一种包含了柔性正电极和柔性负电极的电化学能量存储单元。正负电极都会在柔性的金属丝网上部署镓基液态金属。电化学能量存储单元还包括膜,该膜具有与柔性正电极接触的表面和与柔性负电极接触的相对表面,其结构简图如下图所示:

下列说法不正确的是:

下列说法不正确的是:
| A.由元素周期表可知,氢氧化镓能和苛性钠、苛性钾溶液反应;而纸电池具有柔韧性更好、容量更高、厚度更薄、延展性更好、稳固性更高等一系列的优点。 |
| B.若正极为铜片,负极分别是锌片和另一种银白色金属片,以NaCl溶液为电解液时,发现电流表指针的偏转方向相反,则另一种银白色金属片可能是银片。 |
C.此纸电池负极材料可以是铝片,正极材料可以是石墨片,若此原电池的电解液为NaOH溶液,其电极反应的负极反应式为:Al-e-+2OH-= AlO +H2O。 +H2O。 |
| D.原电池有携带方便、不需维护、可长期(几个月甚至几年)储存或使用等优点,但非氧化还原反应也可以设计成原电池,由此可得出原电池不等于化学电池。 |
您最近一年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
10 . 在学习化学时,我们要对概念有深刻的理解,下列说法中完全正确的是
| A.凡是只有共价键的物质都是共价化合物,但含有共价键的物质可能是离子化合物。 |
| B.凡是属于糖类的都是碳水化合物,但被称为碳水化合物的物质可能并不属于糖类。 |
| C.不同物质的俗名不同,如CaO有生石灰、消石灰,而Ca(OH)2有熟石灰和石灰水。 |
| D.苏打的化学式为Na2CO3,小苏打的是NaHCO3,大苏打可以用于银版照片定影液。 |
您最近一年使用:0次



