名校
解题方法
1 . 如图:某同学用高锰酸钾和浓盐酸制备氯气,验证氯气性质实验装置。相关说法错误的是


| A.脱脂棉中的无水氯化钙可以用碱石灰代替 |
| B.该实验装置可证明干燥的氯气没有漂白作用 |
| C.湿润石蕊试纸先变红,说明生成了酸性物质 |
| D.淀粉碘化钾试纸先变蓝后褪色,说明氯气将I2氧化 |
您最近一年使用:0次
解题方法
2 . 以下为有机物的制备实验装置。下列相关说法错误的是

| A.图1右侧试管中观察到淡黄色沉淀,证明制备溴苯的反应为取代反应 |
| B.图2所制得的硝基苯因溶解有NO2略带黄色,可加入NaOH溶液分液除去 |
| C.图3导气管口应在右侧试管中Na2CO3溶液液面上方,以防止倒吸 |
| D.图4分水器分出生成的水可提高反应转化率 |
您最近一年使用:0次
名校
3 . 1810年,英国化学家戴维以大量事实为依据,确认一种新元素组成的单质氯气。某化学兴趣小组同学利用以下装置制备干燥的氯气并对氯气的性质进行探究。

(1)仪器b的名称为_________ 。某同学认为该实验装置存在一处明显的不足,其改进措施为_________ 。
(2)仪器a中发生反应的化学方程式为_________ 。根据氯气的性质D中的收集装置可以选择_________ (填序号)。

(3)下列有关该实验的说法中不正确的是_________ (填字母)。
A.将b中液体换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
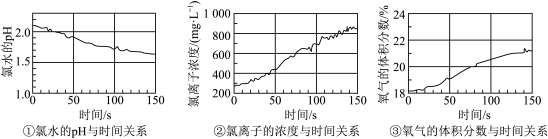
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:_________ 。

(1)仪器b的名称为
(2)仪器a中发生反应的化学方程式为

(3)下列有关该实验的说法中不正确的是
A.将b中液体换为稀盐酸,同样可以产生氯气
B.C中试剂是浓硫酸,目的是干燥氯气
C.E中红色布条不褪色,F中红色布条褪色证明氯气具有漂白性
(4)利用数字化实验探究次氯酸的化学性质,用强光照射盛有氯水的密闭广口瓶;并用传感器测定广口瓶中数据,得到如下图曲线。请用化学方程式解释曲线中氯离子的浓度和氧气体积分数变化的原因:

您最近一年使用:0次
真题
名校
4 . 关于反应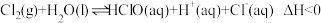 ,达到平衡后,下列说法
,达到平衡后,下列说法不正确 的是
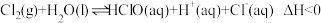 ,达到平衡后,下列说法
,达到平衡后,下列说法A.升高温度,氯水中的 减小 减小 |
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大 增大 |
C.取氯水稀释,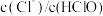 增大 增大 |
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以证明上述反应存在限度 |
您最近一年使用:0次
2022-06-14更新
|
7624次组卷
|
28卷引用:海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题
海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题(已下线)专题20 溶液中粒子浓度大小的比较-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点09 盘点溶液中的“四大”平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)模块综合检测卷2(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)考点22 化学平衡状态与化学平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第三章 水溶液中的离子反应与平衡 第一节 电离平衡浙江省余姚中学2023-2024学年高二上学期第一次月考化学试题(已下线)第2讲 化学平衡状态及化学平衡的移动(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省江门市第一中学2023-2024学年高二上学期第二次段考化学(选考)试题上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题2024届海南省海南中学高三下学期第一次模拟化学试题2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题11-20(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第29练 化学反应的调控-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第10讲 氯及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第21讲 化学平衡状态 化学平衡的移动(练)-2023年高考化学一轮复习讲练测(全国通用)江西省新余市第一中学2022-2023学年高二上学期开学考试化学试题(已下线)第19讲 化学平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题安徽省芜湖市安徽师范大学附属中学2022-2023学年高二上学期期中考查化学试题(已下线)【2022】【高二上】【期中考】【高中化学】59陕西省西安市2023-2024学年高二上学期期末化学测试卷B
名校
5 . 用下列实验装置进行相应实验(夹持装置未画出),说法不正确的是
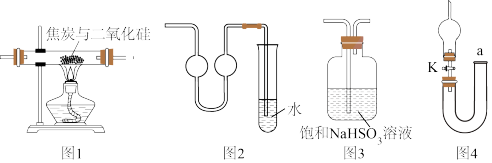

| A.图1装置检验出有CO生成,能证明焦炭与二氧化硅发生了反应 |
| B.图2可用作少量氨气的尾气吸收装置 |
| C.图3装置可以除去SO2中的少量HCl |
| D.图4关闭活塞K,从a处加水可检验装置气密性 |
您最近一年使用:0次
2021-03-15更新
|
774次组卷
|
6卷引用:海南省海南中学2023-2024学年高三上学期第2次月考化学试题
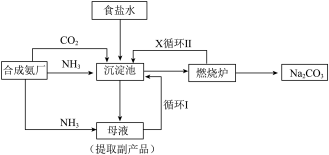
6 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示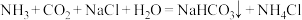 。
。
(1)“侯氏制碱法”誉满全球,其中的“碱”为_______ ,俗称_______ 。
(2)实验室模拟“侯氏制碱法”,下列操作未涉及的是_______。
(3)燃烧炉中发生反应的化学方程式为_______ 。
(4)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了_______ (填I或Ⅱ)的循环。上述流程中X的分子式_______ 。
(5)该流程提取的副产品为_______ 。
(6)为验证产品是否含有NaCl,可取少量试样溶于水后,_______ ,则证明含有NaCl。
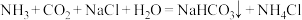 。
。(1)“侯氏制碱法”誉满全球,其中的“碱”为
(2)实验室模拟“侯氏制碱法”,下列操作未涉及的是_______。
A. | B. | C.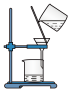 | D.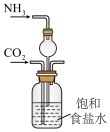 |
(3)燃烧炉中发生反应的化学方程式为
(4)使用原料氯化钠的利用率从70%提高到90%以上,主要是设计了
(5)该流程提取的副产品为
(6)为验证产品是否含有NaCl,可取少量试样溶于水后,
您最近一年使用:0次
7 . 84消毒液适用于家庭、医院、饭店及其他公共场所的物体表面消毒。某小组针对84消毒液的性质展开探究。
实验一:探究84消毒液的氧化性
资料显示:洁厕灵(含盐酸)和84消毒液不能混合使用,否则易产生有毒气体。
他们利用如图所示装置探究上述资料的真实性。
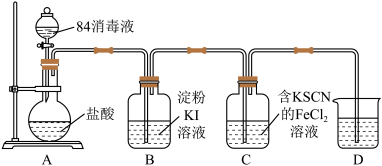
(1)盛装84消毒液的仪器名称是
(2)D装置中应盛装
(3)若B装置中出现
(4)若实验中观察到C装置中溶液先变红色后变黄色,则红色变黄色的原因可能是
实验二:探究84消毒液的漂白性
(5)一定体积和浓度的84消毒液的漂白效率与温度的关系如图所示:
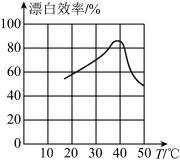
温度高于40℃时,漂白效率急剧减弱的原因可能是
(6)为了探究84消毒液的漂白效率与pH的关系,设计如下实验:
3%的84消毒液 |
|
| 5%品红溶液 | 蒸馏水 | 实验现象 | |
① | 0 | 0 | 2mL | 5滴 | 0 | 不褪色 |
② | 0 | 2mL | 0 | 5滴 | 0 | 不褪色 |
③ | 10mL | 0 | 0 | 5滴 | 5mL | 较快褪色 |
④ | 10mL | 2mL | 0 | 5滴 | 3mL | 缓慢褪色 |
⑤ | 10mL | 0 | 2mL | 5滴 | 3mL | 很快褪色 |
由上述实验可得出的结论是
您最近一年使用:0次
解题方法
8 . 根据如图所示装置(部分仪器已略去)回答下列有关问题。
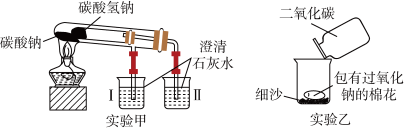
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是_______ (填“I”或“II”),实验甲中该反应烧杯中发生反应的离子方程式是_______ 。
(2)通过实验甲可证明_______ (填“ ”或“
”或“ ”)更稳定。
”)更稳定。
(3)实验乙用来探究 与
与 的反应,观察到的实验现象为包有
的反应,观察到的实验现象为包有 的棉花着火。写出
的棉花着火。写出 与
与 反应的化学方程式:
反应的化学方程式:_______ ,棉花着火说明该反应的特点是_______ (填“放热反应”、“吸热反应”)。
(4)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的 气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为_______ 。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)通过实验甲可证明
 ”或“
”或“ ”)更稳定。
”)更稳定。(3)实验乙用来探究
 与
与 的反应,观察到的实验现象为包有
的反应,观察到的实验现象为包有 的棉花着火。写出
的棉花着火。写出 与
与 反应的化学方程式:
反应的化学方程式:(4)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的
 气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
名校
9 . 完成下列问题
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为 )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为_______ ,该反应中氧化剂和还原剂的个数比为_______ ,该反应每生成2个 转移
转移_______ 个电子。
(2)某同学拟用该原理按如下装置制备并收集纯净的 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置_______ (填“甲”“乙”或“丙”)。 中除
中除 外还含有
外还含有_______ (填化学式),试剂X是_______ 。
(4)通过大量实验证明, 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如_______ 所示(图1或图2),氯离子浓度随时间变化如_______ 所示(图1或图2),请在图3中画出氧气的体积随时间变化的趋势图_______ 。
(1)18世纪70年代,瑞典化学家舍勒将软锰矿(主要成分为
 )与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为
)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。该反应的化学方程式为 转移
转移(2)某同学拟用该原理按如下装置制备并收集纯净的
 ,在虚线框内选用的发生装置
,在虚线框内选用的发生装置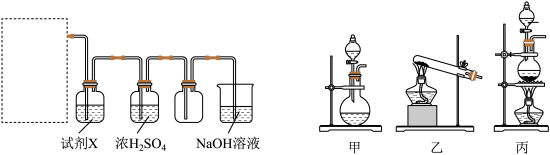
 中除
中除 外还含有
外还含有(4)通过大量实验证明,
 与
与 反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如
反应生成HClO,HClO能杀菌消毒。可利用数字化实验探究HClO的化学性质,用强光照射氯水,得到氯水的pH随时间变化如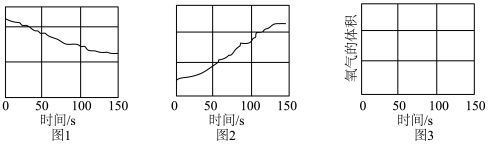
您最近一年使用:0次
10 . Ⅰ.为探究氯气的反应,某课外小组用下图装置进行实验(夹持仪器已略去,气密性已检验),装置A中发生反应的化学方程式为 。打开A中分液漏斗活塞,放下部分浓盐酸,加热,可观察到装置B中溶液变蓝色。已知:淀粉的特征反应——遇
。打开A中分液漏斗活塞,放下部分浓盐酸,加热,可观察到装置B中溶液变蓝色。已知:淀粉的特征反应——遇 变蓝色。
变蓝色。
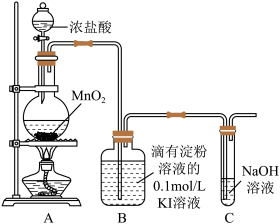
(1)装置A中生成氯气的反应,氧化剂与还原剂的个数之比是:________ ,氧化产物与还原产物的个数之比是________ 。
(2)装置证B中的实验现象可证明氧化性
________  (填“>”或“<”)。
(填“>”或“<”)。
(3)装置C中NaOH的作用是________ 。
Ⅱ.实验结束后,该小组把多余的氯气通入水中,研究氯水性质。
(4)证明氯水中含有氯离子的方案是________ 。
(5)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。

上两图中曲线变化的原因是________ 。
 。打开A中分液漏斗活塞,放下部分浓盐酸,加热,可观察到装置B中溶液变蓝色。已知:淀粉的特征反应——遇
。打开A中分液漏斗活塞,放下部分浓盐酸,加热,可观察到装置B中溶液变蓝色。已知:淀粉的特征反应——遇 变蓝色。
变蓝色。
(1)装置A中生成氯气的反应,氧化剂与还原剂的个数之比是:
(2)装置证B中的实验现象可证明氧化性

 (填“>”或“<”)。
(填“>”或“<”)。(3)装置C中NaOH的作用是
Ⅱ.实验结束后,该小组把多余的氯气通入水中,研究氯水性质。
(4)证明氯水中含有氯离子的方案是
(5)同学们发现久置的氯水会失去漂白性,溶液由黄绿色变为无色。为探究氯水失效的原因,进行实验:用强光照射盛有氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到如下曲线。

上两图中曲线变化的原因是
您最近一年使用:0次


 溶液
溶液

