1 . I.化学小组的同学用10mol/L的浓硫酸配制100mL物质的量浓度为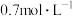 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。
(1)需要量取________ mL上述浓硫酸进行配制。
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是________ 。
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是________ (填序号)。
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为________ 。
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是________ ;产生该现象原因是________________ (用化学方程式解释)。
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是________ 。
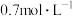 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。(1)需要量取
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是
您最近一年使用:0次
2 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是________ 。
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为________ 。
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为________ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是________ (填化学式,用“>”连接)。
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为________ 。
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是________ 。

(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是
您最近一年使用:0次
解题方法
3 . 表示下列反应的离子方程式正确的是
A.铁跟稀硫酸反应: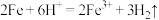 |
B.NaHCO3溶液和NaOH溶液反应: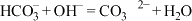 |
C.氢氧化钡溶液和稀硫酸反应: |
D.向澄清石灰水中通入少量CO2: |
您最近一年使用:0次
解题方法
4 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
| A.Fe2O3(Al2O3):加入足量NaOH溶液,过滤 |
| B.NaHCO3溶液(Na2CO3):通入足量的CO2 |
| C.FeCl3溶液(FeCl2):通入足量的氯气 |
| D.CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
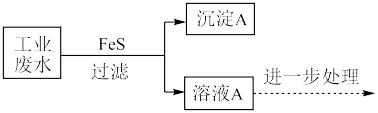
5 . 利用FeS作为沉淀剂除去某工业废水中Pb2+的部分流程如下:
(1)结合化学用语,从平衡移动角度解释可用FeS除去Pb2+的原因___________ 。
(2)可使(1)中平衡发生移动所需最小c(Pb2+)=___________ mol·L-1。(只写计算结果)
(3)处理1 L含Pb2+浓度为3.07 mg·L-1的该废水至合格(Pb2+浓度小于1 mg·L-1)最少所需FeS的质量是___________ mg。
| 溶度积(均为18~25℃数据) | |
| Ksp(FeS) | Ksp(PbS) |
| 约为10-18 | 约为10-28 |
(1)结合化学用语,从平衡移动角度解释可用FeS除去Pb2+的原因
(2)可使(1)中平衡发生移动所需最小c(Pb2+)=
(3)处理1 L含Pb2+浓度为3.07 mg·L-1的该废水至合格(Pb2+浓度小于1 mg·L-1)最少所需FeS的质量是
您最近一年使用:0次
名校
6 . 下列说法中正确的是
| A.电解氯化铜溶液就是氯化铜的电离 |
| B.电解氯化铜溶液是化学变化,不通电也能发生 |
| C.氯化铜溶液是强电解质 |
| D.电解是最强的氧化还原手段,不能自发进行的氧化还原也可以发生 |
您最近一年使用:0次
名校
7 . 下图是一个双液原电池装置图,试回答下列问题。___________ 。
(2)下列说法正确的是___________。

(2)下列说法正确的是___________。
| A.盐桥中的负离子向ZnSO4溶液中移动 | B.电子从铜片经灵敏电流计流向锌片 |
| C.锌片作电池的正极 | D.铜片质量不变 |
您最近一年使用:0次
8 . 与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O和一种未知物质X。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是___________ ,被氧化的元素是___________ 。
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为___________ 。
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。___________
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
(5)在该反应中转移电子2mol时,生成H3PO4___________ mol。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为
(3)完成并配平上述反应的化学方程式,标出电子转移方向和数目。
___________PH3+___________H2SO4+___________KClO3=___________K2SO4+___________H3PO4+___________H2O+___________
(4)根据上述反应可推知___________。
| A.氧化性:KClO3 > H3PO4 | B.氧化性:KClO3 > H2O |
| C.还原性:PH3 > X | D.还原性:PH3 > K2SO4 |
您最近一年使用:0次
名校
9 . 下列有关氧化还原反应的叙述,正确的是
| A.“蜡炬成灰泪始干”中“蜡炬成灰”过程中只发生了物理反应 |
| B.有单质参加或有单质生成的化学反应一定是氧化还原反应 |
| C.氧化还原反应本质上是两个半反应之间竞争电子的反应 |
| D.向CuSO4溶液中通入H2S气体,生成黑色沉淀,此过程中发生了氧化还原反应 |
您最近一年使用:0次
名校
解题方法
10 . 室温下,通过下列实验探究 溶液的性质。
溶液的性质。
(1)实验1的溶液中存在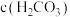
___________  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(2)实验2过程中,水的电离程度___________ (填“逐渐增大”“逐渐减小”或“基本不变”)
(3)实验3反应后的溶液中,所含离子浓度大小与关系正确的是___________。
(4)从平衡移动角度解释实验4中产生气体和沉淀的原因:___________ 。
(5)若想使碳酸氢钠溶液中 的比值变小,可加入的物质是___________。
的比值变小,可加入的物质是___________。
 溶液的性质。
溶液的性质。| 实验1 | 用pH试纸测得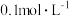  溶液的pH约为8 溶液的pH约为8 |
| 实验2 | 向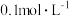  溶液中加入等体积 溶液中加入等体积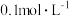 盐酸 盐酸 |
| 实验3 | 向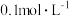  溶液中加入等体积 溶液中加入等体积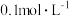 NaOH溶液 NaOH溶液 |
| 实验4 | 向浓 溶液中加入浓 溶液中加入浓 溶液,有气体和沉淀生成 溶液,有气体和沉淀生成 |
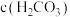
 (填“>”“<”或“=”)
(填“>”“<”或“=”)(2)实验2过程中,水的电离程度
(3)实验3反应后的溶液中,所含离子浓度大小与关系正确的是___________。
A. |
B. |
C. |
D.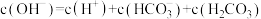 |
(5)若想使碳酸氢钠溶液中
 的比值变小,可加入的物质是___________。
的比值变小,可加入的物质是___________。| A.通入HCl | B.NaOH固体 | C.通入CO2 | D. 固体 固体 |
您最近一年使用:0次



