A.棕色的 体系加压后,颜色先变深后逐渐变浅 体系加压后,颜色先变深后逐渐变浅 |
| B.在配制硫酸亚铁溶液时往往要加入少量铁粉 |
| C.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
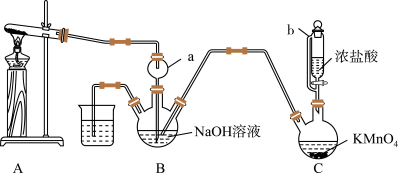
(1)N2H4的电子式是
(2)仪器b的名称为
(3)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(4)采用上述装置制备N2H4时产率较低,可能的原因是
(5)写出装置
 中生成N2H4的化学方程式
中生成N2H4的化学方程式(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
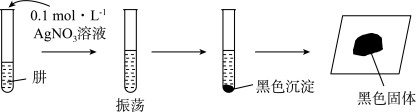
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
操作 | 现象 | 结论 |
 取少量黑色固体于试管中,加入足量 取少量黑色固体于试管中,加入足量 | 黑色固体部分溶解 | 黑色固体中有Ag2O |
 取少量黑色固体于试管中,加入足量稀硝酸,振荡 取少量黑色固体于试管中,加入足量稀硝酸,振荡 | 黑色固体是Ag和Ag2O,则肼具有的性质是碱性和 |
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为
| A.月球中的3He与地球上的3H互为同位素 |
| B.“太空快递小哥”天舟六号壳体材料主要为铝合金,其强度大于纯铝 |
C.“问天”实验舱使用砷化镓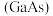 太阳能电池,其中 太阳能电池,其中 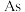 位于周期表的d区 位于周期表的d区 |
| D.长征七号遥七运载火箭采用液氧、煤油等燃料作为推进剂,液氧和煤油均属于混合物 |
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向NaAlO2溶液中滴加NaHCO3溶液 | 出现白色沉淀 | NaAlO2与NaHCO3水解相互促进 |
| B | 常温下,用pH计分别测定相同浓度的NaClO溶液和CH3COONa溶液的酸碱性 | NaClO溶液pH较大 | 酸性:HClO<CH3COOH |
| C | 向AgNO3溶液中依次滴加NaCl、KI溶液 | 依次出现白色、黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| D | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴入几滴K2[Fe(CN)6]溶液 | 无明显现象 | 该过程未发生原电池反应 |
| A.A | B.B | C.C | D.D |
A. 的水解方程式: 的水解方程式: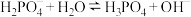 |
B.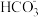 的电离方程式: 的电离方程式: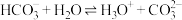 |
C.CaCO3的沉淀溶解平衡表达式: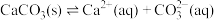 |
D.表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(l)  kJ⋅mol kJ⋅mol |
| A.“保暖贴”在发热过程中应用的是原电池的工作原理 |
| B.医学上常采用硫酸钡作为钡餐,因为硫酸钡难被盐酸溶解 |
C.纯碱可以用作锅炉除垢时 的转化剂 的转化剂 |
D.明矾 可用作净水剂和消毒剂 可用作净水剂和消毒剂 |
7 . 水杨酸A具有解热镇痛的功效,其可作为医药工业的原料,用水杨酸制备平喘药沙丁胺醇的路线如下(Ac表示-COCH3;Ph表示-C6H5)。
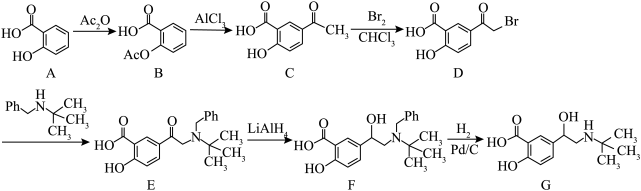
(1)化合物 A的分子式为
 的反应类型为
的反应类型为(2)化合物 D中含有四种官能团,任选两种官能团进行检验。
限选试剂:NaOH溶液、稀硝酸、稀硫酸、新制氢氧化铜悬浊液、饱和溴水、硝酸银、NaHCO3溶液、FeCl3溶液。
官能团名称 | 所选试剂 | 实验现象 |
(3)化合物M(
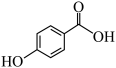 )是化合物A的同分异构体,其沸点M
)是化合物A的同分异构体,其沸点M(4)化合物C有多种同分异构体,写出其中一种能同时满足下列条件的芳香族化合物的结构简式
①能发生水解反应且最多能与4倍物质的量的NaOH反应
②核磁共振氢谱有四组峰,峰面积之比为 3:2:2:1
(5)以水杨酸
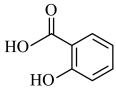 、乙二醇以及甲基丙烯酸(
、乙二醇以及甲基丙烯酸(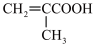 )为原料,利用
)为原料,利用 的原理及所学知识,合成
的原理及所学知识,合成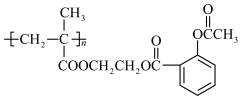
基于你设计的路线,回答下列问题。
①从水杨酸出发,第一步反应的化学方程式为
②最后一步反应中,反应物为
8 . 油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式;
①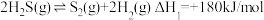
②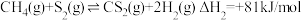
③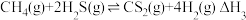
则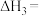
(2)下列叙述能说明反应③达到平衡状态的是 (填字母序号)。
| A.2v正(H2S)=v逆(CS2) | B.恒温恒容条件下,体系压强不再变化 |
| C.气体的总质量不再变化 | D.混合气体平均摩尔质量不再变化 |
(3)反应压强为100kPa,投料比n(CH4)/n(H2S)分别为a、b、c的条件下,反应③中H2S的平衡转化率随温度变化情况如图1所示,则a、b、c由大到小的顺序为
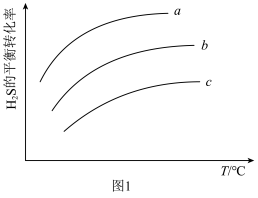
(4)在1275K、100kPa反应条件下,将物质的量之比为3:3:2的H2S、CH4、N2混合气进行反应③(N2不参与反应),平衡时混合气中CS2的分压与H2S的分压相同,H2S的平衡转化率为
 总压
总压 物质的量分数)。
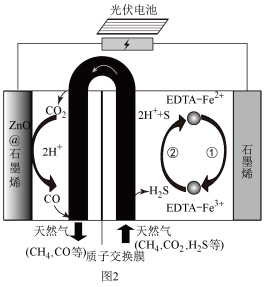
物质的量分数)。(5)我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO2和H2S的高效去除,过程如图2所示,则阳极区发生的总反应为
9 . 镓锗是重要的战略金属资源丹霞冶炼厂以锌精矿(主要成分为ZnS,还含有铁、铜、和锗等金属硫化物)为原料制备Zn、Ga、Ge的工艺流程如图所示:
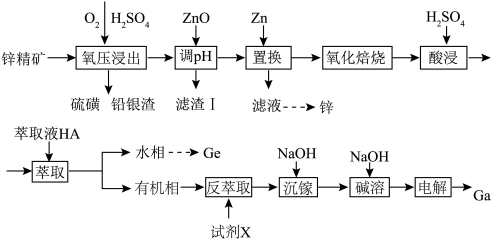
已知:①该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
金属离子 | Fe3+ | Ga3+ | Cu2+ |
开始沉淀时的pH | 2.5 | 3.5 | 5.3 |
沉淀完全时的pH | 3.3 | 4.6 | 6.4 |
②镓与铝同主族,化学性质相似。
(1)基态镓原子的核外电子排布式为
(2)“氧压浸出”时,ZnS发生反应的化学方程式是
(3)“滤渣I”的主要成分为
(4)“萃取”的原理为Mn+(水相)+nHA(有机相)
 MAn(有机相)+nH+(水相)(M为Cu或Ga),则“反萃取”工序中的试剂X宜选用
MAn(有机相)+nH+(水相)(M为Cu或Ga),则“反萃取”工序中的试剂X宜选用(5)反萃取后的水溶液中含有Ga3+、Cu2+,“沉镓”时应控制溶液的pH范围为
(6)写出“碱溶”过程中发生反应的离子方程式
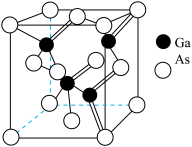
(7)砷化镓GaAs是一种重要的半导体材料,其晶体的立方体晶胞如图所示,设晶胞边长为apm,阿伏加德罗常数为NA,则晶胞的密度为
10 . 我国科研人员将单独脱除SO2的反应与H2O2的制备反应相结合,实现协同转化。协同转化装置如图所示。在电场作用下,双极膜中间层的H2O解离为OH-和H+,并向两极迁移。下列分析正确的
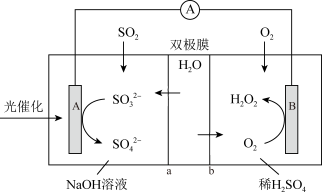
| A.双极膜的a侧应为阳离子交换膜,b侧为阴离子交换膜 |
| B.每脱除标准状况下11.2L的SO2,双极膜处有2mol的H2O解离 |
| C.反应过程中不需补加稀 H2SO4 |
| D.协同转化的总反应为:SO2+O2+2H2O=H2O2+H2SO4 |



