1 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:___________ 性。从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小明认为可能是___________ 。小王觉得可以设计实验验证这一推论,具体操作是___________ 。
(3)配平下列反应:___________ 。
___________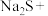 ___________
___________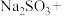 ___________
___________ ___________
___________ ___________
___________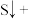 ___________
___________
(4)一种铁基脱硫剂脱除硫化氢( )的方法包括吸收和再生两个阶段,其工艺流程原理如下:
)的方法包括吸收和再生两个阶段,其工艺流程原理如下:___________ 写出“再生”的反应的离子方程式:___________ 。
②当吸收224 mL(标准状况) 时,若要保持脱硫液中
时,若要保持脱硫液中 的物质的量不变,则所通入的氧气的体积为
的物质的量不变,则所通入的氧气的体积为___________ mL。

(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小明认为可能是
(3)配平下列反应:
___________
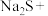 ___________
___________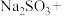 ___________
___________ ___________
___________ ___________
___________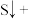 ___________
___________
(4)一种铁基脱硫剂脱除硫化氢(
 )的方法包括吸收和再生两个阶段,其工艺流程原理如下:
)的方法包括吸收和再生两个阶段,其工艺流程原理如下:
②当吸收224 mL(标准状况)
 时,若要保持脱硫液中
时,若要保持脱硫液中 的物质的量不变,则所通入的氧气的体积为
的物质的量不变,则所通入的氧气的体积为
您最近一年使用:0次
解题方法
2 . 海洋资源的利用具有非常广阔的前景。回答下列问题:
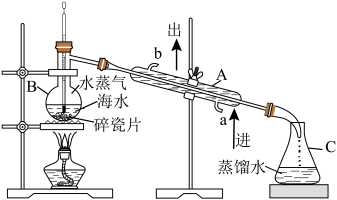
(1)实验室模拟蒸馏法淡化海水如图所示,应向蒸馏烧瓶中加入沸石,目的是___________ 。下述装置图中有___________ 处错误。 、
、 、
、 ,要除去这些杂质离子得到精盐水,加入以下试剂的顺序可为
,要除去这些杂质离子得到精盐水,加入以下试剂的顺序可为___________ (填字母,可重复选用)。
a.NaOH溶液 b. 溶液 c.
溶液 c. 溶液 d.盐酸
溶液 d.盐酸
(3)根据以下数据分析,为什么冶炼镁时选择氯化镁,而冶炼铝时却选择氧化铝?
理由:___________ 。
(4)从海水中提取溴的工业过程如下图所示: .写出步骤②中苦卤(NaBr)被氯气氧化的化学反应方程式
.写出步骤②中苦卤(NaBr)被氯气氧化的化学反应方程式___________ 。
 .请写出步骤④反应的离子方程式:
.请写出步骤④反应的离子方程式:___________ 。
 .上述过程中步骤③④⑤的目的是
.上述过程中步骤③④⑤的目的是___________ 。
(1)实验室模拟蒸馏法淡化海水如图所示,应向蒸馏烧瓶中加入沸石,目的是
 、
、 、
、 ,要除去这些杂质离子得到精盐水,加入以下试剂的顺序可为
,要除去这些杂质离子得到精盐水,加入以下试剂的顺序可为a.NaOH溶液 b.
 溶液 c.
溶液 c. 溶液 d.盐酸
溶液 d.盐酸(3)根据以下数据分析,为什么冶炼镁时选择氯化镁,而冶炼铝时却选择氧化铝?
| 物质 | MgO |  |  |  |
| 熔点/℃ | 2852 | 2054 | 714 | 190 |
(4)从海水中提取溴的工业过程如下图所示:

 .写出步骤②中苦卤(NaBr)被氯气氧化的化学反应方程式
.写出步骤②中苦卤(NaBr)被氯气氧化的化学反应方程式 .请写出步骤④反应的离子方程式:
.请写出步骤④反应的离子方程式: .上述过程中步骤③④⑤的目的是
.上述过程中步骤③④⑤的目的是
您最近一年使用:0次
解题方法
3 . 下列化学用语正确的是
A.HCl的电子式 | B.次氯酸的结构式: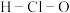 |
C. 的基本结构单元结构为 的基本结构单元结构为 | D.Cl-的结构示意图 |
您最近一年使用:0次
解题方法
4 . 某溶液中含有下表所示离子中的5种,其中各离子的数目相等。向该溶液中加入足量稀盐酸,有气体生成,反应前后阴离子种类不变。下列说法错误的是
已知: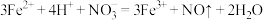
| 阳离子 |  、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 |
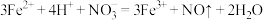
| A.生成的气体为NO | B.原溶液中一定不含有Na+ |
C.原溶液中一定不含 | D.原溶液中含有3种阳离子、2种阴离子 |
您最近一年使用:0次
解题方法
5 . 下列离子方程式书写正确的是
A.刻蚀玻璃: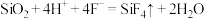 |
B.碳酸氢钠和少量澄清石灰水: |
C.向氯水中通入少量的 : : |
D. 与水的反应: 与水的反应: |
您最近一年使用:0次
6 . 下列属于物理变化的是
①石油的分馏 ②煤的干馏 ③煤的液化 ④溴水中加入苯,振荡、静置后水层无色 ⑤焊接钢轨
⑥用卤水点热豆浆制豆腐 ⑦水处理用臭氧消毒杀菌 ⑧白磷加热到260℃转化为红磷 ⑨电渗析法进行海水淡化
①石油的分馏 ②煤的干馏 ③煤的液化 ④溴水中加入苯,振荡、静置后水层无色 ⑤焊接钢轨
⑥用卤水点热豆浆制豆腐 ⑦水处理用臭氧消毒杀菌 ⑧白磷加热到260℃转化为红磷 ⑨电渗析法进行海水淡化
| A.①④⑥ | B.②④⑧⑨ | C.①③⑤⑦ | D.④⑥⑨ |
您最近一年使用:0次
名校
7 .  可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分
可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分 ,杂质为
,杂质为 )和黄铁矿
)和黄铁矿 为原料制备
为原料制备 其流程如图。
其流程如图。
回答下列问题:
(1) 的价层电子排布图
的价层电子排布图_______ ,“酸浸”过程中,滤渣1的主要成分为S、_______ (填化学式)。
(2)“酸浸”过程中 、
、 的质量浓度、Mn的浸出率与时间的关系如图所示。
的质量浓度、Mn的浸出率与时间的关系如图所示。_______ 。
②80~100min时, 浓度上升的原因可能是
浓度上升的原因可能是_______ 。
(3)“沉铁”过程中依次加入的试剂X、Y为_______ (填字母)。
A.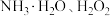 B.
B. C.
C.
(4)“滤液”萃取前调 ,若有机萃取剂用表HR示,则发生萃取的反应可表示为
,若有机萃取剂用表HR示,则发生萃取的反应可表示为 。若,
。若,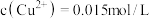 多次萃取后水相中
多次萃取后水相中 为
为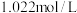 ,则铜的萃取率为
,则铜的萃取率为_______ (结果保留小数点后一位,溶液体积变化忽略不计)。
(5)利用 溶液,用空气氧化法制备
溶液,用空气氧化法制备 。在
。在 溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备
溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备 。写出上述反应的离子方程式:
。写出上述反应的离子方程式:_______ 。
(6)结合图像分析,若要获得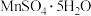 晶体的系列操作步骤为加热
晶体的系列操作步骤为加热_______ 得到_______ ℃饱和溶液,_______ ,过滤酒精洗涤,低温干燥。
 可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分
可用于电子工业生产软磁铁氧体,工业上常以电解金属锰阳极渣(主要成分 ,杂质为
,杂质为 )和黄铁矿
)和黄铁矿 为原料制备
为原料制备 其流程如图。
其流程如图。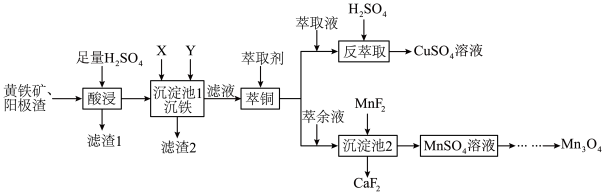
 |  |  |  | |
| 完全沉淀时的pH | 3.7 | 9.7 | 7.4 | 9.8 |
(1)
 的价层电子排布图
的价层电子排布图(2)“酸浸”过程中
 、
、 的质量浓度、Mn的浸出率与时间的关系如图所示。
的质量浓度、Mn的浸出率与时间的关系如图所示。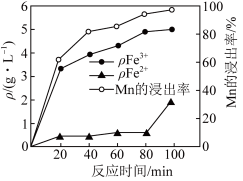
②80~100min时,
 浓度上升的原因可能是
浓度上升的原因可能是(3)“沉铁”过程中依次加入的试剂X、Y为
A.
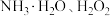 B.
B. C.
C.
(4)“滤液”萃取前调
 ,若有机萃取剂用表HR示,则发生萃取的反应可表示为
,若有机萃取剂用表HR示,则发生萃取的反应可表示为 。若,
。若,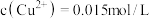 多次萃取后水相中
多次萃取后水相中 为
为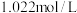 ,则铜的萃取率为
,则铜的萃取率为(5)利用
 溶液,用空气氧化法制备
溶液,用空气氧化法制备 。在
。在 溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备
溶液中滴入一定浓度的氨水,加压通氧气反应7小时制备 。写出上述反应的离子方程式:
。写出上述反应的离子方程式:(6)结合图像分析,若要获得
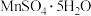 晶体的系列操作步骤为加热
晶体的系列操作步骤为加热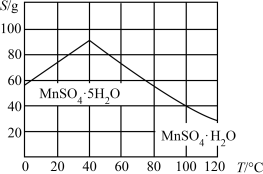
您最近一年使用:0次
名校
解题方法
8 . 下列各组离子在给定溶液中能大量共存的是
A.滴加石蕊变红的溶液: 、 、 、 、 、 、 |
B.0.2 mol∙L-1的NH4Cl溶液: 、 、 、 、 、 、 |
C.在0.1 mol∙L-1醋酸溶液中: 、 、 、 、 、 、 |
D.无色透明溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
9 . 我国古代四大发明之一黑火药的爆炸反应为 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.11.2L N2含π键数目为NA |
| B.每生成13.2g CO2转移电子数目为NA |
| C.0.1molKNO3晶体中含离子数目为0.2 NA |
| D.1L 0.1 mol∙L-1K2S溶液中含S2-数目为0.1 NA |
您最近一年使用:0次
名校
10 . 过硫酸钠(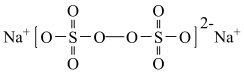 ),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对
),易溶于水,加热至65℃分解。作为强氧化剂,广泛应用于蓄电池工业、造纸工业、食品工业等。某化学小组对 制备和性质及用途进行探究。
制备和性质及用途进行探究。

工业制备过硫酸钠的反应原理:
主反应:

副反应:

实验室设计如图实验装置:
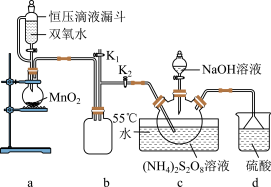
(2)装置b的作用是
(3)上述反应过程中,d装置中主要发生的化学反应方程式为
Ⅱ.探究
 的性质与用途
的性质与用途(4)
 用于废水中苯酚的降解
用于废水中苯酚的降解已知:a.
 具有强氧化性,
具有强氧化性, 浓度较高时会导致
浓度较高时会导致 淬灭。
淬灭。b.
 可将苯酚氧化,但反应速率较慢,加入
可将苯酚氧化,但反应速率较慢,加入 可加快反应。
可加快反应。过程为ⅰ.

ⅱ.
 将苯酚氧化为
将苯酚氧化为 气体
气体①
 氧化苯酚的离子方程式是
氧化苯酚的离子方程式是②将含
 的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。
的溶液稀释后加入苯酚的废水处理器中,调节溶液总体积为1L,pH=1,测得在相同时间内,不同条件下苯酚的降解率如图甲。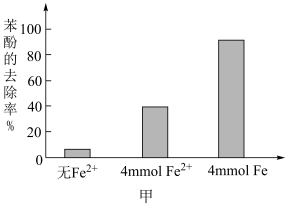
 ,可明显提高苯酚的降解率,主要原因是
,可明显提高苯酚的降解率,主要原因是(5)工业上利用
 能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含
能有效处理燃煤锅炉烟气中的NO气体。一定条件下,将含一定浓度NO的烟气以一定的速率通过含 的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为
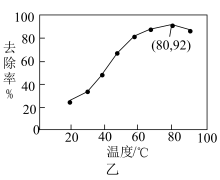
的处理液中,NO去除率随温度变化的关系如图乙所示,80℃时,NO去除率为92%。若NO初始浓度为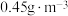 ,
, 达到最大去除率,NO去除的平均反应速率:
达到最大去除率,NO去除的平均反应速率:
 。
。
您最近一年使用:0次



