1 . 锌是一种重要的金属,锌及其化合物被广泛应用于汽车、建筑、船舶、电池等行业。现某科研小组以固体废锌催化剂(主要成分是 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示:
①“浸取”时, 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。
② 时,
时, ,
, 。
。
③深度除杂标准:溶液中 ≤2.0×10-6。
≤2.0×10-6。
(1)“浸取”温度为 ,锌的浸出率可达
,锌的浸出率可达 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为___________ 。
(2)“滤渣1”的主要成分为 、
、___________ 。
(3)“深度除锰”是将残留的 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式___________ 。
(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比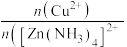 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。
①当 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是___________ (用离子方程式解释)。
②“深度除铜”时 加入量最优选择
加入量最优选择___________ (填标号)。
A.100% B.110% C.120% D.130%
(5) 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:___________ 。
②基态 原子的价电子排布式为
原子的价电子排布式为___________ 。
 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: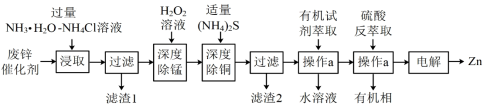
①“浸取”时,
 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。②
 时,
时, ,
, 。
。③深度除杂标准:溶液中
 ≤2.0×10-6。
≤2.0×10-6。(1)“浸取”温度为
 ,锌的浸出率可达
,锌的浸出率可达 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为(2)“滤渣1”的主要成分为
 、
、(3)“深度除锰”是将残留的
 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比
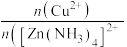 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。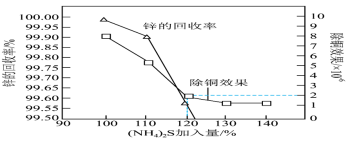
①当
 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是②“深度除铜”时
 加入量最优选择
加入量最优选择A.100% B.110% C.120% D.130%
(5)
 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:
②基态
 原子的价电子排布式为
原子的价电子排布式为
您最近一年使用:0次
2 . 根据所学知识填空
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:___________ 。
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
(3)向1mol KAl(SO4)2溶液中滴加Ba(OH)2溶液至沉淀的物质的量最大时的离子方程式___________
(4)现有以下四种物质:
请根据题意选择恰当的选项用字母代号填空。
①可与KSCN溶液反应,溶液变红的是___________ ;
②常用于焙制糕点,也可用作抗酸药的是___________ ;
③可用于制备硅胶和木材防火剂的是___________ ;
④可用于制造计算机芯片的是___________ 。
(1)正长石的主要成分为KAlSi3O8,将其表示为氧化物形式:
(2)利用焰色反应可以定性鉴别某些金属盐。灼烧Li2SO4时,焰色为___________(填标号)。
| A.黄绿色 | B.洋红色 | C.紫红色 | D.绿色 |
(4)现有以下四种物质:
| A.Si | B.FeCl3 | C.NaHCO3 | D.Na2SiO3 |
①可与KSCN溶液反应,溶液变红的是
②常用于焙制糕点,也可用作抗酸药的是
③可用于制备硅胶和木材防火剂的是
④可用于制造计算机芯片的是
您最近一年使用:0次
名校
3 . 大苏打( )、苏打(
)、苏打( )和小苏打(
)和小苏打( )被誉为“苏氏三兄弟”,在生产、生活中应用广泛。下列化工生产中涉及的离子方程式错误的是
)被誉为“苏氏三兄弟”,在生产、生活中应用广泛。下列化工生产中涉及的离子方程式错误的是
 )、苏打(
)、苏打( )和小苏打(
)和小苏打( )被誉为“苏氏三兄弟”,在生产、生活中应用广泛。下列化工生产中涉及的离子方程式错误的是
)被誉为“苏氏三兄弟”,在生产、生活中应用广泛。下列化工生产中涉及的离子方程式错误的是A.生活中常用泡沫灭火器灭火: |
B.工业上用 溶液和过量的小苏打溶液制备 溶液和过量的小苏打溶液制备 : :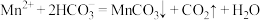 |
C.工业上常用大苏打溶液吸收尾气中的 : : |
D.用石灰乳和饱和苏打溶液制备烧碱:Ca2++CO =CaCO3 =CaCO3 |
您最近一年使用:0次
2024-05-11更新
|
173次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
名校
解题方法
4 . 设 代表阿伏加德罗常数的值。下列关于反应:
代表阿伏加德罗常数的值。下列关于反应: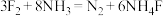 的叙述正确的是
的叙述正确的是
 代表阿伏加德罗常数的值。下列关于反应:
代表阿伏加德罗常数的值。下列关于反应: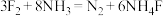 的叙述正确的是
的叙述正确的是| A.上述反应中,氧化剂与还原剂的物质的量之比为3:8 |
B. 固体中含离子数为 固体中含离子数为 |
C.14g氧化产物含孤电子对数为 |
D. 完全反应时转移电子数为 完全反应时转移电子数为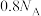 |
您最近一年使用:0次
2024-05-11更新
|
62次组卷
|
2卷引用:江西省部分学校2023-2024学年高三下学期二轮复习联考验收化学试卷
名校
5 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用下图表示。下列关于海洋氮循环的说法不正确的是
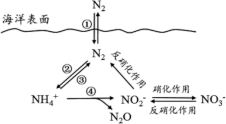
| A.海洋中的氮循环起始于氮的氧化 |
| B.氮循环中涉及氮的固定 |
C.向海洋排放含NO 的废水会影响海洋中NH 的废水会影响海洋中NH 的含量 的含量 |
| D.“硝化作用”可能有氧气的参与 |
您最近一年使用:0次
名校
6 . 下列各图均能表示某种分子的结构,按要求回答下列问题。__________ 模型,其电子式是________________ 。
(2)某气态烃在标准状况下的体积为2.8 L,其质量为2 g,该烃中氢元素的质量分数为25%,则该烃的分子式为________ ,空间构型为________ 。
(3)写出上述中A、E的分子式和结构简式:A.________ ;________________ ; E.________ ;_________________ ;
(4)B中共平面的原子最多有_______ 个,F中共一条直线的原子最多有_______ 个,
(5)互为同系物的是_______ 。互为同分异构体的是_______ 。(填序号)
(6)酚酞是常用的酸碱指示剂,其结构简式如图所示:
A.  B.
B.  C.
C.  D.
D.  E.
E. 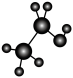 F.
F. 
(2)某气态烃在标准状况下的体积为2.8 L,其质量为2 g,该烃中氢元素的质量分数为25%,则该烃的分子式为
(3)写出上述中A、E的分子式和结构简式:A.
(4)B中共平面的原子最多有
(5)互为同系物的是
(6)酚酞是常用的酸碱指示剂,其结构简式如图所示:
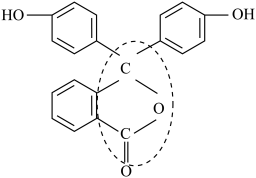
| A.烯烃 | B.芳香化合物 | C.醚类物质 | D.酯类物质 |
您最近一年使用:0次
名校
7 . 设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.常温常压下,50g46%的乙醇水溶液中,含O-H键的总数为3NA |
| B.标准状况下,22.4L乙烷中含有的极性键的数目为6NA |
| C.90g葡萄糖分子中含羟基的数目为3NA |
| D.在浓硫酸、加热的条件下,0.5mol乙酸与足量乙醇充分反应,生成的乙酸乙酯分子数为0.5NA |
您最近一年使用:0次
名校
解题方法
8 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀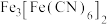 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀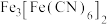 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
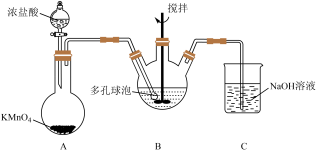
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
名校
解题方法
9 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,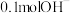 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为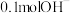 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近一年使用:0次
名校
10 . 设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A. 与 与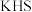 的混合物中含有的阴离子的数目为 的混合物中含有的阴离子的数目为 |
B.常温常压下,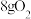 与 与 的混合气体中含有 的混合气体中含有 个电子 个电子 |
C.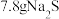 与 与 的混合物,含离子总数为 的混合物,含离子总数为 |
D.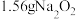 和 和 的混合物中阴、阳离子的总数是 的混合物中阴、阳离子的总数是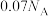 |
您最近一年使用:0次



