23-24高三下·江苏常州·开学考试
1 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
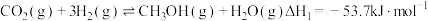
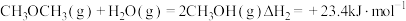
则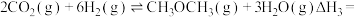
_______ kJ∙mol-1。
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: ,则
,则 的化学式为
的化学式为_______ ,“热分解系统”中每转移 电子,需消耗
电子,需消耗
_______  。
。
(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子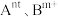 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示:_______ 。
ii.“高温相”具有良好的离子导电性,其主要原因是_______ 。
(4)铜基催化剂 (
( 为
为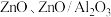 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 上发生反应的总化学方程式
上发生反应的总化学方程式_______ 。
(5)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: 和法拉第效率(
和法拉第效率(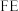 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下:
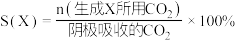

①实验测得,碱性条件生成 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是_______ 。
②实验测得,酸性条件生成 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是_______ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: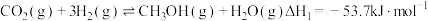
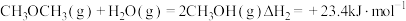
则
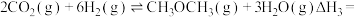
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: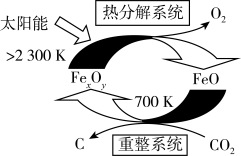
 ,则
,则 的化学式为
的化学式为 电子,需消耗
电子,需消耗
 。
。(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子
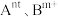 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示: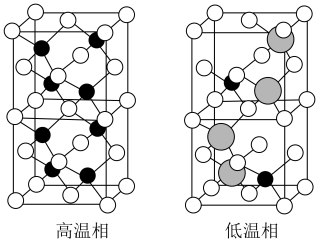
说明:图中,○球为负离子;高温相中的●深色球为正离子或空位;低温相中的 球为
球为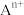 离子,●球为
离子,●球为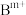 离子。
离子。
ii.“高温相”具有良好的离子导电性,其主要原因是
(4)铜基催化剂
 (
( 为
为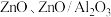 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 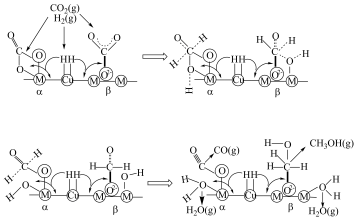
 上发生反应的总化学方程式
上发生反应的总化学方程式(5)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: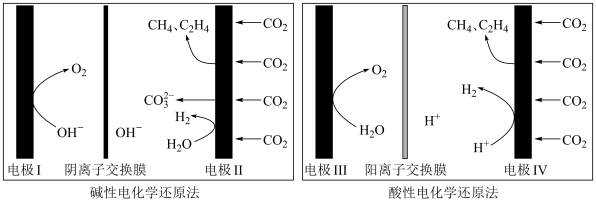
 和法拉第效率(
和法拉第效率(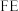 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下: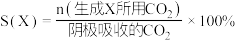

①实验测得,碱性条件生成
 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是②实验测得,酸性条件生成
 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是
您最近一年使用:0次
23-24高三下·江西赣州·阶段练习
解题方法
2 . 钕铁硼永磁材料被广泛应用于汽车、家电、电子产品等领域。以江西赣州某公司的钕铁硼油泥废料(主要物相为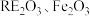 )为原料,回收有价金属的工艺流程如图所示。
)为原料,回收有价金属的工艺流程如图所示。
②配位阴离子的稳定常数越大,配位阴离子越稳定。几种配位阴离子的稳定常数如下:
回答下列问题:
(1)钕(Nd)属于f区元素,其原子轨道共有___________ 种不同的形状。
(2) 溶液能洗涤钕铁硼油泥废料的原因是
溶液能洗涤钕铁硼油泥废料的原因是___________ (用离子方程式表示)。
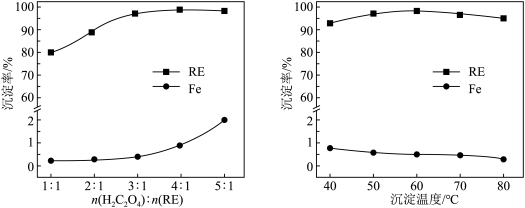
(3)浸取后,对浸取液进行紫外可见光光度测试,结果如图所示。写出 与盐酸反应的离子方程式:
与盐酸反应的离子方程式:___________ 。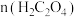 )与
)与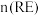 的最佳物质的量之比为
的最佳物质的量之比为___________ ,请说明原因:___________ 。最佳沉淀温度为60℃,,温度继续升高,稀土沉淀率略下降的原因可能是___________ 。
(5)在沉淀后的滤液中加入 ,溶液中主要存在的配位阴离子是
,溶液中主要存在的配位阴离子是___________ ,该离子在加入铁粉后生成 的离子方程式为
的离子方程式为___________ 。
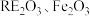 )为原料,回收有价金属的工艺流程如图所示。
)为原料,回收有价金属的工艺流程如图所示。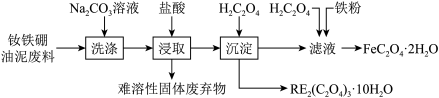
②配位阴离子的稳定常数越大,配位阴离子越稳定。几种配位阴离子的稳定常数如下:
| 配位阴离子 |  | 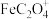 |  | 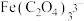 |
| 稳定常数 | 25.4 | 9.4 | 16.2 | 20.2 |
(1)钕(Nd)属于f区元素,其原子轨道共有
(2)
 溶液能洗涤钕铁硼油泥废料的原因是
溶液能洗涤钕铁硼油泥废料的原因是(3)浸取后,对浸取液进行紫外可见光光度测试,结果如图所示。写出
 与盐酸反应的离子方程式:
与盐酸反应的离子方程式: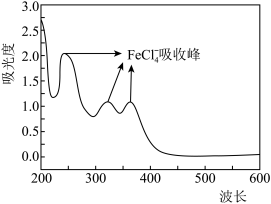
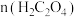 )与
)与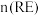 的最佳物质的量之比为
的最佳物质的量之比为(5)在沉淀后的滤液中加入
 ,溶液中主要存在的配位阴离子是
,溶液中主要存在的配位阴离子是 的离子方程式为
的离子方程式为
您最近一年使用:0次
2024-03-09更新
|
487次组卷
|
6卷引用:大题预测卷(江西专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
(已下线)大题预测卷(江西专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)江西省赣州市2024届高三下学期3月摸底考试化学试题江西省赣州市2024届高三下学期年3月摸底考试化学试题(已下线)大题预测卷01 (新高考通用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)(已下线)大题预测卷(安徽专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)(已下线)大题预测卷(新七省高考专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
23-24高三上·贵州黔西·阶段练习
3 . 大苏打( )易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备
)易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备 并探究其性质。
并探究其性质。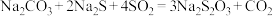 ;
;
② 中S元素的化合价为-2、+6。
中S元素的化合价为-2、+6。
回答下列问题:
(1)给装置A加热应选择_______ (填“水浴”或“酒精灯”)加热。
(2)为了保证 的产量,实验中通入的
的产量,实验中通入的 不能过量,需控制装置A中
不能过量,需控制装置A中 的生成速率,采取的措施是
的生成速率,采取的措施是_______ 。
(3)配制 和
和 混合溶液时,先将
混合溶液时,先将 固体溶于水配成溶液,再将
固体溶于水配成溶液,再将 固体溶于
固体溶于 溶液中,其目的是
溶液中,其目的是_______ 。
(4) 性质的探究。
性质的探究。
①称取一定量的样品,溶解,配成 溶液。
溶液。
②取4mL溶液,向其中加入1mL饱和氯水( ),溶液立即出现浑浊,经检验浑浊物为S。
),溶液立即出现浑浊,经检验浑浊物为S。
假设1:氧化剂氧化: 、HClO等含氯的氧化性微粒氧化了硫元素。
、HClO等含氯的氧化性微粒氧化了硫元素。
假设2:_______(不考虑空气中氧气氧化)。
设计实验方案:
①假设2是_______ 。
②第Ⅱ组实验中胶头滴管加入的试剂是_______ ,发生反应的离子方程式为_______ 。
③依据现象,产生S的主要原因可能是_______ 。
 )易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备
)易溶于水,难溶于乙醇,在中性和碱性环境中稳定,在酸性环境中易变质。某实验小组用下列装置制备 并探究其性质。
并探究其性质。
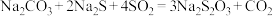 ;
;②
 中S元素的化合价为-2、+6。
中S元素的化合价为-2、+6。回答下列问题:
(1)给装置A加热应选择
(2)为了保证
 的产量,实验中通入的
的产量,实验中通入的 不能过量,需控制装置A中
不能过量,需控制装置A中 的生成速率,采取的措施是
的生成速率,采取的措施是(3)配制
 和
和 混合溶液时,先将
混合溶液时,先将 固体溶于水配成溶液,再将
固体溶于水配成溶液,再将 固体溶于
固体溶于 溶液中,其目的是
溶液中,其目的是(4)
 性质的探究。
性质的探究。①称取一定量的样品,溶解,配成
 溶液。
溶液。②取4mL溶液,向其中加入1mL饱和氯水(
 ),溶液立即出现浑浊,经检验浑浊物为S。
),溶液立即出现浑浊,经检验浑浊物为S。
假设1:氧化剂氧化:
 、HClO等含氯的氧化性微粒氧化了硫元素。
、HClO等含氯的氧化性微粒氧化了硫元素。假设2:_______(不考虑空气中氧气氧化)。
设计实验方案:
| 实验组别 | 胶头滴管滴加试剂 | 现象 |
| 第I组 | 1mL饱和氯水 | 立即出现浑浊 |
| 第Ⅱ组 | _______ | 一段时间后出现浑浊,但浑浊度比第I组小,且有少量气泡生成 |
②第Ⅱ组实验中胶头滴管加入的试剂是
③依据现象,产生S的主要原因可能是
您最近一年使用:0次
2024·广东·模拟预测
名校
解题方法
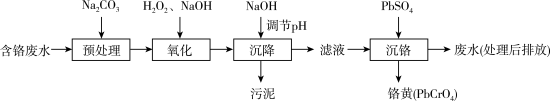
4 . 含铬电镀废水的主要成分如表,常用“Pb2+沉淀法”和“药剂还原沉淀法”进行处理。
I. “Pb2+沉淀法”工艺流程如图。 )及沉淀开始溶解时的pH如表。
)及沉淀开始溶解时的pH如表。
(1)铬元素的价电子排布式:_______ 。已知金属铬为体心立方晶体,密度为7.2g/cm3,求两个Cr原子的最小核间距_______ nm。(只写表达式,不计算)
(2)“氧化”过程中Cr(OH)3转化为 的离子方程式为
的离子方程式为_______ 。
(3)“沉降”过程中应调节pH范围是_______ ~10.5。
(4)已知25℃是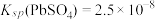 ;
;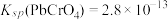 ;
; 。“沉铬”过程中:
。“沉铬”过程中:
①生成铬黄的离子方程式为_______ 。
②从平衡角度分析pH对沉铬率的影响_______ 。
II. “药剂还原沉淀法”工艺流程如图。 被Cr(VI)氧化为
被Cr(VI)氧化为_______ 。
(6)“沉淀”过程中,当溶液pH为8.6时,
_______  。
。
| 离子 | Cr(VI) | Cr3+ | Cu2+ | Fe2+ | Zn2+ |
| 含量mg/L | 28.38 | 12.92 | 0.34 | 0.069 | 0.014 |
 )及沉淀开始溶解时的pH如表。
)及沉淀开始溶解时的pH如表。| 金属离子 | Cu2+ | Fe2+ | Fe3+ | Zn2+ | Cr3+ | |
| pH | 沉淀完全 | 6.7 | 8.3 | 2.8 | 8.2 | 5.6 |
| 沉淀开始溶解 | — | 13.5 | 14.0 | 10.5 | 12.0 | |
(2)“氧化”过程中Cr(OH)3转化为
 的离子方程式为
的离子方程式为(3)“沉降”过程中应调节pH范围是
(4)已知25℃是
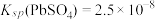 ;
;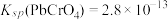 ;
; 。“沉铬”过程中:
。“沉铬”过程中:①生成铬黄的离子方程式为
②从平衡角度分析pH对沉铬率的影响
II. “药剂还原沉淀法”工艺流程如图。
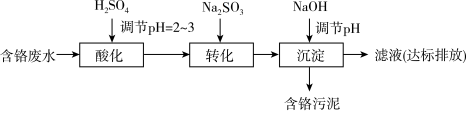
 被Cr(VI)氧化为
被Cr(VI)氧化为(6)“沉淀”过程中,当溶液pH为8.6时,

 。
。
您最近一年使用:0次
2024·江西·模拟预测
5 . 关于反应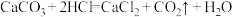 ,下列说法正确的是
,下列说法正确的是
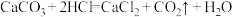 ,下列说法正确的是
,下列说法正确的是A. 分子中没有极性键 分子中没有极性键 | B. 的 的 模型和空间结构一致 模型和空间结构一致 |
C. 的电子式为 的电子式为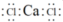 | D. 分子之间的范德华力强于氢键 分子之间的范德华力强于氢键 |
您最近一年使用:0次
2024·江西·模拟预测
名校
6 . 火箭表面耐高温涂层的制备反应为 。阿伏伽德罗常数的值为
。阿伏伽德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 。阿伏伽德罗常数的值为
。阿伏伽德罗常数的值为 ,下列说法正确的是
,下列说法正确的是A. 中共价键的数目为 中共价键的数目为 |
B. 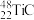 中含有的中子数为 中含有的中子数为 |
C.  固体含有 固体含有 的数目为 的数目为 |
D.消耗 时,该反应中转移的电子数为 时,该反应中转移的电子数为 |
您最近一年使用:0次
2024-01-23更新
|
1104次组卷
|
5卷引用:2024年1月“九省联考”江西卷真题完全解读与考后提升
(已下线)2024年1月“九省联考”江西卷真题完全解读与考后提升(已下线)选择题1-52024年1月江西普通高等学校招生考试适应性测试化学试题(已下线)热点04 有关阿伏加德罗常数的正误判断辽宁省沈阳市东北育才学校高中部2023-2024学年高三下学期第六次模拟考试化学试题
23-24高三上·河南濮阳·期中
名校
解题方法
7 . 钴酸锂( )电池是一种应用广泛的新型电源,放电时的电池反应方程式为
)电池是一种应用广泛的新型电源,放电时的电池反应方程式为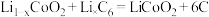 。电池正极材料有
。电池正极材料有 和少量的铝、铁、碳等单质。可利用以下工艺流程回收正极材料中的某些金属资源(还原性:
和少量的铝、铁、碳等单质。可利用以下工艺流程回收正极材料中的某些金属资源(还原性: )。
)。
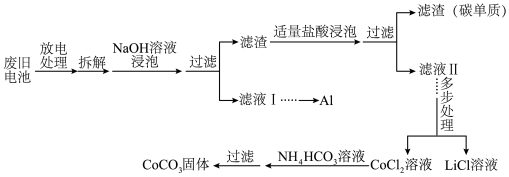
回答下列问题:
(1)基态Co原子的价层电子排布式为___________ 。
(2)“放电处理”时正极的电极反应式为___________ 。
(3)“放电处理”除了考虑“拆解”时的安全因素外,还有利于___________ 。
(4)NaOH溶液浸泡时发生的主要反应的离子方程式为___________ 。
(5)“适量盐酸浸泡”时, 与盐酸反应的化学方程式为
与盐酸反应的化学方程式为___________ 。滤液Ⅱ中的溶质除HCl、LiCl、 外还有
外还有___________ (填化学式)。
(6)加入“ 溶液”发生反应的离子方程式为
溶液”发生反应的离子方程式为___________ 。
 )电池是一种应用广泛的新型电源,放电时的电池反应方程式为
)电池是一种应用广泛的新型电源,放电时的电池反应方程式为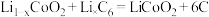 。电池正极材料有
。电池正极材料有 和少量的铝、铁、碳等单质。可利用以下工艺流程回收正极材料中的某些金属资源(还原性:
和少量的铝、铁、碳等单质。可利用以下工艺流程回收正极材料中的某些金属资源(还原性: )。
)。
回答下列问题:
(1)基态Co原子的价层电子排布式为
(2)“放电处理”时正极的电极反应式为
(3)“放电处理”除了考虑“拆解”时的安全因素外,还有利于
(4)NaOH溶液浸泡时发生的主要反应的离子方程式为
(5)“适量盐酸浸泡”时,
 与盐酸反应的化学方程式为
与盐酸反应的化学方程式为 外还有
外还有(6)加入“
 溶液”发生反应的离子方程式为
溶液”发生反应的离子方程式为
您最近一年使用:0次
23-24高三上·江苏扬州·期末
8 . 下列实验目的对应的方案设计、现象和结论都正确的是
| 实验目的 | 方案设计 | 现象和结论 | |
| A | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入2~3mL蒸馏水 | 若无气体生成,则固体粉末为Na2O;若有气体生成,则固体粉末为Na2O2 |
| B | Fe2+是否具有还原性 | 向2mL1.0mol·L−1FeSO4溶液中滴加几滴0.5mol·L−1酸性KMnO4溶液 | 若溶液不变紫红色,则Fe2+具有还原性;若溶液变紫红色,则Fe2+不具有还原性 |
| C | 比较Cl2、Br2、I2的氧化性 | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色,证明氧化性:Cl2>Br2>I2 |
| D | 比较H2CO3与CH3COOH的酸性 | 用pH计测定pH:①NaHCO3溶液②CH3COONa溶液 | pH①>②,证明H2CO3酸性弱于CH3COOH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
23-24高三上·全国·期末
解题方法
9 . 工业合成尿素的反应原理为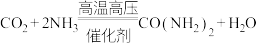 。下列说法正确的是
。下列说法正确的是
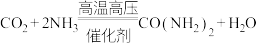 。下列说法正确的是
。下列说法正确的是A.氧原子(8O)基态核外电子排布式为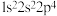 |
B. 的电子式为 的电子式为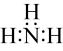 |
C. 中N的化合价为+3 中N的化合价为+3 |
D. 的空间构型为直线形 的空间构型为直线形 |
您最近一年使用:0次
2024-01-16更新
|
879次组卷
|
5卷引用:选择题1-5
(已下线)选择题1-5(已下线)热点02 化学用语 江苏省南京市 盐城市2023-2024学年高三上学期第一次模拟考试化学试题 江苏省南京市、盐城市2023-2024学年高三上学期第一次模拟考试化学试卷(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
23-24高三上·天津·阶段练习
名校
10 . 羰基硫是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。一定条件下, 与CO能反应生成羰基硫:
与CO能反应生成羰基硫:
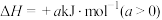 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 与CO能反应生成羰基硫:
与CO能反应生成羰基硫:
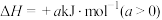 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.1molCO与 充分反应可生成COS分子的数目为 充分反应可生成COS分子的数目为 |
B.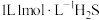 溶液中含有的 溶液中含有的 数目为 数目为 |
C.1molCOS中含有的双键数目为 |
D.每转移 个 个 ,吸收akJ能量 ,吸收akJ能量 |
您最近一年使用:0次



