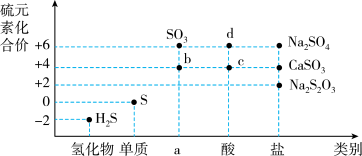
1 . 物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据图正确回答下列含硫物质有关问题。
(1)a对应物质的类别是___________ ;
(2)图中 b、c、d 这三种物质中属于弱电解质的是_______________ (填化学式)。
(3)欲制备Na2S2O3(硫代硫酸钠),根据价类二维图信息分析,合理的是_______。
(4)请结合SO2类别、价态及特性,在如下图实验装置分析SO2的性质(经检验,装置的气密性良好)。
①是检验SO2的___________ 。
②中的现象褪色,体现了SO2的___________ 。
③中产生淡黄色浑浊,体现了SO2的___________ 。
(5)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
产生沉淀的化学式是:①___________ ,②___________ 。
(6)写出SO2与氢氧化钠溶液反应的化学方程式______________ 。
(1)a对应物质的类别是
(2)图中 b、c、d 这三种物质中属于弱电解质的是
(3)欲制备Na2S2O3(硫代硫酸钠),根据价类二维图信息分析,合理的是_______。
| A.Na2S+S | B.Na2SO3+S |
| C.Na2SO3+Na2SO4 | D.SO2+Na2SO4 |
(4)请结合SO2类别、价态及特性,在如下图实验装置分析SO2的性质(经检验,装置的气密性良好)。

①是检验SO2的
②中的现象褪色,体现了SO2的
③中产生淡黄色浑浊,体现了SO2的
(5)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
| 加入的物质 | H2O2 | 氨水 |
| 沉淀的化学式 | ① | ② |
(6)写出SO2与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
解题方法
2 . I、“侯氏制碱法”促进了我国纯碱工业的发展。该法以NaCl、 、
、 等为原料先制得
等为原料先制得 ,进而生产出纯碱,如图是模拟“侯氏制碱法”制取
,进而生产出纯碱,如图是模拟“侯氏制碱法”制取 的部分装置:
的部分装置:
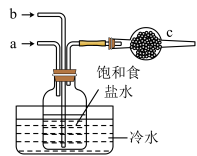
已知: 极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。
极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。
(1)下列操作说法正确的是___________。
II.某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备碳酸钠的实验流程如图:
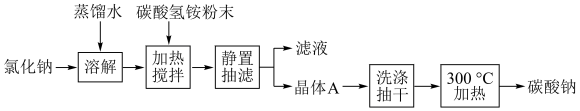
(2)“加热搅拌”中发生反应的化学方程式为___________ ,该反应属于___________ (填基本反应类型);
(3)“300℃加热”需用到的仪器除酒精灯、三角架、泥三角外,还有需要___________ (填主要仪器名称);
(4)若向 中加入过量稀NaOH溶液,所涉及的离子方程式为
中加入过量稀NaOH溶液,所涉及的离子方程式为___________ ;
(5)除去 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是___________ 。
 、
、 等为原料先制得
等为原料先制得 ,进而生产出纯碱,如图是模拟“侯氏制碱法”制取
,进而生产出纯碱,如图是模拟“侯氏制碱法”制取 的部分装置:
的部分装置:
已知:
 极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。
极易溶于水,溶于水时易发生溶液倒吸现象,从而导致安全隐患。(1)下列操作说法正确的是___________。
A.a中先通入 ,然后b通入 ,然后b通入 ,c中放碱石灰 ,c中放碱石灰 |
B.b中先通入 ,然后a通入 ,然后a通入 ,c中放蘸有稀硫酸的脱脂棉 ,c中放蘸有稀硫酸的脱脂棉 |
C.a中先通入 ,然后b通入 ,然后b通入 ,c中放蘸有稀硫酸的脱脂棉 ,c中放蘸有稀硫酸的脱脂棉 |
D.b中先通入 ,然后a通入 ,然后a通入 ,c中放碱石灰 ,c中放碱石灰 |
II.某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备碳酸钠的实验流程如图:

(2)“加热搅拌”中发生反应的化学方程式为
(3)“300℃加热”需用到的仪器除酒精灯、三角架、泥三角外,还有需要
(4)若向
 中加入过量稀NaOH溶液,所涉及的离子方程式为
中加入过量稀NaOH溶液,所涉及的离子方程式为(5)除去
 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是
您最近半年使用:0次
名校
解题方法
3 . 央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知工业明胶含有 会对人体造成伤害,其中铬元素是
会对人体造成伤害,其中铬元素是 价,则其中铁元素是
价,则其中铁元素是_______ 价。 是一种酸根离子,则
是一种酸根离子,则 属于
属于_______ (填“酸”、“碱”、“盐”或“氧化物”)。
(2)明胶的水溶液和 溶液共同具备的性质是
溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置会产生沉淀
b.分散质粒子都可以通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的_______ (填序号)。此方法称为_______ 。
A.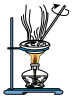 B.
B.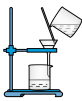 C.
C.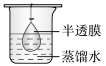
(4)实验室常用向煮沸的蒸馏水中滴加饱和 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的实验操作是
胶体,证明有胶体生成的最常用的实验操作是_______ 。如果向其中滴入过量稀硫酸,出现的现象时是_______ 。
(5)下列关于 胶体的说法正确的是_______。
胶体的说法正确的是_______。
(1)已知工业明胶含有
 会对人体造成伤害,其中铬元素是
会对人体造成伤害,其中铬元素是 价,则其中铁元素是
价,则其中铁元素是 是一种酸根离子,则
是一种酸根离子,则 属于
属于(2)明胶的水溶液和
 溶液共同具备的性质是
溶液共同具备的性质是a.都不稳定,密封放置会产生沉淀
b.分散质粒子都可以通过滤纸
c.二者均有丁达尔效应
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列中的
A.
 B.
B. C.
C.
(4)实验室常用向煮沸的蒸馏水中滴加饱和
 溶液制备
溶液制备 胶体,证明有胶体生成的最常用的实验操作是
胶体,证明有胶体生成的最常用的实验操作是(5)下列关于
 胶体的说法正确的是_______。
胶体的说法正确的是_______。A.利用丁达尔效应分离 胶体和 胶体和 溶液 溶液 |
B. 胶体的胶粒带正电荷,在通电情况下胶粒向直流电源的负极移动,这种现象称为电泳 胶体的胶粒带正电荷,在通电情况下胶粒向直流电源的负极移动,这种现象称为电泳 |
C.向 胶体中加入带相反电性胶粒的胶体会出现沉淀 胶体中加入带相反电性胶粒的胶体会出现沉淀 |
D.向沸腾的 稀溶液中边滴加 稀溶液中边滴加 饱和溶液,边用玻璃棒搅动,然后继续煮沸,也可制备 饱和溶液,边用玻璃棒搅动,然后继续煮沸,也可制备 胶体 胶体 |
您最近半年使用:0次
2023-11-01更新
|
410次组卷
|
2卷引用:陕西省西安高新第一中学2023-2024学年高一上学期第一次月考化学试题
名校
4 . 下列实验操作或事实与预期实验目的或所得结论对应正确的是
| 选项 | 实验操作或事实 | 实验目的或结论 |
| A | 氯气使湿润的淀粉碘化钾试纸变蓝 | 说明氯气具有还原性 |
| B | 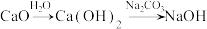 | 用生石灰制备NaOH溶液 |
| C | 用玻璃棒蘸取某无色溶液灼烧后火焰呈黄色 | 无色溶液中含有钠元素 |
| D | 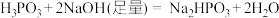 | H3PO3属于三元酸 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
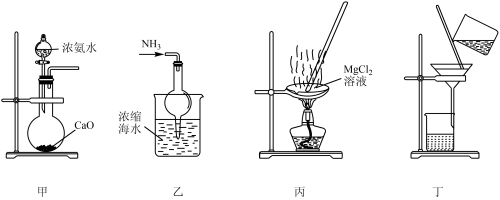
5 . 浓缩海水与氨气反应可得 ,进一步与酸反应可得
,进一步与酸反应可得 ,下列设计的相关实验不能达到实验目的的是
,下列设计的相关实验不能达到实验目的的是
 ,进一步与酸反应可得
,进一步与酸反应可得 ,下列设计的相关实验不能达到实验目的的是
,下列设计的相关实验不能达到实验目的的是
A.用装置甲制取 |
B.用装置乙制得 |
C.用装置丙蒸干溶液获得 |
D.用装置丁从浓缩海水与氨气反应后的混合物中分离出 |
您最近半年使用:0次
2022-04-23更新
|
170次组卷
|
2卷引用:河南省焦作市普通高中2021-2022学年高二下学期期中考试化学试题
名校
6 . 下列实验操作或事实与预期实验目的或所得结论对应正确的是( )
选项 | 实验操作或事实 | 实验目的或结论 |
| A | 淡黄色试液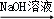 红褐色沉淀 红褐色沉淀 | 说明原溶液中一定含所有FeCl3 |
| B | CaO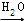 Ca(OH)2 Ca(OH)2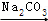 NaOH NaOH | 用生石灰制备NaOH溶液 |
| C | 新收集的酸雨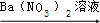 白色沉淀 白色沉淀 | 酸雨中一定含有SO42- |
| D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于三元酸 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2017-07-23更新
|
322次组卷
|
3卷引用:辽宁省瓦房店市高级中学2016-2017学年高二下学期期末考试化学试题
7 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系。
请回答一下问题:
(1) 中
中 的化合价为
的化合价为_______ 。
(2) 是否为碱性氧化物
是否为碱性氧化物_______ (填是或否),理由:_______ 。
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:_______ 。其中检验溶液中 的试剂是
的试剂是_______ 。
(4)电子工业常用 的
的 溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式_______ ;印刷电路板的废液中加入一定量铁粉,充分反应后,准备过滤并收集滤渣。此时,滤渣的成分不可能是_______ 。
aA.没有滤渣 B.有 也有
也有 C.只有
C.只有 D.只有
D.只有

请回答一下问题:
(1)
 中
中 的化合价为
的化合价为(2)
 是否为碱性氧化物
是否为碱性氧化物(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
 的试剂是
的试剂是(4)电子工业常用
 的
的 溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式aA.没有滤渣 B.有
 也有
也有 C.只有
C.只有 D.只有
D.只有
您最近半年使用:0次
名校
8 . 根据已经学过的化学知识,回答下列问题。
I.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)将Cu与稀硫酸混合,二者不能反应,滴入 后,溶液很快变成蓝色,该反应的化学方程式为
后,溶液很快变成蓝色,该反应的化学方程式为___________ 。
(3) 是一种酸式盐,写出
是一种酸式盐,写出 在水中的电离方程式:
在水中的电离方程式:___________ 。
(4)Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
①与酸反应的差异。甲组进行了如下4组实验。

其中实验________ 和________ (填实验序号)可以鉴别 和
和 ,实验现象分别是
,实验现象分别是________ 。
②热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。
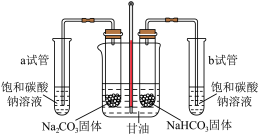
将分别装有 和
和 的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:
的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:___________ ,试管b中发生反应的化学方程式为___________ 。
Ⅱ.物质的量是学习化学的基础。
(5)14.4gCO和 的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为______ 。
(6)19g某二价金属的氯化物 中含有0.4molCl,金属A的相对原子质量是
中含有0.4molCl,金属A的相对原子质量是___________ 。
(7)根据反应 ,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为
,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为___________ mol。
I.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)将Cu与稀硫酸混合,二者不能反应,滴入
 后,溶液很快变成蓝色,该反应的化学方程式为
后,溶液很快变成蓝色,该反应的化学方程式为(3)
 是一种酸式盐,写出
是一种酸式盐,写出 在水中的电离方程式:
在水中的电离方程式:(4)Na2CO3和NaHCO3是厨房中常见的两种盐,可用化学性质的差异进行鉴别。回答下列问题:
①与酸反应的差异。甲组进行了如下4组实验。

其中实验
 和
和 ,实验现象分别是
,实验现象分别是②热稳定性差异。乙组设计如下装置进行实验(加热及夹持装置省略)。

将分别装有
 和
和 的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:
的试管同时放入甘油浴加热(甘油沸点为290℃)。该实验用饱和碳酸钠溶液检验反应的产物,b试管中的实验现象分别为:Ⅱ.物质的量是学习化学的基础。
(5)14.4gCO和
 的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为
的混合气体在标准状况下所占的体积为8.96L,其中CO的质量为(6)19g某二价金属的氯化物
 中含有0.4molCl,金属A的相对原子质量是
中含有0.4molCl,金属A的相对原子质量是(7)根据反应
 ,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为
,可知当有2.5molFeS2参加反应时,被氧化的硫元素的物质的量为
您最近半年使用:0次
9 . 依据与水反应情况对某些物质进行分类,如下图所示。回答下列问题:
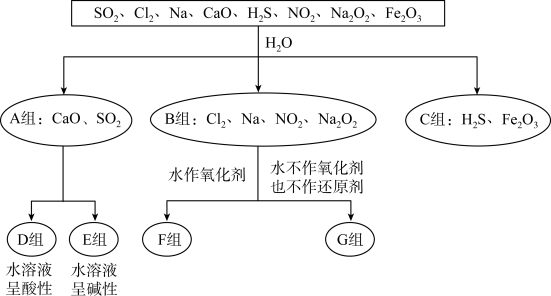
(1)上述物质中属于碱性氧化物的有___________ (填化学式);D组物质属于___________ (填“电解质”或“非电解质”)。
(2) 组物质与水反应的离子方程式为
组物质与水反应的离子方程式为___________ 。
(3)将 通入紫色石蕊溶液中,现象为
通入紫色石蕊溶液中,现象为___________ ;将 通入
通入 溶液中,反应的化学方程式为
溶液中,反应的化学方程式为___________ 。
(4) 和
和 都是常见的消毒剂。工业上可通过反应:
都是常见的消毒剂。工业上可通过反应: 制备
制备 ,其中
,其中 的氧化性比
的氧化性比
___________ (填“强”或“弱”),当消耗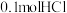 时,转移电子的数目为
时,转移电子的数目为___________ 。

(1)上述物质中属于碱性氧化物的有
(2)
 组物质与水反应的离子方程式为
组物质与水反应的离子方程式为(3)将
 通入紫色石蕊溶液中,现象为
通入紫色石蕊溶液中,现象为 通入
通入 溶液中,反应的化学方程式为
溶液中,反应的化学方程式为(4)
 和
和 都是常见的消毒剂。工业上可通过反应:
都是常见的消毒剂。工业上可通过反应: 制备
制备 ,其中
,其中 的氧化性比
的氧化性比
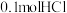 时,转移电子的数目为
时,转移电子的数目为
您最近半年使用:0次
名校
解题方法
10 . Ⅰ.如图为铁及其化合物的“价—类”二维图。

(1)填写二维图中缺失的类别①________ 和化学式②___________ 。
(2)从物质类别上看, 属于盐,可能与
属于盐,可能与_______ 发生反应(填序号);
从化合价角度看,体现 氧化性,可能与
氧化性,可能与______ 反应(填序号)。
① ②KI溶液 ③NaOH溶液 ④
②KI溶液 ③NaOH溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
Ⅱ.某工厂用 溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
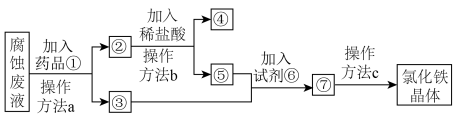
(3)腐蚀废液中加入药品①后,发生反应的离子方程式为___________ 。
(4)④代表的物质是___________ (用化学式表示)。
(5)操作方法a、b、c中是过滤的是________ (填序号)。
(6)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,_________ (补全现象),此过程设计氧化还原反应的方程式为________ 。
(7)工业中常用高铁酸钾( )作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒:
)作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制高铁酸钾的离子反应方程式:
。写出并配平湿法制高铁酸钾的离子反应方程式:___________ 。

(1)填写二维图中缺失的类别①
(2)从物质类别上看,
 属于盐,可能与
属于盐,可能与从化合价角度看,体现
 氧化性,可能与
氧化性,可能与①
 ②KI溶液 ③NaOH溶液 ④
②KI溶液 ③NaOH溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液Ⅱ.某工厂用
 溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
溶液腐蚀镀有铜的绝缘板生产印刷电路,一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。请根据流程,回答下列问题。(提示:为充分除去杂质,所加试剂均为过量)
(3)腐蚀废液中加入药品①后,发生反应的离子方程式为
(4)④代表的物质是
(5)操作方法a、b、c中是过滤的是
(6)若取2 mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(7)工业中常用高铁酸钾(
 )作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒:
)作为高效、多功能的自来水处理剂。湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平湿法制高铁酸钾的离子反应方程式:
。写出并配平湿法制高铁酸钾的离子反应方程式:
您最近半年使用:0次
2024-02-12更新
|
113次组卷
|
2卷引用:天津市第四十二中学2023-2024学年高一上学期第二次月考化学试题



