名校
解题方法
1 . 下列说法不正确的是
| A.把7.2 g纯铁粉加入40 mL浓度未知的HNO3溶液中,充分反应后剩余固体1.6 g,产生NO2和NO的混合气体0.08 mol,若不考虑N2O4的存在,则原HNO3溶液的物质的量浓度为7.0 mol·L-1 |
| B.将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4溶液蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是c2>2c1 |
C.将标准状况下的a L HCl气体溶于1 000 mL水中,得到的盐酸溶液密度为b g·mL-1,则该盐酸溶液的物质的量浓度为 mol·L-1 mol·L-1 |
D.V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中 的物质的量浓度为 的物质的量浓度为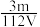 mol·L-1 mol·L-1 |
您最近一年使用:0次
2022-08-05更新
|
636次组卷
|
7卷引用:甘肃省天水市第一中学2021届高三上学期第一次考试化学试题
甘肃省天水市第一中学2021届高三上学期第一次考试化学试题浙江省东阳中学2023届高三浙江省普通高校招生选考科目考试仿真训练化学试题甘肃省天水市第一中学2019-2020学年高二下学期期末考试化学试题(已下线)第一章能力提升检测卷-2022年高考化学一轮复习讲练测(已下线)专题09 物质的量-备战2023年高考化学母题题源解密(广东卷)(已下线)考点07 物质的量浓度(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)新疆和田地区墨玉县2022-2023学年高三上学期11月期中考试化学试题
解题方法
2 . 气体中微量的H2S,对工业生产和环境都有危害。通过以下实验装置利用20%脱硫剂三嗪(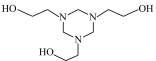 )水溶液除去H2S,并使用2 mol·L-1 CuSO4溶液检验H2S是否除尽。
)水溶液除去H2S,并使用2 mol·L-1 CuSO4溶液检验H2S是否除尽。

回答下列问题:
(1)仪器1的名称是_______ 。装置甲制取CO2,实验室制取CO2的离子方程式为_______ 。
(2)仪器2盛装0.001 mol·L-1H2S水溶液,三颈烧瓶丙中盛装溶液是_______ 。
(3)操作步骤:
①打开开关A、C,放入酸溶液产生CO2,目的是_______ ;
②一段时间后,关小开关C的出气量,打开压缩机开关,同时打开活塞放入H2S水溶液;逐渐减缓仪器1中酸溶液滴入速率并控制气压。使用CO2压缩机的作用是_______ 。
(4)通入二氧化碳所形成的混合气体中,经测量含H2S的量为1000 ×10-6mg·m-3,则该混合气体中c(H2S)计算式为_______ mol·L-1。
(5)三嗪( )水溶液吸收H2S,生成
)水溶液吸收H2S,生成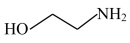 和
和 化学方程式为
化学方程式为_______ 。CuSO4溶液没有出现_______ (填现象), 证明三嗪吸收H2S的化学反应具有_______ 、_______ 等特征,20%三嗪水溶液是很好的脱硫剂。
 )水溶液除去H2S,并使用2 mol·L-1 CuSO4溶液检验H2S是否除尽。
)水溶液除去H2S,并使用2 mol·L-1 CuSO4溶液检验H2S是否除尽。
回答下列问题:
(1)仪器1的名称是
(2)仪器2盛装0.001 mol·L-1H2S水溶液,三颈烧瓶丙中盛装溶液是
(3)操作步骤:
①打开开关A、C,放入酸溶液产生CO2,目的是
②一段时间后,关小开关C的出气量,打开压缩机开关,同时打开活塞放入H2S水溶液;逐渐减缓仪器1中酸溶液滴入速率并控制气压。使用CO2压缩机的作用是
(4)通入二氧化碳所形成的混合气体中,经测量含H2S的量为1000 ×10-6mg·m-3,则该混合气体中c(H2S)计算式为
(5)三嗪(
 )水溶液吸收H2S,生成
)水溶液吸收H2S,生成 和
和 化学方程式为
化学方程式为
您最近一年使用:0次
2022-06-14更新
|
282次组卷
|
2卷引用:江西省抚州市2022届高三下学期4月教学质量监测理综化学试题
名校
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.84g环己烷中含有共价键的数目为12NA |
| B.标准状况下,2.24L氯气参与的氧化还原反应中,转移电子数一定为0.2NA |
| C.11g CO2和N2O的混合物中含有的质子数一定为5.5NA |
| D.1L l mol·L-1CH3COONa溶液中CH3COO-与OH-离子数之和等于NA |
您最近一年使用:0次
2022-06-02更新
|
501次组卷
|
2卷引用:四川省成都市树德中学2022届高三适应性考试化学试题
4 . NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,11.2L  所含的分子数为0.5NA 所含的分子数为0.5NA |
B.0.1mol/L  溶液中,含有的 溶液中,含有的 数目小于0.1NA 数目小于0.1NA |
C.2 mol NO与1 mol  在密闭容器中充分反应后的分子数小于2NA 在密闭容器中充分反应后的分子数小于2NA |
| D.常温下,1 mol Fe与足量的浓硝酸反应转移的电子数为3NA |
您最近一年使用:0次
2022-05-20更新
|
402次组卷
|
5卷引用:重庆市普通高中2022届高三学业水平选择性考试联合诊断化学试题
重庆市普通高中2022届高三学业水平选择性考试联合诊断化学试题(已下线)专题02 化学计量与化学计算-三年(2020-2022)高考真题分项汇编(已下线)专题02 化学计量与化学计算-2022年高考真题模拟题分项汇编(已下线)云南省昆明市官渡区第二中学2023-2024学年高二上学期开学考试化学试题云南省昆明市官渡区第二中学2023-2024学年高三上学期开学考试化学试题
5 . 若NA代表阿伏加德罗常数的值,下列说法正确的是
| A.常温下,18gH2O所含的质子数为18NA |
| B.在标准状况下,5.6LCH4和11.2LCl2在光照下充分反应后的分子数为0.75NA |
| C.1L0.1mol·L-1乙二酸溶液中含H+的数目为0.2NA |
| D.用惰性电极电解饱和食盐水,电子转移的数目为NA时,生成的OH-浓度为1mol·L-1 |
您最近一年使用:0次
6 . 利用压强传感器测定氨气的喷泉实验中的压强变化。下列说法错误的是
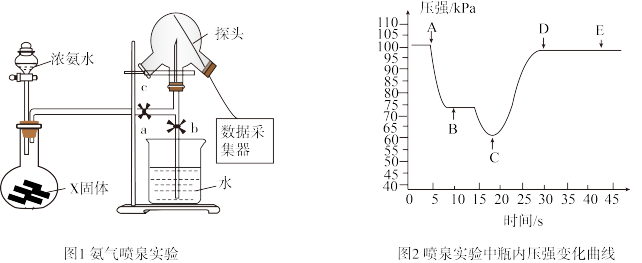

| A.烧瓶中制取氨气时常用的固体为CaO或NaOH |
| B.可用湿润的红色石蕊试纸置于三颈瓶口c处验满 |
| C.关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,A点时喷泉最剧烈 |
D.常温下完成该实验,假设溶液刚好充满烧瓶且混合均匀,则溶液的物质的量浓度大于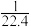 mol/L mol/L |
您最近一年使用:0次
2022-05-16更新
|
326次组卷
|
5卷引用:湖南省株洲市第一中学2021届高三第一次模拟检测化学试题
解题方法
7 . 酒驾检验原理:2K2Cr2O7+3CH3CH2OH+8H2SO4=3CH3COOH+2Cr2(SO4)3+11H2O+2K2SO4。设NA为阿伏加德罗常数的值,下列说法正确的是
| A.lmol[2K2Cr2O7+3CH3CH2OH]完全反应转移电子数为6NA |
B.25℃时,1LpH=1的H2SO4溶液中含SO 数目为0.1NA 数目为0.1NA |
| C.等物质的量的CH3CH2OH和CH3COOH充分反应生成的H2O中含氢键数为2NA |
| D.1molCH3COOH中含sp2—sp3σ键的数目为2NA |
您最近一年使用:0次
8 . 为了探究市售Fe3O4能否与常见的酸(盐酸、稀硫酸)发生反应,实验小组做了以下工作。
Ⅰ.Fe3O4的制备
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可制行Fe3O4,反应的离子方程式为_______ 。
Ⅱ.Fe3O4与酸反应的热力学论证
(2)理论上完全溶解1.16gFe3O4至少需要3 mol/LH2SO4溶液的体积约为_______ mL(保留1位小数)。
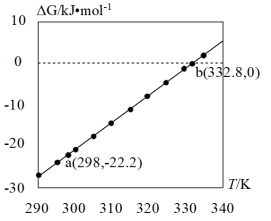
(3)查阅文献:吉布斯自由能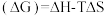 ,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是_______ 。
Ⅲ.Fe3O4与酸反应的实验研究
用10 mL3 mol/LH2SO4溶液浸泡1.0 g Fe3O4粉末,5分钟后各取2 mL澄清浸泡液,按编号i进行实验。(所用 、KSCN溶液均为0.1 mol/L,Fe2+遇
、KSCN溶液均为0.1 mol/L,Fe2+遇 溶液生成蓝色沉淀。)
溶液生成蓝色沉淀。)
(4)实验ⅱ的作用是_______ 。
(5)实验ⅰ中滴加K3[Fe(CN)6]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为了验证这一推断,可改进的方法是_______ 。
(6)实验ⅲ:用10 mL6 mol/L盐酸代替H2SO4浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe3O4与H+反应,为了验证这一推测,可在用H2SO4溶液浸泡时加入_______ ,然后重复实验i。
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是_______ 。
Ⅰ.Fe3O4的制备
(1)将可溶性亚铁盐和铁盐按一定配比混合后,加入NaOH溶液,在一定条件下反应可制行Fe3O4,反应的离子方程式为
Ⅱ.Fe3O4与酸反应的热力学论证
(2)理论上完全溶解1.16gFe3O4至少需要3 mol/LH2SO4溶液的体积约为
(3)查阅文献:吉布斯自由能
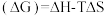 ,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
,在100 kPa下,Fe3O4与酸反应的△G与温度T的关系如图所示。Fe3O4与酸自发反应的温度条件是
Ⅲ.Fe3O4与酸反应的实验研究
用10 mL3 mol/LH2SO4溶液浸泡1.0 g Fe3O4粉末,5分钟后各取2 mL澄清浸泡液,按编号i进行实验。(所用
 、KSCN溶液均为0.1 mol/L,Fe2+遇
、KSCN溶液均为0.1 mol/L,Fe2+遇 溶液生成蓝色沉淀。)
溶液生成蓝色沉淀。)| 编号 | i | ii |
| 实验操作 | 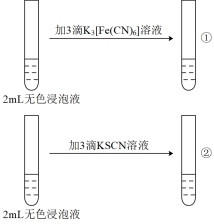 | 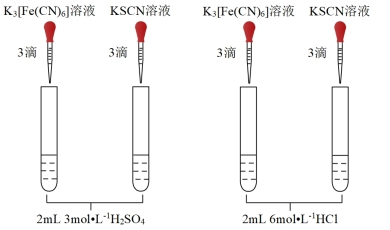 |
| 现象 | ①无蓝色沉淀 ②溶液显红色 | 均无明显现象 |
(5)实验ⅰ中滴加K3[Fe(CN)6]溶液无蓝色沉淀生成,其可能原因是Fe2+的浓度太小,为了验证这一推断,可改进的方法是
(6)实验ⅲ:用10 mL6 mol/L盐酸代替H2SO4浸泡样品后,重复实验ⅰ,发现试管①有蓝色沉淀,试管②溶液显红色,说明Cl-有利于Fe3O4与H+反应,为了验证这一推测,可在用H2SO4溶液浸泡时加入
(7)实验ⅳ:用20 mL6 mol/L盐酸浸泡1.0 g天然磁铁矿粉末,20 min后浸泡液几乎无色,重复实验i,发现试管①、②均无明显现象,与实验iii现象不同的可能原因是
您最近一年使用:0次
2022-05-05更新
|
540次组卷
|
3卷引用:福建省三明市2022届普通高中毕业班下学期5月质量测试化学试题
福建省三明市2022届普通高中毕业班下学期5月质量测试化学试题(已下线)专题17 化学实验综合题-三年(2020-2022)高考真题分项汇编福建省泉州第一中学2023-2024学年高三上学期12月月考化学试题
名校
9 . NA为阿伏加德罗常数的值。下列叙述正确的是
| A.1molOH-中含有9NA个电子 |
| B.1molCl2与NaOH完全反应,转移2NA个电子 |
| C.14gC2H4与C3H6混合物中含有2NA个氢原子 |
| D.10mL0.1mol·L-1NaAlO2溶液中含有2×10-3NA个氧原子 |
您最近一年使用:0次
2022-05-03更新
|
480次组卷
|
3卷引用:河南省许昌济源平顶山2022届高三下学期第三次质量检测理科综合化学试题
河南省许昌济源平顶山2022届高三下学期第三次质量检测理科综合化学试题(已下线)第06练 物质的量-2023年高考化学一轮复习小题多维练(全国通用)湖南省株洲市攸攸县第二中学2022-2023学年高三上学期第五次月考化学试题
解题方法
10 . 单质硫在热的NaOH溶液中发生如下反应:3S+6NaOH 2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S
2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S Na2Sx,S+Na2SO3
Na2Sx,S+Na2SO3 Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO
Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
。
请计算:
(1)a mol Na2Sx和b mol Na2S2O3中a∶b=____ 。
(2)NaClO溶液的物质的量浓度为____ mol·L-1 (写出计算过程)。
 2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S
2Na2S+Na2SO3+3H2O。若硫过量,会进一步生成Na2Sx和Na2S2O3:(x-1)S+Na2S Na2Sx,S+Na2SO3
Na2Sx,S+Na2SO3 Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO
Na2S2O3。现有3.84 g硫与含0.06 mol NaOH的热溶液完全反应,生成a mol Na2Sx和b mol Na2S2O3,在混合溶液中加入NaClO碱性溶液300 mL,恰好将硫元素全部转化为SO 。
。请计算:
(1)a mol Na2Sx和b mol Na2S2O3中a∶b=
(2)NaClO溶液的物质的量浓度为
您最近一年使用:0次
2022-04-16更新
|
420次组卷
|
2卷引用:浙江省宁波市2022届高三下学期高考模拟考试(二模)化学试题



