1 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.100g46%的乙醇溶液中含有O-H键的数目为 |
B.标准状况下,11.2LHF中电子的数目为 |
C.pH=1的 溶液中 溶液中 的数目为 的数目为 |
D.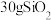 中含有的Si-O键数目为 中含有的Si-O键数目为 |
您最近一年使用:0次
名校
解题方法
2 . 相对分子质量为Mr的气态化合物V L(标准状况)溶于m g水中,得到溶液的质量分数为w%,物质的量浓度为c mol·L-1,密度为ρ g·cm-3,则下列说法正确的是
A.溶液密度ρ可表示为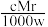 | B.物质的量浓度c可表示为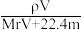 |
C.溶液的质量分数w%可表示为 | D.相对分子质量Mr可表示为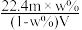 |
您最近一年使用:0次
2023-10-29更新
|
1095次组卷
|
42卷引用:山西省晋城市第一中学校2023-2024学年高三上学期第四次调研化学试题
山西省晋城市第一中学校2023-2024学年高三上学期第四次调研化学试题湖北省部分重点中学2022-2023年高一上学期期末联合考试化学试题(已下线)第12讲 物质的量浓度的相关计算-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)(已下线)第2讲 物质的浓度及溶液配制黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题黑龙江省哈尔滨师范大学附属中学2024届高三上学期开学考试化学试题湖南省部分学校2023-2024学年高三上学期第二次联考化学试题辽宁省东北育才学校科学高中部2023-2024学年高一上学期第一次月考化学试题山东省新泰市第一中学(实验部)2023-2024学年高一上学期第二次月考化学试题黑龙江省实验中学2023-2024学年高一上学期第二次阶段测试化学试题天津市第一中学2023-2024学年高一上学期月考(第三章单元测验1)化学试题广东省广州市黄广中学2023-2024学年高一上学期化学竞赛选拔考试2015-2016学年黑龙江铁人中学高一上第一阶段测化学卷(已下线)2018年9月16日《每日一题》人教必修1- 每周一测湖南省长沙市周南梅溪湖中学2018-2019学年高一下学期一模检测化学试题【全国百强校】四川省成都市石室中学2018-2019学年高一上学期10月月考化学试题广东省揭阳市惠来县第一中学2018-2019学年高一上学期期中考试化学试题辽宁省抚顺市第一中学2020届高三上学期期中考试化学试题人教版高一化学必修1第一章—第三章综合测试题江西省南昌市新建区第一中学2019—2020学年高一上学期第一次月考化学试题鲁科版高中化学必修1第一章《认识化学科学》测试卷云南省丽江市华坪县第一中学2019—2020学年高一上学期期末考试化学试题云南省昭通市绥江县二中2019-2020学年高一上学期期末考试化学试题河北省沧州市第一中学2019-2020学年高二4月月考化学试题(已下线)【南昌新东方】2019 雷氏学校 高一上第一次月考(已下线)考点02 物质的量与阿伏加德罗常数-2020年高考化学命题预测与模拟试题分类精编江西省南昌市八一中学2019-2020学年高一下学期开学考试(5月)化学试题宁夏贺兰县景博中学2019-2020学年高一上学期第一次月考化学试题浙江省诸暨中学2019-2020学年高二下学期期中考试化学试题(已下线)【南昌新东方】4.进贤一中 田荣达江西省南昌新建一中2020-2021学年高一上学期第一次月考化学试题黑龙江省齐齐哈尔市讷河市拉哈一中2020-2021学年高一上学期12月月考化学试题江西省南昌市进贤县第一中学2020-2021学年高一上学期第一次月考化学试题(已下线)课时12 物质的量浓度与溶液的配制-2022年高考化学一轮复习小题多维练(全国通用)河南省郑州市第一中学2020-2021学年高一上学期第一次月考化学试题陕西省周至县第四中学2021-2022学年高三上学期10月月考化学试题(已下线)考点02 化学用语和常用化学计量-备战2022年高考化学学霸纠错(全国通用)陕西省西安市第一中学2021-2022学年高一上学期10月月考化学试题湖北省荆州中学2021-2022学年高一上学期期末考试化学试题黑龙江省哈尔滨市第九中学校2022-2023学年高一上学期11月月考化学试题内蒙古鄂尔多斯市第一中学2022-2023 学年高一上学期期末考试化学试题河北省石家庄二中实验学校2023-2024学年高一上学期12月月考化学试题
名校
3 . 用 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.常温下,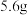 铁与足量浓硫酸充分反应转移的电子数为 铁与足量浓硫酸充分反应转移的电子数为 |
B.标准状态下,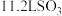 分子中所含的 分子中所含的 原子数为 原子数为 |
C.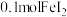 与 与 反应时,转移电子的数目为 反应时,转移电子的数目为 |
D.浓度均为 的 的 溶液和 溶液和 溶液中, 溶液中, 数目均为 数目均为 |
您最近一年使用:0次
2023-10-09更新
|
290次组卷
|
2卷引用:陕西省渭南市大荔县2023-2024学年高三一模考试化学试题
4 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,2.24LSO3中电子的数目为4NA |
B.NaHCO3溶液中Na+和HCO 个数比为1∶1 个数比为1∶1 |
| C.28gC2H4和C3H6的混合气体中含有的C原子数为2NA |
| D.pH=2的H2SO4溶液中H+数目为0.01NA |
您最近一年使用:0次
名校
解题方法
5 . 化学计量在生产和科研中应用广泛。回答下列问题:
(1) 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为___________ ,其质子的物质的量为___________ 。
(2)某气态氧化物的化学式为 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(3)若 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为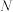 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为___________ (用含字母的代数式表示)。
(4)标准状况下将a LX气体(摩尔质量为 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为___________ 。
(5)将 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为___________ (忽略混合前后溶液体积的变化)。
(6)某混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
___________ 。
(1)
 个
个 分子在标准状况下的体积为
分子在标准状况下的体积为(2)某气态氧化物的化学式为
 ,标准状况下
,标准状况下 该氧化物的体积为
该氧化物的体积为 ,则
,则 的摩尔质量为
的摩尔质量为(3)若
 g某气体A2,含有的分子数为
g某气体A2,含有的分子数为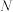 ,
, 气体在标准状况下的体积约为
气体在标准状况下的体积约为 ,则阿伏加德罗常数的数值可表示为
,则阿伏加德罗常数的数值可表示为(4)标准状况下将a LX气体(摩尔质量为
 )全部溶于0.1 L水(水的密度为
)全部溶于0.1 L水(水的密度为 )中(假设气体与水不反应),所得溶液的密度为
)中(假设气体与水不反应),所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为(5)将
 溶液与
溶液与 溶液相混合,则混合溶液中
溶液相混合,则混合溶液中 的物质的量浓度为
的物质的量浓度为(6)某混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则该混合溶液中
,则该混合溶液中
您最近一年使用:0次
2023-09-21更新
|
227次组卷
|
2卷引用:河南省部分名校2023-2024学年高三上学期核心模拟考试(一)化学试题
6 . 高铁酸钾 是新型多功能水处理剂,其生产工艺如图所示:
是新型多功能水处理剂,其生产工艺如图所示:
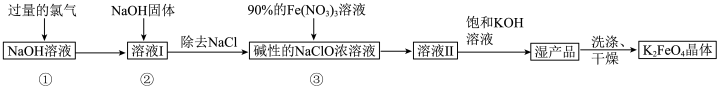
已知:① 与
与 溶液反应的产物与反应温度有关,温度较低时产物为
溶液反应的产物与反应温度有关,温度较低时产物为 和
和 ;温度较高时产物为
;温度较高时产物为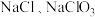 和
和 。
。
②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出 与
与 溶液在较高温度下反应的离子方程式:
溶液在较高温度下反应的离子方程式:___________ 。
(2)向“溶液Ⅰ”中加入 固体起到的作用有降低
固体起到的作用有降低 的溶解度、
的溶解度、___________ 、___________ ;
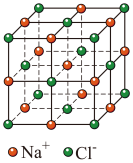
(3) 晶胞结构如图,设晶胞边长为apm,NA为阿伏加德罗常数的值,则距离最近的
晶胞结构如图,设晶胞边长为apm,NA为阿伏加德罗常数的值,则距离最近的 间的距离为
间的距离为___________  ,该晶体的密度为
,该晶体的密度为___________  。(列出计算式)
。(列出计算式)
(4)配制 溶液时,将
溶液时,将 固体溶解在
固体溶解在 水中(水的密度近似为
水中(水的密度近似为 ),所得溶液的密度为
),所得溶液的密度为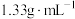 ,则该溶液的物质的量浓度为
,则该溶液的物质的量浓度为___________  。(保留3位有效数字)
。(保留3位有效数字)
(5)步骤③发生的反应中氧化剂与还原剂的物质的量之比n(氧化剂)∶n(还原剂)
___________ 。对“湿产品”进行“洗涤、干燥”时,洗涤剂最好选用___________ (填标号)溶液和异丙醇。
A. B.
B. C.
C.
 是新型多功能水处理剂,其生产工艺如图所示:
是新型多功能水处理剂,其生产工艺如图所示:
已知:①
 与
与 溶液反应的产物与反应温度有关,温度较低时产物为
溶液反应的产物与反应温度有关,温度较低时产物为 和
和 ;温度较高时产物为
;温度较高时产物为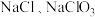 和
和 。
。②同一条件下,溶液的碱性越强,高铁酸盐的稳定性越高。
回答下列问题:
(1)写出
 与
与 溶液在较高温度下反应的离子方程式:
溶液在较高温度下反应的离子方程式:(2)向“溶液Ⅰ”中加入
 固体起到的作用有降低
固体起到的作用有降低 的溶解度、
的溶解度、(3)
 晶胞结构如图,设晶胞边长为apm,NA为阿伏加德罗常数的值,则距离最近的
晶胞结构如图,设晶胞边长为apm,NA为阿伏加德罗常数的值,则距离最近的 间的距离为
间的距离为 ,该晶体的密度为
,该晶体的密度为 。(列出计算式)
。(列出计算式)
(4)配制
 溶液时,将
溶液时,将 固体溶解在
固体溶解在 水中(水的密度近似为
水中(水的密度近似为 ),所得溶液的密度为
),所得溶液的密度为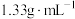 ,则该溶液的物质的量浓度为
,则该溶液的物质的量浓度为 。(保留3位有效数字)
。(保留3位有效数字)(5)步骤③发生的反应中氧化剂与还原剂的物质的量之比n(氧化剂)∶n(还原剂)

A.
 B.
B. C.
C.
您最近一年使用:0次
2023-09-09更新
|
282次组卷
|
2卷引用:黑龙江省大庆市2023-2024学年高三上学期第一次教学质量检测化学试题
名校
解题方法
7 . 有BaCl2和NaCl的混合溶液aL,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀,消耗xmolH2SO4;另一份滴加AgNO3溶液,使Cl-离子完全沉淀,消耗ymolAgNO3.则原混合溶液中的c(Na+)
A.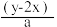 mol·L-1 mol·L-1 | B.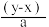 mol·L-1 mol·L-1 |
C.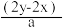 mol·L-1 mol·L-1 | D.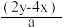 mol·L-1 mol·L-1 |
您最近一年使用:0次
名校
8 . 下列配制溶液的说法正确的有:①1L水中溶解了5.85gNaCl,所得溶液的物质的量浓度为0.1mol/L;②31gNa2O溶于水得到1L溶液,所得溶液的物质的量浓度为0.5mol/L;③标准状况下,22.4LHCl溶于水配成1L溶液,所得盐酸的物质的量浓度为1mol/L;④从1L0.1mol/LHNO3溶液中取出250mL,剩余溶液中 的浓度为0.075mol/L;⑤将25gCuSO4·5H2O晶体溶于75g水中所得溶质的质量分数为16%;⑥将一定量18.4mol/L的硫酸与水等质量混合,所得溶液的浓度大于9.2mol/L
的浓度为0.075mol/L;⑤将25gCuSO4·5H2O晶体溶于75g水中所得溶质的质量分数为16%;⑥将一定量18.4mol/L的硫酸与水等质量混合,所得溶液的浓度大于9.2mol/L
 的浓度为0.075mol/L;⑤将25gCuSO4·5H2O晶体溶于75g水中所得溶质的质量分数为16%;⑥将一定量18.4mol/L的硫酸与水等质量混合,所得溶液的浓度大于9.2mol/L
的浓度为0.075mol/L;⑤将25gCuSO4·5H2O晶体溶于75g水中所得溶质的质量分数为16%;⑥将一定量18.4mol/L的硫酸与水等质量混合,所得溶液的浓度大于9.2mol/L| A.①③ | B.④⑥ | C.③⑤ | D.⑤⑥ |
您最近一年使用:0次
名校
9 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.0.1mol⋅L  溶液中含 溶液中含 的数目为 的数目为 |
B.100g质量分数为46%的乙醇水溶液中含醇羟基的数目为 |
C.18.9g某三肽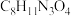 中的肽键数目为 中的肽键数目为 |
D.3.2g 和 和 的混合气体中含氧原子数目为 的混合气体中含氧原子数目为 |
您最近一年使用:0次
10 . 钪的特殊性质,使其在电子工业、航天、核技术、激光技术、冶金、化工、医学、农业等各方面得到广泛应用。一种利用高温沸腾氯化烟尘(主要成分为AlCl3、FeCl3、TiCl4、ScCl3等,还含有其他难溶于酸的物质)回收Sc的工艺流程如图。

已知:钪(原子序数为21)与铝类似,其氢氧化物具有两性;钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。
请回答以下问题:
(1)某次实验中需要使用480mL3mol·L-1的盐酸,用浓盐酸(密度为1.2g·cm-3,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为_______ mL,需要使用的玻璃仪器除烧杯、量筒、玻璃棒外,还需要的是_______ 。
(2)钪的一种核素可用作示踪原子,用于对恶性肿瘤放射治疗,该种核素的中子数为25,则该核素的符号为_______ 。
(3)“反萃取”时,若加入的氢氧化钠溶液过量,则Sc(OH)3沉淀会溶解。写出Se(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式:_______ 。
(4)加入草酸进行“沉淀转化”,将Sc(OH)3沉淀转化为Sc2(C2O4)3。25°C时pH=2的草酸溶液中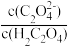 =
=_______ 。(25°C时,草酸的电离平衡常数为Ka1=5.0×10-2,Ka2=5.4×10-5)
(5)草酸钪在空气中“灼烧”可制得Sc2O3,写出反应的化学方程式:_______ 。
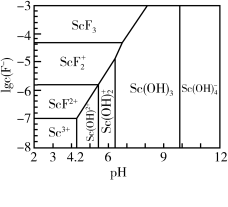
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。若溶液中c(F-)=1×10-5mol·L-1,“调pH”过程中控制pH=5,此时三价Sc的主要存在形式为_______ (填化学式)。

已知:钪(原子序数为21)与铝类似,其氢氧化物具有两性;钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。
请回答以下问题:
(1)某次实验中需要使用480mL3mol·L-1的盐酸,用浓盐酸(密度为1.2g·cm-3,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为
(2)钪的一种核素可用作示踪原子,用于对恶性肿瘤放射治疗,该种核素的中子数为25,则该核素的符号为
(3)“反萃取”时,若加入的氢氧化钠溶液过量,则Sc(OH)3沉淀会溶解。写出Se(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式:
(4)加入草酸进行“沉淀转化”,将Sc(OH)3沉淀转化为Sc2(C2O4)3。25°C时pH=2的草酸溶液中
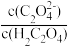 =
=(5)草酸钪在空气中“灼烧”可制得Sc2O3,写出反应的化学方程式:
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。若溶液中c(F-)=1×10-5mol·L-1,“调pH”过程中控制pH=5,此时三价Sc的主要存在形式为

您最近一年使用:0次



