名校
1 . 设 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是
 为阿伏加德罗常数的值。下列叙述错误的是
为阿伏加德罗常数的值。下列叙述错误的是A.1L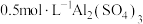 溶液中 溶液中 数目小于 数目小于 |
B.氢氧燃料电池中有1mol气体发生还原反应时转移的电子数为 |
C.298K下,1L 硫酸溶液中 硫酸溶液中 数为 数为 |
D.2.0g重水与足量钠反应产生的气体含中子数为 |
您最近一年使用:0次
2024-03-01更新
|
654次组卷
|
3卷引用:题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)
(已下线)题型3 有关NA的综合考查(25题)-2024年高考化学常考点必杀300题(新高考通用)四川省雅安市雅安中学等校联考2023-2024学年高三下学期开学考试理综试题-高中化学2024届四川省部分学校高三一模联考理科综合试题-高中化学
2024高三下·全国·专题练习
2 . 乙酰水杨酸(阿司匹林)是目前常用药物之一,实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
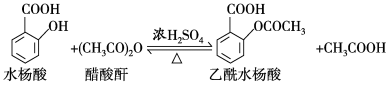
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作:
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
(2)①中需使用冷水,目的是___________ 。
(3)②中饱和碳酸氢钠的作用是___________ ,以便过滤除去难溶杂质。
(4)④采用的纯化方法为___________ 。
(5)本实验的产率是___________ %。

| 水杨酸 | 醋酸酐 | 乙酰水杨酸 | |
| 熔点/℃ | 157~159 | -72~-74 | 135~138 |
| 相对密度/(g·cm-3) | 1.44 | 1.10 | 1.35 |
| 相对分子质量 | 138 | 102 | 180 |
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤;
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
| A.热水浴 | B.酒精灯 | C.煤气灯 | D.电炉 |
(3)②中饱和碳酸氢钠的作用是
(4)④采用的纯化方法为
(5)本实验的产率是
您最近一年使用:0次
3 . 我国科学家李亚栋、钱逸泰等利用以下反应原理合成了金刚石,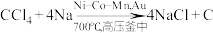 (金刚石)。
(金刚石)。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
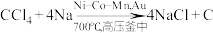 (金刚石)。
(金刚石)。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.12g金刚石中含有的C-C键的数目为 |
B.标准状况下,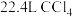 含有 含有 键数目为 键数目为 |
C. 溶液中 溶液中 和 和 数目之和为 数目之和为 |
D.每消耗46g的钠单质,转移的电子数目为 |
您最近一年使用:0次
4 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下, 含 含 分子数为 分子数为 |
B.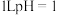 的硫酸溶液含氢离子数为 的硫酸溶液含氢离子数为 |
C.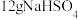 晶体含阴离子数为 晶体含阴离子数为 |
D.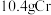 含未成对电子数为 含未成对电子数为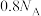 |
您最近一年使用:0次
2024-02-02更新
|
309次组卷
|
4卷引用:选择题11-16
2024高三·全国·专题练习
5 . 某铝土矿的主要成分为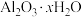 ,还含有
,还含有 和
和 杂质。称取
杂质。称取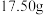 铝土矿样品,加入
铝土矿样品,加入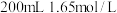 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
(1)该试样中 的物质的量为
的物质的量为___________ mol。
(2)样品中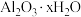 的x=
的x=___________ 。
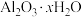 ,还含有
,还含有 和
和 杂质。称取
杂质。称取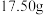 铝土矿样品,加入
铝土矿样品,加入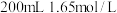 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。(1)该试样中
 的物质的量为
的物质的量为(2)样品中
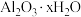 的x=
的x=
您最近一年使用:0次
6 .  为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是A.常温常压下, 金刚石含有4NA个共价键 金刚石含有4NA个共价键 |
B. 的乙酸和盐酸混合溶液含0.1NA个 的乙酸和盐酸混合溶液含0.1NA个 |
C.标准状态下,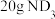 含有的质子数为10NA 含有的质子数为10NA |
D.电解水生成 氢气,外电路通过1NA个电子 氢气,外电路通过1NA个电子 |
您最近一年使用:0次
2024高三·全国·专题练习
7 . 用 代表阿伏加德罗常数的值。下列说法不正确的是
代表阿伏加德罗常数的值。下列说法不正确的是_______ 。
A.(2023·海南卷)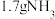 完全溶于
完全溶于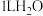 所得溶液,
所得溶液, 微粒数目为
微粒数目为
B.(2023·浙江卷)向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
C.(2023·浙江卷)标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA
D.(2023·广东卷)体积为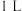 的
的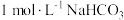 溶液中,
溶液中, 数目为
数目为
E.(2021·天津卷)1mol/LHCl溶液中,HCl分子的数目为NA
F.(2021·浙江卷) 的
的 水溶液中含有氧原子数为
水溶液中含有氧原子数为
 代表阿伏加德罗常数的值。下列说法不正确的是
代表阿伏加德罗常数的值。下列说法不正确的是A.(2023·海南卷)
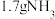 完全溶于
完全溶于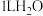 所得溶液,
所得溶液, 微粒数目为
微粒数目为
B.(2023·浙江卷)向1L0.1mol/LCH3COOH溶液通氨气至中性,铵根离子数为0.1NA
C.(2023·浙江卷)标准状况下,11.2LCl2通入水中,溶液中氯离子数为0.5NA
D.(2023·广东卷)体积为
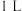 的
的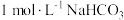 溶液中,
溶液中, 数目为
数目为
E.(2021·天津卷)1mol/LHCl溶液中,HCl分子的数目为NA
F.(2021·浙江卷)
 的
的 水溶液中含有氧原子数为
水溶液中含有氧原子数为
您最近一年使用:0次
2024高三·全国·专题练习
8 . NA为阿伏加德罗常数的值。下列说法正确的是_______ 。
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g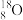 中含有的中子数为NA
中含有的中子数为NA
D.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
A.(2023·全国卷)标准状况下,2.24LSO3中电子的数目为4.00NA
B.(2023·广东卷)NaCl和NH4Cl的混合物中含1molCl-,则混合物中质子数为28NA
C.(2022·辽宁卷)1.8g
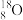 中含有的中子数为NA
中含有的中子数为NAD.(2022·浙江6月)8g CH4含有中子数为3NA
E.(2022·海南卷)2.8g56Fe含有的中子数为1.3NA
F.(2021·天津卷)180g葡萄糖中,C原子的数目为6NA
G.(2021·广东卷)23gNa与足量H2O反应生成的H2分子数目为NA
H.(2021·河北卷)22.4L(标准状况)氟气所含的质子数为18NA
I.(2021·湖北卷)23gCH3CH2OH中sp3杂化的原子数为NA
J.(2021·湖北卷)0.5molXeF4中氙的价层电子对数为3NA
K.(2021·湖南卷)18gH218O含有的中子数为10NA
L.(2021·海南卷)0.1mol 27Al3+中含有的电子数为1.3NA
M.(2021·海南卷)0.1mol肼(H2N-NH2)含有的孤电子对数为0.2NA
N.(2021·全国甲卷)18g重水(D2O)中含有的质子数为10NA
您最近一年使用:0次
名校
解题方法
9 . 乙酰苯胺俗称退热冰,是常用的化工原料和重要的化学试剂。某实验小组拟用一定量的乙酸和苯胺制备一定量的乙酰苯胺,具体实验步骤如下:
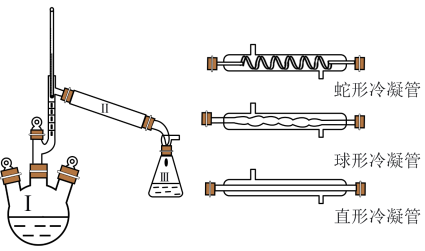
步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
回答下列问题
(1)Ⅱ处空白位置应选择的仪器为___________ (填“蛇形冷凝管”“球形冷凝管”或“直形冷凝管”);反应开始后发现忘加沸石,正确的操作为___________ 。
(2)步骤1中,发生反应的化学方程式是___________ ;温度计控温在105℃的原因是___________ 。
(3)步骤2中,用冷水进行洗涤的原因是___________ 。
(4)步骤3中,趁热抽滤的目的是___________ 。
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为___________ (结果保留2位有效数字)。

步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g/mL) | 溶解性 | |
| 乙酸 | 60 | 16.6 | 117.9 | 1.05 | 能溶于水、乙醇、乙醚 |
| 苯胺 | 93 | -6 | 184 | 1.022 | 微溶于水,易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 114 | 304 | 1.12 | 微溶于冷水,能溶于热水 |
(1)Ⅱ处空白位置应选择的仪器为
(2)步骤1中,发生反应的化学方程式是
(3)步骤2中,用冷水进行洗涤的原因是
(4)步骤3中,趁热抽滤的目的是
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为
您最近一年使用:0次
10 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下, 中含有的氯原子数为 中含有的氯原子数为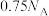 |
B.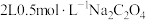 溶液中的 溶液中的 数目为 数目为 |
C.密闭容器中, 和 和 在催化剂作用下充分反应后分子总数为 在催化剂作用下充分反应后分子总数为 |
D.1molNa与足量 反应生成 反应生成 和 和 的混合物,转移的电子数为 的混合物,转移的电子数为 |
您最近一年使用:0次
2023-12-21更新
|
941次组卷
|
6卷引用:热点04 有关阿伏加德罗常数的正误判断
(已下线)热点04 有关阿伏加德罗常数的正误判断2024届四川省内江市高中高三上学期第一次模拟考试(一模)理综试题浙江省宁波市2023-2024学年高二上学期九校联考化学试题(已下线)专题01 基本概念-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)江西省宜春市丰城市东煌学校2023-2024学年高二上学期1月期末化学试题江西省宜春市丰城市东煌学校2023-2024学年高二上学期12月月考化学试题



