1 . 化学与人类生产、生活密切相关,利用所学知识进行填空(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)下列物质能导电且属于电解质的是___________(填字母)。
(2)NaH可在野外作生氢剂,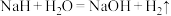 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为___________ 。
(3)标准状况下,44.8L 对应的物质的量是
对应的物质的量是___________ ,其含有的共价键类型为___________ 键。(填极性或者非极性)
(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是___________ (填化学式)
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为_______ 。
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(1)下列物质能导电且属于电解质的是___________(填字母)。
| A.氯化钠固体 | B.熔融的氯化钠 | C.氯化钠溶液 | D.钠 |
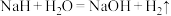 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)标准状况下,44.8L
 对应的物质的量是
对应的物质的量是(4)工业上以氯气和石灰乳为原料制造漂白粉,漂白粉的有效成分是
(5)将4gNaOH溶于水配成1L溶液,然后取出10mL,这10mL溶液的物质的量浓度为
您最近一年使用:0次
名校
2 . 某化学小组在实验室用63%的浓HNO3(其密度为1.39g/cm3,已知1/cm3=1mL)配制480mL0.50mol/L稀HNO3,并探究稀HNO3与物质的反应,①石灰石②氧化铜③二氧化硫④NaOH溶液⑤铁丝⑥碳酸钠⑦氯化银。回答下列问题:
(1)该浓硝酸的物质的量浓度为_____ mol•L-1,应量取浓硝酸的体积为_____ mL(保留三位有效数字)
(2)物质①~⑦中,常温下可导电的物质为_____ (填序号,下同),属于非电解质的为_____ 。
(3)向足量⑥的溶液中通入少量氯气反应的化学方程式_____ 。
(4)将③通入足量次氯酸钠溶液中发生反应的离子方程式为_____ 。
(1)该浓硝酸的物质的量浓度为
(2)物质①~⑦中,常温下可导电的物质为
(3)向足量⑥的溶液中通入少量氯气反应的化学方程式
(4)将③通入足量次氯酸钠溶液中发生反应的离子方程式为
您最近一年使用:0次
名校
3 . 实验室需用 硫酸铜溶液,下列有关该溶液的配制说法正确的是
硫酸铜溶液,下列有关该溶液的配制说法正确的是
 硫酸铜溶液,下列有关该溶液的配制说法正确的是
硫酸铜溶液,下列有关该溶液的配制说法正确的是A.用托盘天平称取胆矾 |
| B.实验中必须用到的玻璃仪器为:烧杯、量筒、容量瓶、玻璃棒 |
| C.定容时仰视容量瓶的刻度线,会造成所配溶液物质的量浓度偏高 |
| D.定容摇匀后发现液面低于刻度线,应再滴加蒸馏水至刻度线 |
您最近一年使用:0次
2024-02-10更新
|
265次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一上学期1月教学测评期末化学试题
4 . 下列说法中,正确的是
A. 的质量是 的质量是 |
B. 中含有的分子数约为 中含有的分子数约为 |
C. 的体积一定是 的体积一定是 |
D. 溶液中含有 溶液中含有 |
您最近一年使用:0次
5 . 某食品级Na2SO3,每袋中含Na2SO3 100.8 g。下列说法正确的是
| A.每袋添加剂中含钠离子0.8 mol |
| B.该添加剂可使紫色石蕊溶液退色 |
| C.每袋添加剂最多消耗氧气8.96 L |
D.某红酒中要求Na2SO3浓度为 ,每袋该添加剂可满足400 L红酒需要 ,每袋该添加剂可满足400 L红酒需要 |
您最近一年使用:0次
6 . 现有下列物质:①铜丝②FeCl3溶液③氯化氢气体④NaHSO4固体⑤干冰⑥ 胶体⑦硫酸亚铁铵晶体
胶体⑦硫酸亚铁铵晶体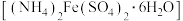 ⑧稀氨水
⑧稀氨水
(1)上述物质中属于电解质的是___________ (填序号,下同),能够导电的是___________ 。写出属于酸式盐的物质溶于水的电离方程式___________ 。
(2)②与⑧在溶液中反应的离子方程式为___________ 。
(3)硫酸亚铁铵晶体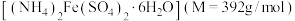 俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制
俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制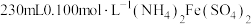 溶液,回答问题:
溶液,回答问题:
①配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需___________ 。
②用电子天平(精确度为0.01g)称量硫酸亚铁铵晶体___________ g。
③下列操作将导致所配制的溶液浓度偏高的是___________ (填选项)。
A.摩尔盐放置过程中失去了部分结晶水
B.配制过程中没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
(4)将VL标准状况下的物质③溶于100mL水中(水的密度近似为1g·mL-1),得到密度为ρg·mL-1的溶液,该溶液的物质的量浓度是___________ mol·L-1(列出计算式)。
 胶体⑦硫酸亚铁铵晶体
胶体⑦硫酸亚铁铵晶体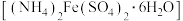 ⑧稀氨水
⑧稀氨水(1)上述物质中属于电解质的是
(2)②与⑧在溶液中反应的离子方程式为
(3)硫酸亚铁铵晶体
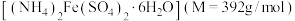 俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制
俗名为摩尔盐。某学校化学兴趣小组使用摩尔盐配制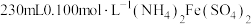 溶液,回答问题:
溶液,回答问题:①配制溶液过程中需要的玻璃仪器除量筒、烧杯、玻璃棒外,还需
②用电子天平(精确度为0.01g)称量硫酸亚铁铵晶体
③下列操作将导致所配制的溶液浓度偏高的是
A.摩尔盐放置过程中失去了部分结晶水
B.配制过程中没有洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.定容后振荡容量瓶发现液面低于刻度线,继续加蒸馏水定容
(4)将VL标准状况下的物质③溶于100mL水中(水的密度近似为1g·mL-1),得到密度为ρg·mL-1的溶液,该溶液的物质的量浓度是
您最近一年使用:0次
7 . 运用化学反应原理研究硫单质及其化合物的反应,对生产、生活、环境保护等领域有着重要的意义。
(1)工业上采用 催化还原
催化还原 ,不仅可以消除
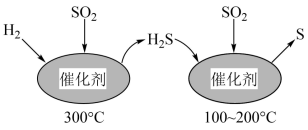
,不仅可以消除 污染,还可得到单质S。反应分两步完成,如图所示,
污染,还可得到单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为___________ 。
(2)工业上常用 溶液对燃煤烟气进行脱硫、脱硝。
溶液对燃煤烟气进行脱硫、脱硝。
已知 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成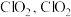 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 。
。
①实验室模拟脱硫过程:先加稀硫酸调节 吸收液的
吸收液的 为5,再向其中通入含
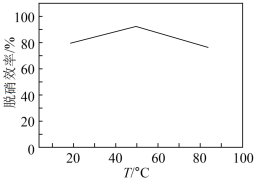
为5,再向其中通入含 的模拟烟气,测得脱硫效率(即
的模拟烟气,测得脱硫效率(即 的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于
的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于 时,随温度升高脱硫效率下降的原因是
时,随温度升高脱硫效率下降的原因是___________ 。
②煤燃烧排放的烟气含有 和
和 ,采用
,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有 和
和 的烟气通入盛有
的烟气通入盛有 溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
表中y=_______ 。若该溶液为 (吸收前后溶液体积不变),该过程转移的电子数为
(吸收前后溶液体积不变),该过程转移的电子数为______ mol。(写出计算过程)。
(1)工业上采用
 催化还原
催化还原 ,不仅可以消除
,不仅可以消除 污染,还可得到单质S。反应分两步完成,如图所示,
污染,还可得到单质S。反应分两步完成,如图所示, 催化还原
催化还原 第一步反应的化学方程式为
第一步反应的化学方程式为
(2)工业上常用
 溶液对燃煤烟气进行脱硫、脱硝。
溶液对燃煤烟气进行脱硫、脱硝。已知
 溶液具有强氧化性,酸性条件下
溶液具有强氧化性,酸性条件下 发生歧化反应生成
发生歧化反应生成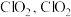 易溶于水,具有强氧化性,可氧化
易溶于水,具有强氧化性,可氧化 。
。①实验室模拟脱硫过程:先加稀硫酸调节
 吸收液的
吸收液的 为5,再向其中通入含
为5,再向其中通入含 的模拟烟气,测得脱硫效率(即
的模拟烟气,测得脱硫效率(即 的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于
的吸收率)随温度变化的曲线如图所示。结合已知信息分析,温度大于 时,随温度升高脱硫效率下降的原因是
时,随温度升高脱硫效率下降的原因是
②煤燃烧排放的烟气含有
 和
和 ,采用
,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。将含有 和
和 的烟气通入盛有
的烟气通入盛有 溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):
溶液的反应器中,反应一段时间后,测得溶液中离子浓度的有关数据如表(其他离子忽略不计):| 离子 |  |  |  |  |  |
浓度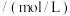 | 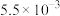 |  |  |  |  |
 (吸收前后溶液体积不变),该过程转移的电子数为
(吸收前后溶液体积不变),该过程转移的电子数为
您最近一年使用:0次
名校
8 . 如图是某硫酸试剂瓶上的部分内容。下列说法正确的是
硫酸化学纯( )( )( ) )品名:硫酸 化学式:  相对分子质量:98 密度:  质量分数:  |
A.该硫酸可以干燥 气体 气体 |
B.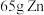 与该硫酸反应能产生 与该硫酸反应能产生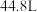 (标准状况)气体 (标准状况)气体 |
C.若不小心将该硫酸溅到了皮肤上,应立即用 溶液清洗 溶液清洗 |
D.实验室需要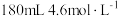 的稀硫酸,配制时应量取该硫酸 的稀硫酸,配制时应量取该硫酸 |
您最近一年使用:0次
9 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.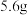 铁粉在 铁粉在 中充分燃烧,转移电子数为 中充分燃烧,转移电子数为 |
B.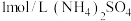 溶液中含有的 溶液中含有的 的数目为 的数目为 |
C.含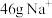 的 的 固体中的阴离子数目为 固体中的阴离子数目为 |
D.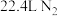 和 和 的混合气体中原子数目为 的混合气体中原子数目为 |
您最近一年使用:0次
名校
10 . 请回答:
(1)小苏打的化学式是___________ ;漂白粉的主要成分是___________ (用化学式表示)。
(2)质量分数为36.5%的HCl溶液,密度为1.17g/cm3,求其物质的量浓度为___________ mol/L。
(3)实验室用软锰矿制备氯气的离子方程式___________ 。
(1)小苏打的化学式是
(2)质量分数为36.5%的HCl溶液,密度为1.17g/cm3,求其物质的量浓度为
(3)实验室用软锰矿制备氯气的离子方程式
您最近一年使用:0次



