名校
1 . 化学实验室里有一瓶盐酸,上面的标签如图所示。下列说法正确的是

| A.该试剂瓶中的盐酸属于纯净物 |
B.配制100mL 1.00 的稀盐酸需该盐酸10mL 的稀盐酸需该盐酸10mL |
C.该盐酸物质的量浓度为12 |
| D.配制稀盐酸时,取用浓盐酸的量筒使用后应洗涤,并将洗涤液也注入容量瓶中 |
您最近一年使用:0次
2023-11-04更新
|
287次组卷
|
2卷引用:清华大学附属中学2023-2024学年高一上学期期中考试化学试题
名校
2 . 化学计量在化学知识体系中占有重要地位,请回答下列问题。
(1)标准状况下,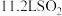 的物质的量是
的物质的量是___________ ,质量是___________ g。
(2)同温同压下,质量相等的 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是___________ ,密度最大的是___________ 。
(3) 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为___________ 。
(4) 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为___________ ,生成的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(5)现有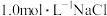 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为___________ 。
(1)标准状况下,
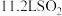 的物质的量是
的物质的量是(2)同温同压下,质量相等的
 、
、 、
、 、
、 四种气体中,含有分子数目最多的是
四种气体中,含有分子数目最多的是(3)
 中含有的
中含有的 为
为 ,则X的摩尔质量为
,则X的摩尔质量为(4)
 的盐酸与
的盐酸与 铁屑反应,参与反应的
铁屑反应,参与反应的 物质的量为
物质的量为 在标准状况下的体积为
在标准状况下的体积为(5)现有
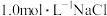 溶液
溶液 ,若取
,若取 该溶液用水稀释到
该溶液用水稀释到 ,所得溶液的
,所得溶液的 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
名校
解题方法
3 . 《黄帝九鼎神丹经诀》卷九中记载着“炼石胆取精华法”,即干馏石胆(胆矾)而获得硫酸。硫酸是一种重要的工业原料,可用于制造肥料、药物、炸药、颜料、洗涤剂、蓄电池等,也广泛应用于净化石油、金属冶炼等工业中。请根据要求回答下列问题:
(1)纯净的液态硫酸______ (填“能”或“几乎不能”)导电,在硫酸不断稀释的过程中,溶液导电能力的变化情况为______ 。
(2)硫酸是强酸,具有酸的通性,如稀硫酸与氧化铁反应的化学方程式为______ ,但浓硫酸与氧化亚铁反应的化学方程式为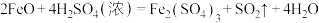 ,该反应属于
,该反应属于______ (填“氧化还原反应”或“非氧化还原反应”)。
(3)某浓硫酸的说明如图所示。该浓硫酸的物质的量浓度为______  ,从中取出100mL,则该100mL浓硫酸的物质的量浓度为
,从中取出100mL,则该100mL浓硫酸的物质的量浓度为______  ,含
,含 的物质的量为
的物质的量为______ mol。
(4)如果取5mL该浓硫酸,加水稀释至10mL,那么稀释后的硫酸的质量分数______ (填“大于”、“小于”或“等于”,下同)49%;如果取5mL该浓硫酸,加等质量的水稀释,那么稀释后的硫酸的物质的量浓度______ 原浓硫酸的物质的量浓度的一半。
(1)纯净的液态硫酸
(2)硫酸是强酸,具有酸的通性,如稀硫酸与氧化铁反应的化学方程式为
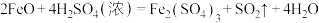 ,该反应属于
,该反应属于(3)某浓硫酸的说明如图所示。该浓硫酸的物质的量浓度为
 ,从中取出100mL,则该100mL浓硫酸的物质的量浓度为
,从中取出100mL,则该100mL浓硫酸的物质的量浓度为 ,含
,含 的物质的量为
的物质的量为| 硫酸 化学纯 CP 500mL 品名:硫酸 化学式:  相对分子质量:98 密度:1.84  质量分数:98% |
您最近一年使用:0次
名校
4 . 汽车、电动车一般使用铅酸蓄电池,某铅酸蓄电池用的是28%的稀硫酸,现用98%(密度1.84g/cm3)的浓硫酸配制该稀硫酸。下列说法中正确的是
| A.28%的稀硫酸中溶质与溶剂的质量比为28:100 |
| B.若配制3.5kg28%的稀硫酸,用托盘天平称量10kg98%的浓硫酸即可 |
| C.配制该稀硫酸时,把水沿容器内壁缓慢注入浓硫酸中 |
| D.若用该浓硫酸与水体积比1:1混合后得到的溶液溶质的质量分数大于49% |
您最近一年使用:0次
名校
解题方法
5 . 84消毒液、ClO2是常见的含氯消毒剂。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目_______ 。
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为_______ mol·L-1。
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是_______ 。
②试管2中纸片褪色更快的原因是_______ 。
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是_______ 。
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。
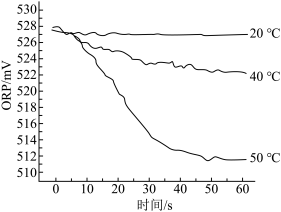
④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是_______ 。
资料:84消毒液中含氟微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映物质的氧化一还原性,ORP值越大,氧化性越强。通常情况下,应将84消毒液原液稀释后使用;一般不用于衣服等纺织品的洗涤消毒。
(1)制备ClO2的一种反应为:2NaClO3+2NaCl+2H2SO4=2ClO2↑+Cl2↑+2Na2SO4+2H2O,用单线桥法标出其电子转移的方向和数目
(2)取含次氯酸钠0.2mol·L-1的消毒液1mL,加水稀释至200mL,则稀释后次氯酸钠的物质的量浓度为
(3)为研究84消毒液的性质与使用条件,进行下列实验:
【实验1】向两支试管中分别加入2mL84消毒液,在试管l中加入2mL水,试管2中加入2mL白醋,再分别放入相同的红色纸片。观察到试管2中纸片褪色更快。
①实验中在试管l中加入2mL水的目的是
②试管2中纸片褪色更快的原因是
③如果实验中加浓盐酸,会有黄绿色气体产生,反应的离子方程式是
【实验2】测定84消毒液在不同温度时ORP随时间的变化情况,结果如图所示。

④实验表明,随温度升高,ORP值下降。50℃时ORP值下降较快的原因是
您最近一年使用:0次
22-23高一上·广东深圳·期末
名校
解题方法
6 . 实验室中需要配制0.2mol/L的CuSO4溶液480mL,请回答下面问题。
(1)用天平称取CuSO4•5H2O晶体的质量是_____ g。
(2)完成上述实验,除需要如图所示的仪器外,还需要的玻璃仪器是_____ 。
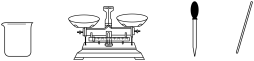
(3)在使用胆矾配制溶液时,需要使用两次玻璃棒,作用是_____ 。
(4)下列实验操作会使配制的溶液浓度偏低的是_____ 。
(5)若用0.2mol/LCuSO4溶液配制250mL0.1mol/LCuSO4溶液,需要量取_____ mL0.2mol/LCuSO4。
(6)铜屑放入稀硫酸中不发生反应,向体系通入O2,铜屑可以逐渐溶解生成CuSO4,该反应的离子方程式为_____ 。
(7)某养殖场消毒液由CuSO4、Na2SO4、NaCl混合而成,已知部分离子浓度如表:
该消毒液c(Cu2+)=_____ 。
(1)用天平称取CuSO4•5H2O晶体的质量是
(2)完成上述实验,除需要如图所示的仪器外,还需要的玻璃仪器是

(3)在使用胆矾配制溶液时,需要使用两次玻璃棒,作用是
(4)下列实验操作会使配制的溶液浓度偏低的是
| A.容量瓶内有水,未经过干燥处理 |
| B.定容时,仰视刻度线 |
| C.转移溶液后的烧杯和玻璃棒未洗涤 |
| D.定容后液面超过刻度线,吸出一部分水 |
(6)铜屑放入稀硫酸中不发生反应,向体系通入O2,铜屑可以逐渐溶解生成CuSO4,该反应的离子方程式为
(7)某养殖场消毒液由CuSO4、Na2SO4、NaCl混合而成,已知部分离子浓度如表:
| 离子符号 | Na+ | SO | Cl- |
| c/mol•L-1 | 1.3 | 0.4 | 0.9 |
您最近一年使用:0次
23-24高一上·浙江·期末
解题方法
7 . 下列对某些问题的认识正确的是
| A.98%的浓硫酸用等体积的水稀释后,硫酸的质量分数为49% |
| B.Na能与水反应,因此不能利用钠的置换反应制备其他金属单质X |
| C.纯碱属于盐,其水溶液不宜用带玻璃塞的玻璃瓶盛放 |
| D.铝合金、 不锈钢、足球烯(C60)都是重要的金属材料 |
您最近一年使用:0次
解答题-实验探究题
|
较易(0.85)
|
8 . 用胆矾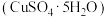 配制
配制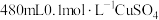 溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等。
溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等。
(1)下列有关容量瓶的使用方法的操作中,错误的是_______(填序号)。
(2)配制时,还缺少的玻璃仪器是_______ 。该实验中两次用到玻璃棒,其作用分别是搅拌和_______ 。
(3)配制该溶液时,可以选择用托盘天平称取固体 的质量为
的质量为_______ g。
(4)定容时的操作:当液面接近容量瓶刻度线 时,改用胶头滴管滴加蒸馏水至
时,改用胶头滴管滴加蒸馏水至_______ ,再将容量瓶塞盖好,反复上下颠倒摇匀。
(5)配制过程中,下列操作使所配溶液的浓度偏大的有_______(填序号)。
(6)从配制好的 溶液中取出
溶液中取出 ,加蒸馏水将其稀释至
,加蒸馏水将其稀释至 ,稀释后
,稀释后 溶液的浓度为
溶液的浓度为_______  。
。
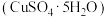 配制
配制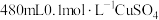 溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等。
溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等。(1)下列有关容量瓶的使用方法的操作中,错误的是_______(填序号)。
| A.使用容量瓶前检查它是否漏水 |
| B.容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 |
| C.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁 |
| D.容量瓶是细颈、梨形的平底玻璃瓶,瓶口配有磨口玻璃塞或塑料塞 |
(3)配制该溶液时,可以选择用托盘天平称取固体
 的质量为
的质量为(4)定容时的操作:当液面接近容量瓶刻度线
 时,改用胶头滴管滴加蒸馏水至
时,改用胶头滴管滴加蒸馏水至(5)配制过程中,下列操作使所配溶液的浓度偏大的有_______(填序号)。
| A.用“左码右物”的称量方法称量晶体 |
| B.移液后,未洗涤烧杯和玻璃棒 |
| C.胆矾晶体部分失去结晶水 |
| D.定容时,俯视刻度线 |
 溶液中取出
溶液中取出 ,加蒸馏水将其稀释至
,加蒸馏水将其稀释至 ,稀释后
,稀释后 溶液的浓度为
溶液的浓度为 。
。
您最近一年使用:0次
9 . 配制250mL0.125mol/L的NaOH溶液
(1)通过计算需要称量NaOH_______ g。进溶解、冷却后,需转移到_______ mL的容量瓶中,再洗掉烧杯、玻璃棒再将洗涤液转移到容量瓶中,最后,缓缓地把蒸馏水注入容量瓶,直到液面接近刻度_______ 处,改用_______ (仪器)加水到刻度线,使溶液的_______ 正好跟刻度线相切。塞好瓶塞,反复摇匀。
(2)配制稀的氢氧化钠溶液,也可用稀释法。如,取10mL 6mol/L的NaOH溶液加水稀释至100mL,溶液的物质的量浓度变为_______ mol/L。
(1)通过计算需要称量NaOH
(2)配制稀的氢氧化钠溶液,也可用稀释法。如,取10mL 6mol/L的NaOH溶液加水稀释至100mL,溶液的物质的量浓度变为
您最近一年使用:0次
名校
解题方法
10 . 关于如图所示过程的说法正确的是
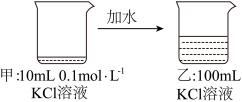

| A.甲比乙中溶质的质量分数小 | B.乙中 |
| C.乙比甲中KCl的溶解度大 | D.乙中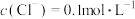 |
您最近一年使用:0次
2023-01-05更新
|
225次组卷
|
3卷引用:北京市东城区2022-2023学年高一上学期期末统一检测化学试卷



