22-23高一上·全国·课时练习
解题方法
1 . 关于溶液稀释,下列说法正确的是
| A.稀释过程中,离子的浓度不变 | B.稀释过程中,溶液的物质的量不变 |
| C.稀释过程中,溶质的质量及物质的量不变 | D.稀释过程中,溶液的密度不变 |
您最近一年使用:0次
21-22高一·全国·假期作业
解题方法
2 . 2020年,全球爆发的新型冠状病毒肺炎疫情严重影响人们的身体健康。“84消毒液”能有效杀灭各种细菌和病毒,某同学购买了一瓶某品牌的“84消毒液”,其瓶体上的消毒液说明如图:
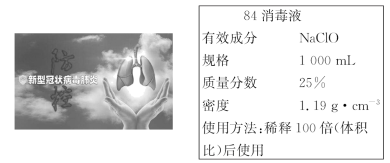
(1)工业上制备“84消毒液”的化学方程式为____ 。
(2)该“84消毒液”中的NaClO的物质的量浓度为____ 。
(3)该同学取100mL“84消毒液”稀释后用于消毒,稀释后的溶液的物质的量浓度_____ 。

(1)工业上制备“84消毒液”的化学方程式为
(2)该“84消毒液”中的NaClO的物质的量浓度为
(3)该同学取100mL“84消毒液”稀释后用于消毒,稀释后的溶液的物质的量浓度
您最近一年使用:0次
名校
3 . 溶液的配制过程能引起浓度偏低的是
①用1g的饱和氨水加5g水配成1:5(体积比)的稀氨水
②配制一定浓度的氢氧化钠溶液,称量10.5g 溶质固体时,10g砝码放入托盘天平左盘并移动游码至0.5刻度处进行称量(其他操作均正确)
③10%的乙醇的20%的乙醇等体积混合配制15%的乙醇溶液
④质量分数为30%和50%的两种硫酸等质量混合配成40%的硫酸
⑤在90mL水中加入18.4mol/L的硫酸10mL,配制1.84mol/L的硫酸溶液
⑥向100g浓度为cmol/L的硫酸中加入100mL水,可得浓度为c/2mol/L 的硫酸
⑦用浓硫酸配制一定浓度的稀硫酸,量取浓溶液时仰视刻度线
①用1g的饱和氨水加5g水配成1:5(体积比)的稀氨水
②配制一定浓度的氢氧化钠溶液,称量10.5g 溶质固体时,10g砝码放入托盘天平左盘并移动游码至0.5刻度处进行称量(其他操作均正确)
③10%的乙醇的20%的乙醇等体积混合配制15%的乙醇溶液
④质量分数为30%和50%的两种硫酸等质量混合配成40%的硫酸
⑤在90mL水中加入18.4mol/L的硫酸10mL,配制1.84mol/L的硫酸溶液
⑥向100g浓度为cmol/L的硫酸中加入100mL水,可得浓度为c/2mol/L 的硫酸
⑦用浓硫酸配制一定浓度的稀硫酸,量取浓溶液时仰视刻度线
| A.①③⑤⑥ | B.②③⑥ | C.①②④ | D.②⑤⑦ |
您最近一年使用:0次
名校
4 . 共和国勋章获得者钟南山院士强调,要注意疫情防控常态化,坚持做好日常消毒工作。常见的消毒剂有漂白粉、84消毒液(有效成分NaClO)、双氧水等。
Ⅰ.已知某“84消毒液”瓶体部分标签如下所示:84消毒液:(有效成分)NaClO;(规格)1000mL;(质量分数)25%;(密度)1.19g/cm3
(1)该“84消毒液”的物质的量浓度为_______  (计算结果保留两位有效数字)。
(计算结果保留两位有效数字)。
(2)“84消毒液”与“洁厕灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。写出反应的离子方程式:_______ ;
(3)实验室用 的浓盐酸配制
的浓盐酸配制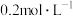 的盐酸240mL;得浓盐酸的体积为
的盐酸240mL;得浓盐酸的体积为_______ mL;使用的定量仪器有_______ 。
(4)84消毒液若与双氧水溶液混合减弱或失去杀菌消毒功能(反应产物之一是 ),解释原因
),解释原因_______ 。
Ⅱ.实验室制备84消毒液的装置如图1所示:
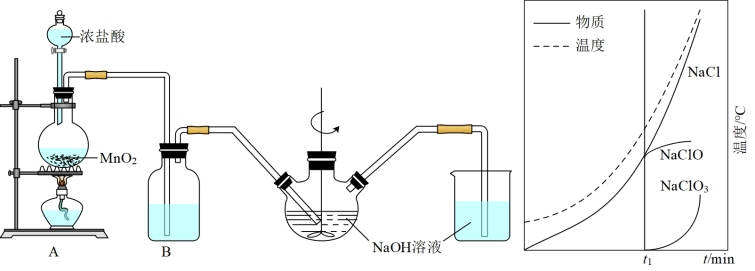
(5)装置B中盛放的试剂是_______ ;简述该装置对制取NaClO的作用_______ 。
(6)三颈烧瓶中生成各物质的物质的量和溶液的温度随时间的变化如图2所示。 分钟后所发生主要反应的化学方程式为
分钟后所发生主要反应的化学方程式为_______ 。
Ⅰ.已知某“84消毒液”瓶体部分标签如下所示:84消毒液:(有效成分)NaClO;(规格)1000mL;(质量分数)25%;(密度)1.19g/cm3
(1)该“84消毒液”的物质的量浓度为
 (计算结果保留两位有效数字)。
(计算结果保留两位有效数字)。(2)“84消毒液”与“洁厕灵”(主要成分为盐酸)一起使用反而会弄巧成拙,产生有毒的气体,造成中毒事件。写出反应的离子方程式:
(3)实验室用
 的浓盐酸配制
的浓盐酸配制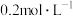 的盐酸240mL;得浓盐酸的体积为
的盐酸240mL;得浓盐酸的体积为(4)84消毒液若与双氧水溶液混合减弱或失去杀菌消毒功能(反应产物之一是
 ),解释原因
),解释原因Ⅱ.实验室制备84消毒液的装置如图1所示:

(5)装置B中盛放的试剂是
(6)三颈烧瓶中生成各物质的物质的量和溶液的温度随时间的变化如图2所示。
 分钟后所发生主要反应的化学方程式为
分钟后所发生主要反应的化学方程式为
您最近一年使用:0次
2022高一·上海·专题练习
名校
解题方法
5 . 现有1 L含SO3为30%的发烟硫酸(密度为1.95 g/cm3),要把它稀释成质量分数为95%的浓硫酸,需加水约为
| A.120 mL | B.180 mL | C.240 mL | D.300 mL |
您最近一年使用:0次
6 . 将1LNa2CO3溶液加水稀释,稀释过程中c(Na+)随溶液体积的变化曲线如图,下列说法正确的是
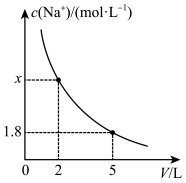

| A.将Na2CO3溶液稀释需用到烧杯、玻璃棒、漏斗等仪器 |
| B.图中x=9 |
| C.将该Na2CO3溶液与足量盐酸反应最多收集100.8LCO2 |
| D.Na2CO3溶液的初始浓度为4.5mol·L-1 |
您最近一年使用:0次
7 . 氯及其化合物在生产生活中有重要的作用。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为_______ 。
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与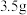 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是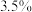 。
。
上述500mL“××牌84消毒液”中含有的 的质量为
的质量为_______ g(“有效氯”含量按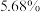 、溶液密度按
、溶液密度按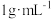 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按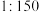 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为_______  (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。
(2) 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
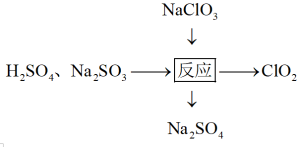
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目_______ ,该反应的还原剂为_______ 。
(1)已知某品牌的84消毒液和洁厕灵的部分标签如图所示:
| ××牌洁厕灵 规格:1L 有效成分:盐酸,表面活性剂,香精 | ××牌84消毒液 规格:  有效成分:  (“有效氯”含量:  ) ) |
①王女士在清洁马桶时,在倒入上述洁厕灵后将上述84消毒液也倒入其中,随后突然晕倒,送往医院抢救无效死亡。该过程发生反应的离子方程式为
②已知“有效氯”的基本含义是指一定质量的这种消毒剂与多少质量的氯气的氧化能力相当,其数值可以用此时氯气的质量对消毒剂质量的百分比表示。例如,100g某84消毒液与
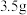 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是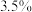 。
。上述500mL“××牌84消毒液”中含有的
 的质量为
的质量为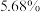 、溶液密度按
、溶液密度按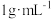 计算);现需要将原消毒液与水按
计算);现需要将原消毒液与水按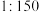 比例稀释后用于织物消毒。则稀释后的溶液中
比例稀释后用于织物消毒。则稀释后的溶液中 的浓度为
的浓度为 (忽略混合后溶液体积变化,保留两位有效数字)。
(忽略混合后溶液体积变化,保留两位有效数字)。(2)
 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目
您最近一年使用:0次
2022-01-25更新
|
242次组卷
|
2卷引用:山东省威海市2021-2022学年高一上学期期末考试化学试题
8 . 实验室里需用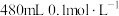 的
的 溶液。现有下列仪器:
溶液。现有下列仪器:
A.烧杯 B.500mL量筒 C.500mL容量瓶 D.玻璃棒 E.天平
(1)用无水 固体配制时,必须使用的仪器有
固体配制时,必须使用的仪器有___________ (填序号),还缺少的玻璃仪器是___________ (写名称)。
(2)用托盘天平称取无水 固体的质量为
固体的质量为___________ g。
(3)假如其他操作均准确无误,下列操作会使所配置溶液浓度偏大的是___________(填序号)。
(4)将 的
的 溶液稀释成
溶液稀释成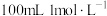 的
的 溶液,需要用量筒量取
溶液,需要用量筒量取 的
的 溶液
溶液___________ mL。
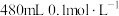 的
的 溶液。现有下列仪器:
溶液。现有下列仪器:A.烧杯 B.500mL量筒 C.500mL容量瓶 D.玻璃棒 E.天平
(1)用无水
 固体配制时,必须使用的仪器有
固体配制时,必须使用的仪器有(2)用托盘天平称取无水
 固体的质量为
固体的质量为(3)假如其他操作均准确无误,下列操作会使所配置溶液浓度偏大的是___________(填序号)。
| A.定容时俯视观察刻度线 |
B.移液时,对用于溶解 的烧杯没有洗涤 的烧杯没有洗涤 |
| C.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 |
| D.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,又补加水至刻度线 |
 的
的 溶液稀释成
溶液稀释成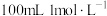 的
的 溶液,需要用量筒量取
溶液,需要用量筒量取 的
的 溶液
溶液
您最近一年使用:0次
2022-01-20更新
|
313次组卷
|
2卷引用:安徽省蚌埠市2021-2022学年高一上学期期末学业水平测试化学试题
9 . 孔雀石铜矿(含Cu、Fe、Al等元素)是工业上提取铁、铜等金属的原材料,某工厂由孔雀石铜矿制备单质铜和绿矾( )的工艺流程如下:
)的工艺流程如下:
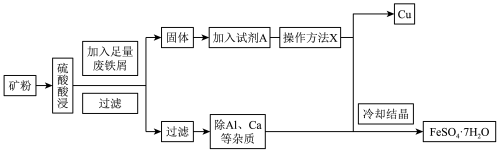
回答下列问题:
(1)试剂A为___________ ,此步骤涉及反应的离子方程式是___________ ,1molA参与上述反应转移电子的物质的量为___________ 。
(2)操作X是___________ 。
(3)实验室需要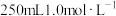 稀硫酸,化学小组用98%浓硫酸(
稀硫酸,化学小组用98%浓硫酸(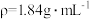 )配制上述稀硫酸,配制过程中可能用到下列仪器:①100mL量筒②25mL量筒③烧杯④托盘天平⑤250mL容量瓶⑥胶头滴管⑦玻璃棒,按使用时出现的先后顺序排列是___________。
)配制上述稀硫酸,配制过程中可能用到下列仪器:①100mL量筒②25mL量筒③烧杯④托盘天平⑤250mL容量瓶⑥胶头滴管⑦玻璃棒,按使用时出现的先后顺序排列是___________。
(4)将稀释后的硫酸转移到容量瓶之前需___________ 。若将稀释后的硫酸立即转移到容量瓶将使所配溶液的物质的量浓度___________ 。(填“偏高”“偏低”或“无影响”)
 )的工艺流程如下:
)的工艺流程如下:
回答下列问题:
(1)试剂A为
(2)操作X是
(3)实验室需要
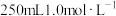 稀硫酸,化学小组用98%浓硫酸(
稀硫酸,化学小组用98%浓硫酸(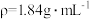 )配制上述稀硫酸,配制过程中可能用到下列仪器:①100mL量筒②25mL量筒③烧杯④托盘天平⑤250mL容量瓶⑥胶头滴管⑦玻璃棒,按使用时出现的先后顺序排列是___________。
)配制上述稀硫酸,配制过程中可能用到下列仪器:①100mL量筒②25mL量筒③烧杯④托盘天平⑤250mL容量瓶⑥胶头滴管⑦玻璃棒,按使用时出现的先后顺序排列是___________。| A.①③⑤⑦⑥ | B.②③⑦⑤⑥ | C.④③⑤⑦⑥ | D.①③⑦⑤⑥ |
您最近一年使用:0次
10 . 回答下列问题。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。属于混合物的是___________ (填序号,下同);能导电的是___________ ;属于电解质的是___________ ;属于非电解质的是___________ 。分别写出④和⑤的电离方程式:___________ 。
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①过氧乙酸(CH3COOOH)的摩尔质量是___________ 。38gCH3COOOH中含有的O原子数为___________ NA,含有的H原子的物质的量为___________ 。
②过氧化氢(H2O2)极易分解,在MnO2催化作用下能完全分解为水和氧气,写出其化学方程式___________ 。过氧化氢的水溶液叫双氧水,2mol/L的双氧水500mL完全分解生成氧气的体积为___________ L(标准状态),转移电子数为___________ NA
③在相同状态下质量相同的臭氧和氯气,他们的物质的量之比为___________ ,原子个数之比为___________ ,密度之比为___________ 。
④84消毒液的有效成分为NaClO,同时还含有少量的NaCl,某84消毒液有效氯含量为3.55%,密度1.0g/mL,将此溶液稀释200倍后进行使用,此时c(NaClO) =___________ mol/L。
(1)下列物质中:①SO2;②液态氯化氢;③CH4;④熔融NaOH;⑤NH4Cl固体;⑥氨水。属于混合物的是
(2)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常见的消毒药品:84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。回答下面问题:
①过氧乙酸(CH3COOOH)的摩尔质量是
②过氧化氢(H2O2)极易分解,在MnO2催化作用下能完全分解为水和氧气,写出其化学方程式
③在相同状态下质量相同的臭氧和氯气,他们的物质的量之比为
④84消毒液的有效成分为NaClO,同时还含有少量的NaCl,某84消毒液有效氯含量为3.55%,密度1.0g/mL,将此溶液稀释200倍后进行使用,此时c(NaClO) =
您最近一年使用:0次



