名校
解题方法
1 . 用0.1000mol/L 标准溶液滴定20.00mL
标准溶液滴定20.00mL 溶液,测得溶液电导率
溶液,测得溶液电导率 及
及 随滴入
随滴入 标准溶液的体积
标准溶液的体积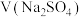 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
 标准溶液滴定20.00mL
标准溶液滴定20.00mL 溶液,测得溶液电导率
溶液,测得溶液电导率 及
及 随滴入
随滴入 标准溶液的体积
标准溶液的体积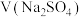 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是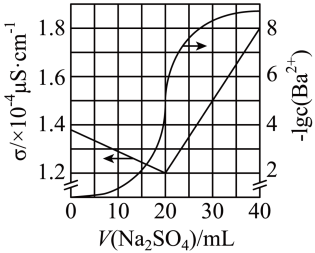
A. 溶液的浓度为0.1000mol/L 溶液的浓度为0.1000mol/L |
B. |
C.等浓度的 比 比 导电能力差 导电能力差 |
D.配制 标准溶液时,容量瓶洗涤后未干燥,所配溶液的浓度不变 标准溶液时,容量瓶洗涤后未干燥,所配溶液的浓度不变 |
您最近一年使用:0次
2 . 向一定体积和浓度的Ba(OH)2溶液中滴入某浓度的NH4HSO4溶液,其导电能力随滴入溶液体积的变化如图所示。下列说法不正确的是
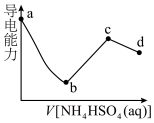

A.bc段之间存在某点,其溶液中:c(NH )=2c(SO )=2c(SO ) ) |
B.c点溶液中:c(H+)+c(NH )=2c(SO )=2c(SO )+c(OH-) )+c(OH-) |
| C.bc段反应的离子方程式为OH-+H+=H2O |
| D.b点溶液导电能力最弱,d点过后,最终溶液的导电能力几乎不再变化 |
您最近一年使用:0次
解题方法
3 . 向一定体积的Ba(OH)2溶液中逐滴加入NaHSO4稀溶液,其导电能力随加入的溶液体积变化的曲线如下图所示。下列说法中不正确 的是
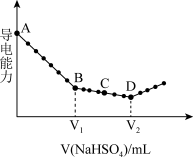

A.AB段反应的离子方程式:Ba2++OH-+H++S =BaSO4↓+H2O =BaSO4↓+H2O |
| B.C点发生反应的离子方程式:OH-+H+=H2O |
C.D点对应的溶液中存在的离子主要是Na+、S |
| D.V1、V2的关系为V1∶V2=2∶5 |
您最近一年使用:0次
名校
4 . 在两份相同的Ba(OH)2溶液中,分别滴入相同浓度的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如下图所示。(已知:相同体积、相同浓度的H2SO4、NaHSO4液中,H2SO4、NaHSO4的数量相同)
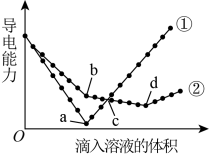
(1)图中①代表滴加哪种溶液的变化曲线___________ 。(填化学式)
(2)b点溶液中大量存在的离子是___________ 。
(3)a、d两点对应的溶液均显___________ (填“酸性”、“中性”、“碱性)
(4)曲线①中的a点导电能力最弱的原因是___________ 。(用化学方程式表示)
(5)c点两溶液中氢离子数量①___________ ②。(填大于,小于或等于)
(6)曲线②中的c点显___________ (填“酸性”、“中性”、“碱性”)
(7)曲线②中的b、d两点对应所加溶液的体积比为___________ 。

(1)图中①代表滴加哪种溶液的变化曲线
(2)b点溶液中大量存在的离子是
(3)a、d两点对应的溶液均显
(4)曲线①中的a点导电能力最弱的原因是
(5)c点两溶液中氢离子数量①
(6)曲线②中的c点显
(7)曲线②中的b、d两点对应所加溶液的体积比为
您最近一年使用:0次
名校
解题方法
5 . 分类是化学研究中常用的方法。下列分类方法正确的是
| A.漂白粉、氢氧化铁胶体、冰水混合物、氯水、铝热剂都属于混合物 |
B.已知次磷酸 与足量的 与足量的 反应只能生成一种盐 反应只能生成一种盐 ,则该盐为正盐 ,则该盐为正盐 |
C. 溶于氢氧化钠可以发生 溶于氢氧化钠可以发生 ,故 ,故 为酸性氧化物 为酸性氧化物 |
D. 溶于水能导电,故 溶于水能导电,故 属于电解质 属于电解质 |
您最近一年使用:0次
6 . 根据下列物质:① ②
② ③
③ 溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧
溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧ 晶体,回答下列有关问题:
晶体,回答下列有关问题:
(1)以上物质中属于强电解质的是________ (填编号)
(2)常温,测得 中
中 为
为 ,则
,则 在该温度下的电离常数
在该温度下的电离常数 约为
约为___________ (结果保留一位小数)
(3)常温, ,下列有关说法正确的是_________。
,下列有关说法正确的是_________。
(4)室温下,将三支装入含酚酞的 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入
溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入CaO。写出
晶体,在乙烧杯中加入CaO。写出 溶液中碳元素的守恒关系式:
溶液中碳元素的守恒关系式:___________ ;一段时间后,甲烧杯试管中溶液颜色___________ (填“变深”、“变浅”、“不变”);结合方程式解释乙烧杯中加CaO后其试管内颜色变化的原因:__________ 。
(5)将1g 溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程,
溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程, 始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
 ②
② ③
③ 溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧
溶液 ④冰醋酸⑤CO2 ⑥Mg ⑦CaO ⑧ 晶体,回答下列有关问题:
晶体,回答下列有关问题:(1)以上物质中属于强电解质的是
(2)常温,测得
 中
中 为
为 ,则
,则 在该温度下的电离常数
在该温度下的电离常数 约为
约为(3)常温,
 ,下列有关说法正确的是_________。
,下列有关说法正确的是_________。| A.向冰醋酸中加水,溶液的导电能力先增大后减小 |
B.向 溶液中加水稀释, 溶液中加水稀释, 增大 增大 |
C.等温等浓度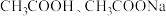 混合溶液中: 混合溶液中: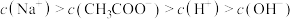 |
D.pH为3的 溶液中,水电离的 溶液中,水电离的 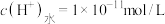 |
(4)室温下,将三支装入含酚酞的
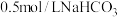 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入
溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入CaO。写出
晶体,在乙烧杯中加入CaO。写出 溶液中碳元素的守恒关系式:
溶液中碳元素的守恒关系式:(5)将1g
 溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程,
溶于100mL蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入10mL蒸馏水(加水过程, 始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
始终未完全溶解),观察电导率的变化,重复操作,绘图如下: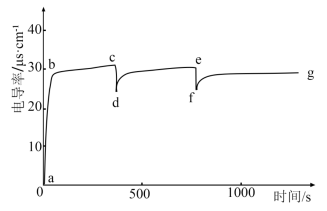
| A.c、e点电导率相等 |
| B.d、f点为饱和溶液 |
C.b→c电导率基本不变的原因是 到溶解平衡 到溶解平衡 |
| D.g点再加10mL蒸馏水可重复c→d、e→f图像 |
您最近一年使用:0次
2024-01-22更新
|
105次组卷
|
2卷引用:广西钦州市第四中学2023-2024学年高二上学期1月考试化学试卷
名校
7 . 已知: ;
; 。现有常温下由水电离出的
。现有常温下由水电离出的 均为
均为 的4种溶液:①HCl溶液②
的4种溶液:①HCl溶液② 溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是
溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是
 ;
; 。现有常温下由水电离出的
。现有常温下由水电离出的 均为
均为 的4种溶液:①HCl溶液②
的4种溶液:①HCl溶液② 溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是
溶液③NaOH溶液④氨水。有关上述溶液的比较中不正确的是A.等体积的①、③溶液分别与足量铝粉反应,生成 的量③多 的量③多 |
B.向等体积溶液中分别加水稀释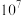 倍后,溶液的pH:④≈③≈②≈① 倍后,溶液的pH:④≈③≈②≈① |
C.四种溶液以体积比 混合后,所得溶液显中性 混合后,所得溶液显中性 |
| D.等体积的四种溶液导电能力顺序:④≈②>①≈③ |
您最近一年使用:0次
名校
解题方法
8 . 某学习小组用电导率传感器完成了两组测定。实验Ⅰ:在 溶液中滴入
溶液中滴入 溶液;实验Ⅱ:向
溶液;实验Ⅱ:向 溶液中滴入
溶液中滴入 溶液。两个实验的电导率变化情况如下图。下列相关说法正确的是
溶液。两个实验的电导率变化情况如下图。下列相关说法正确的是

 溶液中滴入
溶液中滴入 溶液;实验Ⅱ:向
溶液;实验Ⅱ:向 溶液中滴入
溶液中滴入 溶液。两个实验的电导率变化情况如下图。下列相关说法正确的是
溶液。两个实验的电导率变化情况如下图。下列相关说法正确的是
| A.曲线①代表的是实验Ⅱ的测定结果 |
B.ab段和de段的离子方程式均为 |
C.cd段的离子方程式为: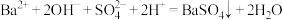 |
| D.b、d两点的溶质成分相同 |
您最近一年使用:0次
2024-01-11更新
|
194次组卷
|
2卷引用:河南省郑州市2023-2024学年高三上学期第一次质量检测化学试题
名校
解题方法
9 . 下列选项描述与对应图像相符的是
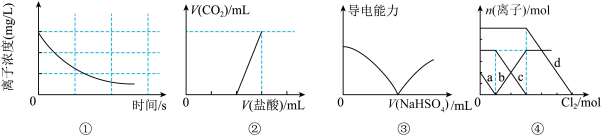

A.图①为新制氯水在阳光直射时,溶液中 浓度随着时间变化的曲线 浓度随着时间变化的曲线 |
B.图②为往 与 与 的物质的量之比为 的物质的量之比为 的混合液中滴加盐酸的体积与产生 的混合液中滴加盐酸的体积与产生 体积变化的图像 体积变化的图像 |
C.图③为往 溶液中滴加 溶液中滴加 溶液的体积与导电性变化的图像 溶液的体积与导电性变化的图像 |
D.图④为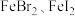 混合液中部分离子的物质的量随氯气通入的变化图像,其中a代表的是 混合液中部分离子的物质的量随氯气通入的变化图像,其中a代表的是 |
您最近一年使用:0次
2023-12-27更新
|
540次组卷
|
3卷引用:湖北省(T8联考)2024届高三上学期第一次学业质量评价化学试题
名校
解题方法
10 . Ⅰ.有下列物质:① 固体;②
固体;② ;③
;③ ;④稀硫酸;⑤二氧化碳气体;⑥铜;⑦醋酸;⑧蔗糖晶体;⑨熔融氧化钠。
;④稀硫酸;⑤二氧化碳气体;⑥铜;⑦醋酸;⑧蔗糖晶体;⑨熔融氧化钠。
(1)属于强电解质的是(用序号填空)_______ ;
(2)②在水溶液中的电离方程式为_______ ,①与②在溶液中反应使溶液呈中性的离子方程式为_______ 。
(3)③与⑥可以发生如下反应: ,氧化剂与还原剂的个数比为
,氧化剂与还原剂的个数比为_______ 。
Ⅱ.有一瓶无色透明溶液,只含 、
、 、
、 、
、 、
、 、
、 、
、 中的某几种,且每种离子的个数一样多,经实验:
中的某几种,且每种离子的个数一样多,经实验:
①取少量原溶液加入足量的 溶液产生白色沉淀,
溶液产生白色沉淀,
②取少量原溶液加 溶液不产写沉淀;
溶液不产写沉淀;
③取少量原溶液加 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
回答下列问题:
(4)试分析原溶液中一定含有的离子是_______ ,一定不含有的阴离子是_______ 。
(5)写出①中反应的离子方程式:_______ 。
 固体;②
固体;② ;③
;③ ;④稀硫酸;⑤二氧化碳气体;⑥铜;⑦醋酸;⑧蔗糖晶体;⑨熔融氧化钠。
;④稀硫酸;⑤二氧化碳气体;⑥铜;⑦醋酸;⑧蔗糖晶体;⑨熔融氧化钠。(1)属于强电解质的是(用序号填空)
(2)②在水溶液中的电离方程式为
(3)③与⑥可以发生如下反应:
 ,氧化剂与还原剂的个数比为
,氧化剂与还原剂的个数比为Ⅱ.有一瓶无色透明溶液,只含
 、
、 、
、 、
、 、
、 、
、 、
、 中的某几种,且每种离子的个数一样多,经实验:
中的某几种,且每种离子的个数一样多,经实验:①取少量原溶液加入足量的
 溶液产生白色沉淀,
溶液产生白色沉淀,②取少量原溶液加
 溶液不产写沉淀;
溶液不产写沉淀;③取少量原溶液加
 溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。回答下列问题:
(4)试分析原溶液中一定含有的离子是
(5)写出①中反应的离子方程式:
您最近一年使用:0次



