解题方法
1 . 硼氢化钠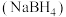 在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为
在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为 ,含少量杂质
,含少量杂质 )制取
)制取 ,其工艺流程如下:
,其工艺流程如下:

已知:硼氢化钠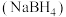 常温下能与水反应,易溶于异丙胺(沸点为
常温下能与水反应,易溶于异丙胺(沸点为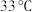 )。
)。
(1) 和
和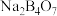 都是硼酸盐,请写出一元弱酸硼酸
都是硼酸盐,请写出一元弱酸硼酸 在水中的电离方程式
在水中的电离方程式_______ 。
(2)粉碎的目的是_______ ;滤渣的成分是_______ (写化学式、下同)。
(3)操作1的步骤是____ 、冷却结晶;操作2、操作3的名称分别为_____ 、_______ 。
(4)高温合成过程中,加料之前需先在反应器中通入氩气,该操作的目的是_______ 。
(5)流程中可循环利用的物质是_______ 。写出副产物硅酸钠的一种用途_______ 。
(6) 被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克
被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克 的还原能力。
的还原能力。 的有效氢含量为
的有效氢含量为_____ (保留两位小数)。
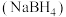 在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为
在化工等领域具有重要的应用价值,工业上可用硼镁矿(生要成分为 ,含少量杂质
,含少量杂质 )制取
)制取 ,其工艺流程如下:
,其工艺流程如下:
已知:硼氢化钠
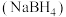 常温下能与水反应,易溶于异丙胺(沸点为
常温下能与水反应,易溶于异丙胺(沸点为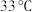 )。
)。(1)
 和
和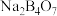 都是硼酸盐,请写出一元弱酸硼酸
都是硼酸盐,请写出一元弱酸硼酸 在水中的电离方程式
在水中的电离方程式(2)粉碎的目的是
(3)操作1的步骤是
(4)高温合成过程中,加料之前需先在反应器中通入氩气,该操作的目的是
(5)流程中可循环利用的物质是
(6)
 被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克
被称为万能还原剂,“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克 的还原能力。
的还原能力。 的有效氢含量为
的有效氢含量为
您最近一年使用:0次
2022·江苏·模拟预测
解题方法
2 . 含硫矿物如黄铁矿(FeS2)、黄铜矿、芒硝在工业上有着重要的用途。收集黄铜矿炼铜过程中产生的SO2制备SO3,其反应为2SO2(g)+O2(g) 2SO3(g)
2SO3(g) 
 下列有关说法正确的是
下列有关说法正确的是

 2SO3(g)
2SO3(g) 
 下列有关说法正确的是
下列有关说法正确的是
| A.SO2溶于水所得溶液能导电,所以SO2是电解质 |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.电负性:O<S |
| D.黄铜矿的晶胞如图所示,则其化学式为:CuFeS2 |
您最近一年使用:0次
解题方法
3 . 煤和石油是重要的能源物质,一方面对其开发利用推动人类社会快速进入工业文明时代,另一方面化石燃料燃烧产生 带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
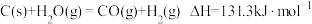
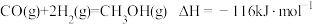
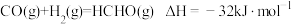
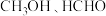 等产物在化工生产中都有广泛用途。下列有关
等产物在化工生产中都有广泛用途。下列有关 的说法正确的是
的说法正确的是
 带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为:
带来的环境问题日益凸显,“碳中和”已成为新时代绿色发展理念。煤经汽化、液化后再利用,可提高效能、降低污染,其常见原理为: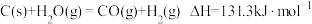
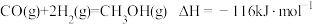
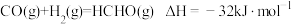
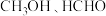 等产物在化工生产中都有广泛用途。下列有关
等产物在化工生产中都有广泛用途。下列有关 的说法正确的是
的说法正确的是A. 中 中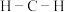 的键角比 的键角比 中的大 中的大 |
B. 的水溶液不能导电 的水溶液不能导电 |
C. 的空间构型为平面正三角形 的空间构型为平面正三角形 |
D. 和 和 形成的 形成的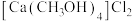 中有6个配位键 中有6个配位键 |
您最近一年使用:0次
4 . 硼及其化合物生产中有广泛用途,硼和铝位于同主族,具有相类似的化学性质。
(1)硼和氯气反应生成 BCl3,在该分子中,硼原子最外层有__________ 个电子。
(2)硼与氢氧化钠溶液反应生成 Na[B(OH)4](四羟基合硼酸钠)和氢气,该反应的化学方程式为____________ 。
(3)B(OH)3(硼酸)是一元弱酸,它在水中类似氨的电离: NH3+H2O⇌ +OH- ,硼酸在水中电离的方程式为
+OH- ,硼酸在水中电离的方程式为____ 。
(4)NaBH4 是有机合成中重要的还原剂。工业上合成方法之一是:Na2B4O7 +16Na+8H2 +7SiO2 7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是
7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是___________ ,制备1 mol NaBH4时转移 ____________ mol 电子。
(5)NaBH4与水反应生成Na[B(OH)4]和一种气体,写出化学方程式:_____________ 。
(1)硼和氯气反应生成 BCl3,在该分子中,硼原子最外层有
(2)硼与氢氧化钠溶液反应生成 Na[B(OH)4](四羟基合硼酸钠)和氢气,该反应的化学方程式为
(3)B(OH)3(硼酸)是一元弱酸,它在水中类似氨的电离: NH3+H2O⇌
 +OH- ,硼酸在水中电离的方程式为
+OH- ,硼酸在水中电离的方程式为(4)NaBH4 是有机合成中重要的还原剂。工业上合成方法之一是:Na2B4O7 +16Na+8H2 +7SiO2
 7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是
7Na2SiO3 +4NaBH4 ,在该反应中,氧化剂是(5)NaBH4与水反应生成Na[B(OH)4]和一种气体,写出化学方程式:
您最近一年使用:0次



