名校
解题方法
1 . 为了探究铁及其化合物的氧化性和还原性,某同学设计了如下实验方案,其中符合实验要求且完全正确的是( )
| 选项 | 实验操作 | 实验现象 | 离子反应 | 实验结论 |
| A | 向氯化亚铁溶液中通入氯气 | 浅绿色溶液变成棕黄色溶液 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| B | 在氯化亚铁溶液中加入锌片 | 浅绿色溶液变成无色溶液 | Fe2++Zn=Fe+Zn2+ | Fe2+具有还原性 |
| C | 在氯化铁溶液中加入铁粉 | 棕黄色溶液变成浅绿色溶液 | Fe3++Fe=2Fe2+ | 铁单质具有还原性 |
| D | 在氯化铁溶液中加入铜粉 | 蓝色溶液变成棕黄色溶液 | 2Fe3++Cu=2Fe2++Cu2+ | Fe2+具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-05更新
|
475次组卷
|
6卷引用:【南昌新东方】外国语2019-2020 高一(上)期末
(已下线)【南昌新东方】外国语2019-2020 高一(上)期末江西省南昌市外国语学校2019-2020学年高一上学期期末考试化学试题鲁科版必修一2019—2020学年第三章检测试题(已下线)考点12 常见金属元素单质及其重要化合物3——铁、铜-2020年【衔接教材·暑假作业】新高三一轮复习化学(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)黑龙江省大庆市肇州县肇州中学2020-2021学年高一下学期第一次月考化学试题
2 . 亚硝酸钠( )的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
)的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
已知:
① 有强氧化性又有还原性;
有强氧化性又有还原性;
②NO能被酸性 氧化成硝酸根离子。
氧化成硝酸根离子。
某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的 。
。
反应原理为:

回答下列问题:
(1)甲装置中盛稀硝酸的仪器名称是___________ ;反应过程中观察到丙中的现象为___________ 。
(2)甲装置中发生反应的化学方程式:___________ 。
(3)甲中滴入稀硝酸前需先通入 ,原因是
,原因是___________ 。
(4)丁中酸性 的作用
的作用___________ 。
(5)人体正常的血红蛋白含有 ,但若误食亚硝酸钠,会导致血红蛋白含有的
,但若误食亚硝酸钠,会导致血红蛋白含有的 转化为
转化为 而中毒,服用维生素C可解毒。解毒时维生素C的作用是
而中毒,服用维生素C可解毒。解毒时维生素C的作用是___________ (填“还原性”或“氧化性”)。
(6)某学生将新制氯水滴加到 溶液中,观察到氯水褪色,生成
溶液中,观察到氯水褪色,生成 利HCl,写出该反应的离子方程式:
利HCl,写出该反应的离子方程式:___________ 。
 )的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。
)的外观与NaCl相似,有毒。它在工业上可作染料、助染剂,医药上能用作器碱消毒剂、防腐剂等。已知:
①
 有强氧化性又有还原性;
有强氧化性又有还原性;②NO能被酸性
 氧化成硝酸根离子。
氧化成硝酸根离子。某兴趣小组用下列装置(夹持仪器已省略)制取较纯净的
 。
。反应原理为:


回答下列问题:
(1)甲装置中盛稀硝酸的仪器名称是
(2)甲装置中发生反应的化学方程式:
(3)甲中滴入稀硝酸前需先通入
 ,原因是
,原因是(4)丁中酸性
 的作用
的作用(5)人体正常的血红蛋白含有
 ,但若误食亚硝酸钠,会导致血红蛋白含有的
,但若误食亚硝酸钠,会导致血红蛋白含有的 转化为
转化为 而中毒,服用维生素C可解毒。解毒时维生素C的作用是
而中毒,服用维生素C可解毒。解毒时维生素C的作用是(6)某学生将新制氯水滴加到
 溶液中,观察到氯水褪色,生成
溶液中,观察到氯水褪色,生成 利HCl,写出该反应的离子方程式:
利HCl,写出该反应的离子方程式:
您最近一年使用:0次
2022-03-07更新
|
391次组卷
|
3卷引用:陕西省渭南市大荔县2021-2022学年高一上学期期末考试化学试题
陕西省渭南市大荔县2021-2022学年高一上学期期末考试化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)山西省怀仁市大地中学高中部2021-2022学年高二下学期第三次月考化学试题
名校
解题方法
3 . 按要求回答下列问题:
(1)KMnO4作为强氧化剂,其氧化性随溶液的酸性增强而增大,在酸性介质中还原产物是Mn2+,在中性或碱性介质中还原产物主要是MnO2,试写出在酸性条件下氧化H2O2的离子方程式:___________ 。
(2)工业上可用KClO3溶液与Na2SO3溶液在稀H2SO4存在下制得ClO2气体,试写出该反应的离子方程式:___________ 。
(3)在强酸性混合稀土溶液中加入H2O2,可以将溶液中Ce3+氧化成Ce(OH)4沉淀得以分离,试写出该反应的离子方程式___________ 。
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:___________ 。
(1)KMnO4作为强氧化剂,其氧化性随溶液的酸性增强而增大,在酸性介质中还原产物是Mn2+,在中性或碱性介质中还原产物主要是MnO2,试写出在酸性条件下氧化H2O2的离子方程式:
(2)工业上可用KClO3溶液与Na2SO3溶液在稀H2SO4存在下制得ClO2气体,试写出该反应的离子方程式:
(3)在强酸性混合稀土溶液中加入H2O2,可以将溶液中Ce3+氧化成Ce(OH)4沉淀得以分离,试写出该反应的离子方程式
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 还原反应在工农业生产和日常生活中有广泛运用
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是___________ ;
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有___________ 。 (填“氧化性”或“还原性”);
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是___________ 。(填“氧化作用”或“还原作用”);
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是___________ ;
(5)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,生成CuCl2和FeCl2,写出离子方程式___________ 。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖(C6H12O6)提供能量以维持生命活动,反应为:C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质。此类食物防腐剂应具有
(3)铁是生物体中不可缺少的微量元素,铁在人体中是以Fe2+和Fe3+的形式存在的,而Fe2+更容易被吸收。服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中维生素C所起的作用是
(4)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式,而硫酸铁则无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是
(5)Fe3+在工业上有重要用途。例如印刷电路板是由高分子材料和铜箔复合而成,可用FeCl3溶液作“腐蚀剂”刻制印刷电路,生成CuCl2和FeCl2,写出离子方程式
您最近一年使用:0次
2024-02-29更新
|
53次组卷
|
2卷引用:海南省海口市第一中学2023-2024学年高一上学期期末考试化学试题(重点班)
名校
5 . 电石(成分为CaC2)中常含有硫化物,在反应时常产生有毒气体。工业上利用如下流程除去电石渣浆(含CaO)上层清液中的S2−,并制取石膏CaSO4•2 H2O。

下列说法正确的是

下列说法正确的是
| A.过程Ⅰ中的反应会使溶液的碱性增强 |
B.过程Ⅱ的离子方程式为4MnO +2S2−+10H+=4Mn(OH)2+S2O +2S2−+10H+=4Mn(OH)2+S2O +H2O +H2O |
C.将上层清液中0.1mol的S2−转化为SO ,理论上共需要0.2mol的O2 ,理论上共需要0.2mol的O2 |
D.由上述转化过程可知,氧化性:MnO >O2>S2O >O2>S2O |
您最近一年使用:0次
2023-08-04更新
|
451次组卷
|
3卷引用:专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
(已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)山东省东营市2022-2023学年高一上学期1月期末考试化学试题湖南省长沙麓山国际实验学校2023-2024学年高一上学期第二次适应性测试化学试卷
名校
解题方法
6 . 宏观辨识、微观探析和符号表征是体现化学学科特征的思维方式。某化学兴趣小组设计实验,探究离子反应及氧化还原反应的本质。
Ⅰ.离子反应
(1)向0.2mol·L-1Ba(OH)2溶液中滴入几滴酚酞溶液,装置如图。接通电源,向该溶液中滴入0.2molL-1H2SO4溶液。
①接通电源前,能说明Ba(OH)2在水中电离的实验现象为_______ 。
②随着H2SO4溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是Ba2+和OH-浓度降低,写出该反应的离子方程式_______ 。
(2)向0.2mol·L-1Ba(OH)2溶液中滴入0.1mol·L-1的盐酸,测定电导率的变化如图所示。
回答下列问题:_______ 。
②下列化学反应的离子方程式与Ba(OH)2溶液和稀盐酸反应相同的是_______ 。
A.Ba(OH)2溶液和稀硫酸 B.澄清石灰水和稀硝酸
C.NaOH溶液和NaHCO3溶液 D.浓氨水和浓盐酸
Ⅱ.氧化还原反应
(3)部分含硫物质如图所示,其中H2S和X是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。 ,其中反应①的离子方程式是
,其中反应①的离子方程式是______________ ,若欲将X转化成“安全物质”Z,使其对环境的影响最小,需加入_________ (填字母)。
a.氧化剂 b.还原剂 c.酸性物质 d.碱性物质
X转化为Z可以说明氧化还原的实质是_________ ,检验Z中阴离子的实验操作方法是_________ 。
Ⅰ.离子反应
(1)向0.2mol·L-1Ba(OH)2溶液中滴入几滴酚酞溶液,装置如图。接通电源,向该溶液中滴入0.2molL-1H2SO4溶液。
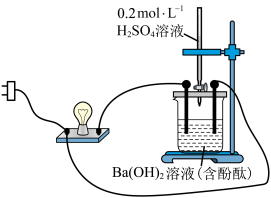
①接通电源前,能说明Ba(OH)2在水中电离的实验现象为
②随着H2SO4溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是Ba2+和OH-浓度降低,写出该反应的离子方程式
(2)向0.2mol·L-1Ba(OH)2溶液中滴入0.1mol·L-1的盐酸,测定电导率的变化如图所示。
回答下列问题:
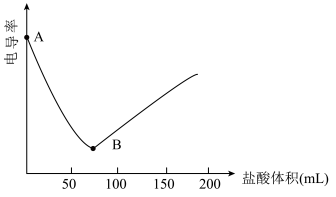
②下列化学反应的离子方程式与Ba(OH)2溶液和稀盐酸反应相同的是
A.Ba(OH)2溶液和稀硫酸 B.澄清石灰水和稀硝酸
C.NaOH溶液和NaHCO3溶液 D.浓氨水和浓盐酸
Ⅱ.氧化还原反应
(3)部分含硫物质如图所示,其中H2S和X是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。
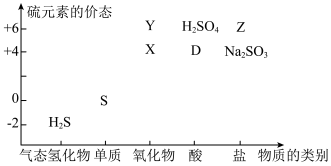
 ,其中反应①的离子方程式是
,其中反应①的离子方程式是a.氧化剂 b.还原剂 c.酸性物质 d.碱性物质
X转化为Z可以说明氧化还原的实质是
您最近一年使用:0次
2023-04-23更新
|
172次组卷
|
3卷引用:河南省南阳市2022-2023学年高一上学期1月期末考试化学试题
河南省南阳市2022-2023学年高一上学期1月期末考试化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)河南省南阳市唐河县第一高级中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
7 . NaClO、 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。
(1) 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为___________ (不考虑 的分解)。
的分解)。
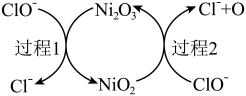
(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是___________ (填“氧化剂”或“还原剂”),当 和
和 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为___________ 。
②NaClO可在碱性条件下将 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为___________ 。
(3)以氯酸钠、硫酸和二氧化硫为原料制备 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
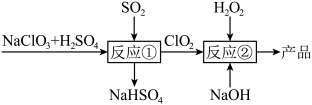
反应①的离子方程式为___________ ;理论上,该流程中参与反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。(1)
 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为 的分解)。
的分解)。(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收
 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是 和
和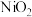 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
②NaClO可在碱性条件下将
 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为(3)以氯酸钠、硫酸和二氧化硫为原料制备
 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
反应①的离子方程式为
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
8 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再经过一系列操作可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
(1)为除去溶液中的Fe2+,可先加入______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为______ ,然后加入适量的______ ,(从下面四个选项选择)调节溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常残留在溶液中的离子浓度小于1×10-5mol∙L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol∙L-1,则Cu(OH)2开始沉淀时溶液的pH为______ , 完全沉淀时溶液的pH为
完全沉淀时溶液的pH为______ ,通过计算确定上述方案______ (填“可行”或“不可行”)。
(3)pH=6,CuSO4溶液中由水电离出的c(H+)是______ 。
(1)为除去溶液中的Fe2+,可先加入
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常残留在溶液中的离子浓度小于1×10-5mol∙L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol∙L-1,则Cu(OH)2开始沉淀时溶液的pH为
 完全沉淀时溶液的pH为
完全沉淀时溶液的pH为(3)pH=6,CuSO4溶液中由水电离出的c(H+)是
您最近一年使用:0次
2023-03-13更新
|
255次组卷
|
3卷引用:河北省石家庄市辛集市2022-2023学年高二上学期期末教学质量监测化学试题
河北省石家庄市辛集市2022-2023学年高二上学期期末教学质量监测化学试题(已下线)专题08 沉淀溶解平衡-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)河北省石家庄市西山学校2023-2024学年高二上学期期末考试化学试题
20-21高一上·全国·期末
9 . 已知反应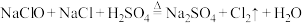 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
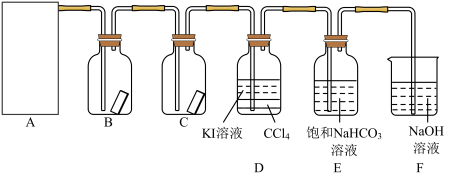
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是_______ (填字母)。
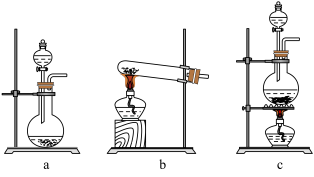
(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是_______ ,请提出合理的改进方法:_______ 。
(3)写出氯气与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ,该反应中氧化剂与还原剂的物质的量之比为_______ 。为验证尾气吸收后的溶液中存在 ,正确的操作是
,正确的操作是_______ 。
(4)氯气通入饱和 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有_______ (填化学式)。
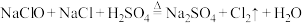 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是

(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
(3)写出氯气与
 溶液反应的离子方程式:
溶液反应的离子方程式: ,正确的操作是
,正确的操作是(4)氯气通入饱和
 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有
您最近一年使用:0次
2024-03-04更新
|
50次组卷
|
7卷引用:期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)
(已下线)期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)四川省天府新区太平中学2022-2023学年高一上学期期末考试化学试题内蒙古自治区通辽市科尔沁左翼中旗实验高级中学2023-2024学年高一上学期1月期末化学试题(已下线)第二章单元检测 (测)--2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)四川省宜宾市叙州区第二中学校2022-2023学年高一下学期开学考试化学试题安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题重庆市巫山县官渡中学2020-2021学年高一下学期第一次月考化学试题



