20-21高一上·全国·期末
1 . 已知反应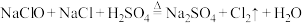 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
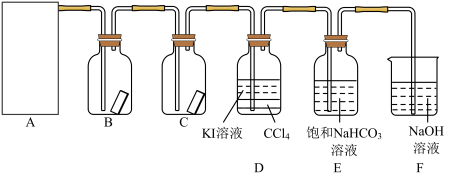
试回答下列问题:
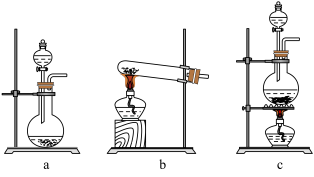
(1)在该实验中,以下可用于制取氯气的装置是_______ (填字母)。
(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是_______ ,请提出合理的改进方法:_______ 。
(3)写出氯气与 溶液反应的离子方程式:
溶液反应的离子方程式:_______ ,该反应中氧化剂与还原剂的物质的量之比为_______ 。为验证尾气吸收后的溶液中存在 ,正确的操作是
,正确的操作是_______ 。
(4)氯气通入饱和 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有_______ (填化学式)。
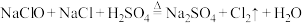 ,为探究氯气的性质,某同学设计了如图所示的实验装置。
,为探究氯气的性质,某同学设计了如图所示的实验装置。
试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是

(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
(3)写出氯气与
 溶液反应的离子方程式:
溶液反应的离子方程式: ,正确的操作是
,正确的操作是(4)氯气通入饱和
 溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明
溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验可证明 与
与 反应的产物中含有
反应的产物中含有
您最近一年使用:0次
2024-03-04更新
|
41次组卷
|
7卷引用:期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)
(已下线)期末模拟卷(一)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)四川省天府新区太平中学2022-2023学年高一上学期期末考试化学试题内蒙古自治区通辽市科尔沁左翼中旗实验高级中学2023-2024学年高一上学期1月期末化学试题(已下线)第二章单元检测 (测)--2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)四川省宜宾市叙州区第二中学校2022-2023学年高一下学期开学考试化学试题安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题重庆市巫山县官渡中学2020-2021学年高一下学期第一次月考化学试题
名校
解题方法
2 . NaClO、 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。
(1) 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为___________ (不考虑 的分解)。
的分解)。
(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是___________ (填“氧化剂”或“还原剂”),当 和
和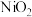 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为___________ 。
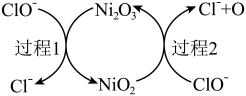
②NaClO可在碱性条件下将 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为___________ 。
(3)以氯酸钠、硫酸和二氧化硫为原料制备 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
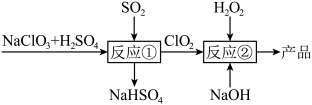
反应①的离子方程式为___________ ;理论上,该流程中参与反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
 、
、 为常见高效的消毒剂和漂白剂。
为常见高效的消毒剂和漂白剂。(1)
 是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为
是国际上公认的安全绿色消毒剂。可用氯酸钠和H2O2溶液在酸性条件下制备,反应的化学方程式为 (未配平)。该反应中
(未配平)。该反应中 与
与 的化学计量数之比为
的化学计量数之比为 的分解)。
的分解)。(2)①“84”消毒液的有效成分为NaClO。工业上常用碱性NaClO废液吸收
 ,部分催化过程如图所示。“过程1”中
,部分催化过程如图所示。“过程1”中 是
是 和
和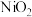 以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
以物质的量之比1∶2发生“过程2”的反应,该反应的离子方程式为
②NaClO可在碱性条件下将
 氧化为
氧化为 ,而自身被还原为NaCl,则
,而自身被还原为NaCl,则 与NaClO的个数比为
与NaClO的个数比为(3)以氯酸钠、硫酸和二氧化硫为原料制备
 ,进而再利用
,进而再利用 与
与 溶液反应制备亚氯酸钠(
溶液反应制备亚氯酸钠( ),具体流程如下:
),具体流程如下:
反应①的离子方程式为
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
3 . 化学的特征是从微观层次认识物质,以符号形式描述物质。下列反应的离子方程式书写正确的是
| 选项 | 反应 | 离子方程式 |
| A | 少量的 通入澄清石灰水中 通入澄清石灰水中 |  |
| B |  溶液中加入稀氨水 溶液中加入稀氨水 |  |
| C | 稀硫酸和氢氧化钡溶液反应 |  |
| D | 向 溶液中通入少量的 溶液中通入少量的 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
23-24高二上·北京·阶段练习
名校
解题方法
4 . 为探究 溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
(1)配制 的
的 溶液,测其
溶液,测其 约为0.7,即
约为0.7,即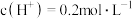 。
。
①用化学用语解释 溶液呈酸性的原因:
溶液呈酸性的原因:___________ 。
②下列实验方案中,能使 溶液
溶液 升高的是
升高的是___________ (填字母序号)。
a.加水稀释 b.加入 固体 c.滴加浓KSCN溶液 d.加入
固体 c.滴加浓KSCN溶液 d.加入 固体
固体
(2)小组同学利用上述 溶液探究其与足量锌粉的反应。实验操作及现象如表:
溶液探究其与足量锌粉的反应。实验操作及现象如表:
已知: 的性质与Al相似,能发生反应:
的性质与Al相似,能发生反应:
①红褐色沉淀是:___________ (化学式),其溶度积常数表达式Ksp=___________ ,结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:___________ 。
②用离子方程式解释反应后溶液为浅绿色的原因:___________ 。
③分离出黑色固体,经下列实验证实了其中含有的主要物质。
i.黑色固体可以被磁铁吸引;
ii.向黑色固体中加入足量的 溶液,产生气泡;
溶液,产生气泡;
iii.将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv.向iii反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是___________ 。
b.小组同学认为上述实验无法确定黑色固体中是否含有 ,理由是
,理由是___________ 。
(3)为进一步探究上述 溶液中
溶液中 和
和 氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
小组同学得出结论:在 溶液中,
溶液中, 的氧化性比
的氧化性比 更强。
更强。
 溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
溶液中的离子平衡和离子反应,某小组同学进行了如下实验。(1)配制
 的
的 溶液,测其
溶液,测其 约为0.7,即
约为0.7,即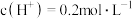 。
。①用化学用语解释
 溶液呈酸性的原因:
溶液呈酸性的原因:②下列实验方案中,能使
 溶液
溶液 升高的是
升高的是a.加水稀释 b.加入
 固体 c.滴加浓KSCN溶液 d.加入
固体 c.滴加浓KSCN溶液 d.加入 固体
固体(2)小组同学利用上述
 溶液探究其与足量锌粉的反应。实验操作及现象如表:
溶液探究其与足量锌粉的反应。实验操作及现象如表:| 操作 | 现象 |
向反应瓶中加入 锌粉,然后加入 锌粉,然后加入 的 的 溶液,搅拌 溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
 的性质与Al相似,能发生反应:
的性质与Al相似,能发生反应:
①红褐色沉淀是:
②用离子方程式解释反应后溶液为浅绿色的原因:
③分离出黑色固体,经下列实验证实了其中含有的主要物质。
i.黑色固体可以被磁铁吸引;
ii.向黑色固体中加入足量的
 溶液,产生气泡;
溶液,产生气泡;iii.将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv.向iii反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是
b.小组同学认为上述实验无法确定黑色固体中是否含有
 ,理由是
,理由是(3)为进一步探究上述
 溶液中
溶液中 和
和 氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
氧化性的相对强弱,继续实验并观察到反应开始时现象如表:| 操作 | 现象 |
将 的 的 溶液与 溶液与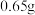 锌粉混合 锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
将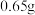 锌粉混合 锌粉混合 | 溶液中立即产生大量气泡 |
 溶液中,
溶液中, 的氧化性比
的氧化性比 更强。
更强。
您最近一年使用:0次
23-24高二上·贵州·期中
名校
5 . 镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为 、
、 及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。
及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。

已知:
① 和
和 都能与盐酸发生氧化还原反应。
都能与盐酸发生氧化还原反应。
②常温下,部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
提示:当离子浓度小于 时,认为该种离子沉淀完全。
时,认为该种离子沉淀完全。
回答下列问题:
(1)“步骤①”用稀硫酸浸取金属电极芯前,需先粉碎金属电极芯,粉碎的目的是_______________ 。常温下,0.05 的稀硫酸的pH=
的稀硫酸的pH=__________ ,若将该稀硫酸的温度升高到40℃,pH将__________ (填“增大”、“减小”或“不变”)。
(2)“步骤②”调pH的范围为__________ 。
(3)常温下, ,则m=
,则m=__________ 。
(4)“步骤④”中从环保角度分析不采用盐酸的原因是_______________________ 。
(5)“步骤⑤”制 的离子方程式为
的离子方程式为___________________________________ 。
(6) 在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[
在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[ ]。该反应的离子方程式为
]。该反应的离子方程式为______________________________________ 。
 、
、 及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。
及少量铁、铝的氧化物等]生产硫酸镍﹑碳酸钴,其工艺流程如图所示。
已知:
①
 和
和 都能与盐酸发生氧化还原反应。
都能与盐酸发生氧化还原反应。②常温下,部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
金属阳离子 |
|
|
|
|
|
|
开始沉淀时pH | 6.3 | 1.5 | 3.4 | 7.2 | — | 7.0 |
完全沉淀时pH | 8.3 | 2.8 | 4.7 | 9.1 | 1.1 | 9.0 |
 时,认为该种离子沉淀完全。
时,认为该种离子沉淀完全。回答下列问题:
(1)“步骤①”用稀硫酸浸取金属电极芯前,需先粉碎金属电极芯,粉碎的目的是
 的稀硫酸的pH=
的稀硫酸的pH=(2)“步骤②”调pH的范围为
(3)常温下,
 ,则m=
,则m=(4)“步骤④”中从环保角度分析不采用盐酸的原因是
(5)“步骤⑤”制
 的离子方程式为
的离子方程式为(6)
 在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[
在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料[ ]。该反应的离子方程式为
]。该反应的离子方程式为
您最近一年使用:0次
2023-12-05更新
|
294次组卷
|
4卷引用:期末押题卷02-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
(已下线)期末押题卷02-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)广东省清远市阳山县南阳中学2023-2024学年高二上学期第二次月考(期中)化学试题贵州省部分学校2023-2024学年高二上学期11月期中考试化学试题安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第三次月考化学试题
22-23高一上·安徽淮北·期末
名校
解题方法
6 . 下列离子方程式书写正确的是
A.氢氧化钙溶液与过量的 溶液反应: 溶液反应: |
B.将铜片插入到稀 溶液中: 溶液中: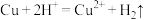 |
C.酸性 溶液中滴加 溶液中滴加 溶液: 溶液: |
D. 和 和 溶液反应至 溶液反应至 恰好沉淀: 恰好沉淀: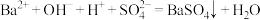 |
您最近一年使用:0次
22-23高一上·山东淄博·期末
名校
7 . 某学习小组将氯气和空气按体积比1∶3混合,通入含水 的碳酸钠中制备
的碳酸钠中制备 ,然后用水吸收
,然后用水吸收 制备次氯酸溶液。
制备次氯酸溶液。
ⅰ. 在饱和食盐水中溶解度很小,能与含水
在饱和食盐水中溶解度很小,能与含水 的碳酸钠反应生成
的碳酸钠反应生成 。
。
ⅱ. 极易溶于水生成
极易溶于水生成 ;
; 的沸点为
的沸点为 ,
, 以上分解为
以上分解为 和
和 。
。
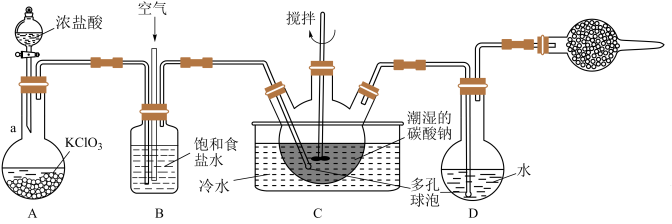
(1)仪器 的名称是
的名称是_________ ,A中发生反应的离子方程式为_________ 。
(2)实验中须控制 与空气(不参与反应)的体积比为
与空气(不参与反应)的体积比为 ,装置
,装置 的作用
的作用__________________ (答出2条即可)
(3)装置 中生成
中生成 ,反应的化学方程式为
,反应的化学方程式为__________________ 。
(4)将制得的 溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:①
溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:① 与
与 发生中和反应,②
发生中和反应,②____________ 。设计实验探究溶液红色褪去的原因___________________________ 。
(5)测定装置D中 溶液的物质的量浓度的实验方案:取
溶液的物质的量浓度的实验方案:取 溶液,加入足量
溶液,加入足量 溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为
溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为 ,则
,则 溶液的物质的量浓度为
溶液的物质的量浓度为______  (
( 可被
可被 还原成
还原成 )。
)。
 的碳酸钠中制备
的碳酸钠中制备 ,然后用水吸收
,然后用水吸收 制备次氯酸溶液。
制备次氯酸溶液。ⅰ.
 在饱和食盐水中溶解度很小,能与含水
在饱和食盐水中溶解度很小,能与含水 的碳酸钠反应生成
的碳酸钠反应生成 。
。ⅱ.
 极易溶于水生成
极易溶于水生成 ;
; 的沸点为
的沸点为 ,
, 以上分解为
以上分解为 和
和 。
。
(1)仪器
 的名称是
的名称是(2)实验中须控制
 与空气(不参与反应)的体积比为
与空气(不参与反应)的体积比为 ,装置
,装置 的作用
的作用(3)装置
 中生成
中生成 ,反应的化学方程式为
,反应的化学方程式为(4)将制得的
 溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:①
溶液加入滴有酚酞的氢氧化钠溶液中,观察到溶液红色褪去。溶液褪色的原因可能有两个:① 与
与 发生中和反应,②
发生中和反应,②(5)测定装置D中
 溶液的物质的量浓度的实验方案:取
溶液的物质的量浓度的实验方案:取 溶液,加入足量
溶液,加入足量 溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为
溶液,再加入足量硝酸银溶液,过滤,洗涤,干燥,用电子天平称量沉淀的质量为 ,则
,则 溶液的物质的量浓度为
溶液的物质的量浓度为 (
( 可被
可被 还原成
还原成 )。
)。
您最近一年使用:0次
2023-08-22更新
|
733次组卷
|
5卷引用:专题04 钠、氯及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
(已下线)专题04 钠、氯及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册) 山东省淄博实验中学2022-2023学年高一上学期期末考试化学试题黑龙江省大庆铁人中学2023-2024学年高一上学期期末考试化学试题海南省白沙学校2023-2024学年高一上学期期末考试化学试题四川省射洪中学校2023-2024学年高一(强基班)上学期第三次月考化学试题
22-23高一上·山东淄博·期末
名校
8 . 现有以下物质:①Ca(HCO3)2溶液;②CO2;③熔融Na2CO3;④NaOH;⑤SiO2;⑥Fe(OH)3胶体;⑦氨水;⑧Na2O2
(1)其中能导电的电解质:_________ (填编号,下同);属于非电解质的是:_________ 。
(2)请写出①和过量④的离子反应方程式__________________ 。
(3)利用 Fe(OH)3胶体进行下列实验:将其装入 形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带_________ 电荷(填“正”或“负”)。
(4)⑤为酸性氧化物,写出④与⑤反应的离子方程式__________________ 。
(5) Na2O2可作熔矿剂和氧化剂,则高温熔融条件下可将Cr2O3氧化为Na2CrO4,该反应的化学方程式为__________________ 。
(1)其中能导电的电解质:
(2)请写出①和过量④的离子反应方程式
(3)利用 Fe(OH)3胶体进行下列实验:将其装入
 形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带
形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带(4)⑤为酸性氧化物,写出④与⑤反应的离子方程式
(5) Na2O2可作熔矿剂和氧化剂,则高温熔融条件下可将Cr2O3氧化为Na2CrO4,该反应的化学方程式为
您最近一年使用:0次
名校
9 . 下列离子方程式的书写正确的是
A.氯气与水的反应: |
B.用稀盐酸与碳酸钙反应制取 : :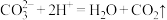 |
C.用氯化铁溶液腐蚀铜线路板: |
D.氧化铜与稀硫酸反应: |
您最近一年使用:0次
2023-08-05更新
|
334次组卷
|
5卷引用:四川省绵阳实验高级中学2022-2023学年高一上学期线上期末考试化学试题
四川省绵阳实验高级中学2022-2023学年高一上学期线上期末考试化学试题(已下线)专题02 离子反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)陕西省西安市高陵区第三中学2023-2024学年高一上学期期末化学试卷吉林省“BEST合作体”2023-2024学年高一上学期期末考试化学试题安徽省淮北市第一中学2023-2024学年高一下学期开学考试 化学试卷
10 . 下列各组离子能在溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次







