解题方法
1 . 下列方程式书写正确的是
A. 溶液中: 溶液中: |
B.小苏打与盐酸反应: |
C.往硫酸氢钠溶液中逐滴加入氢氧化钡溶液至呈中性: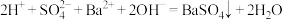 |
D.钠投入硫酸铜溶液中: |
您最近一年使用:0次
解题方法
2 . 镍、钴及其化合物在工业上有广泛的应用。以含镍废料(主要成分为NiO,含少量FeO、Fe2O3、CoO、BaO和SiO2)为原料制备NixOy,和碳酸钴(CoCO3)的工艺流程如图。
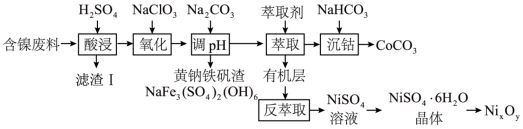
已知:Ksp[Co(OH)2]=2×10-15,请回答以下问题:
(1)“滤渣I”主要成分是___________ 。
(2)“氧化”时反应的离子方程式是___________ ,为证明添加NaClO3已足量,可用___________ (写化学式)溶液进行检验。
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为___________ 。
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+ NiX2+2H+。在萃取过程中加入适量氨水,其作用是
NiX2+2H+。在萃取过程中加入适量氨水,其作用是___________ 。“反萃取”需要往有机层中加___________ (填试剂)。
(5)若起始时c(Co2+)=0.02mol∙L-1,“沉钴”过程中应控制pH___________ (填范围)。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
由NiSO4溶液获得稳定的NiSO4•6H2O晶体的操作依次是蒸发浓缩、___________ 、过滤、洗涤、干燥。

已知:Ksp[Co(OH)2]=2×10-15,请回答以下问题:
(1)“滤渣I”主要成分是
(2)“氧化”时反应的离子方程式是
(3)“调pH”过程中生成黄钠铁钒沉淀,该反应的离子方程式为
(4)“萃取”和“反萃取”可简单表示为:2HX+Ni2+
 NiX2+2H+。在萃取过程中加入适量氨水,其作用是
NiX2+2H+。在萃取过程中加入适量氨水,其作用是(5)若起始时c(Co2+)=0.02mol∙L-1,“沉钴”过程中应控制pH
(6)资料显示,硫酸镍结晶水合物的形态与温度有如表关系。
| 温度 | 低于30.8°C | 30.8°C~53.8°C | 53.8°C~280°C | 高于280°C |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
您最近一年使用:0次
3 . 钴酸锂( )电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
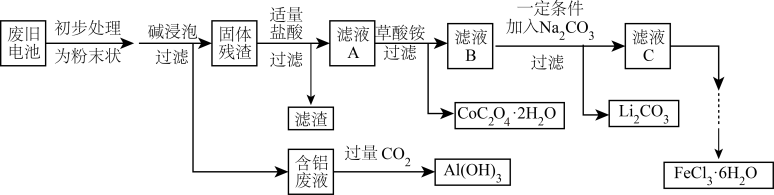
已知:①还原性: ;
;
② 和
和 结合生成较稳定的
结合生成较稳定的 ,在强酸性条件下分解重新生成
,在强酸性条件下分解重新生成 。
。
(1)基态 的简化电子排布式为
的简化电子排布式为___________ 。
(2)碱浸泡时铝转化为[Al(OH)4]- 的离子方程式为___________ 。
(3) 和HCl反应时的物质的量之比为
和HCl反应时的物质的量之比为___________ 。滤液A中的溶质除HCl、LiCl外还有___________ (填化学式)。滤渣的主要成分为___________ (填化学式)。
(4)在空气中加热一定质量的 固体样品时,其固体失重率数据见下表(其中220~300℃不发生反应),请完成300~350℃时的化学方程式。已知:
固体样品时,其固体失重率数据见下表(其中220~300℃不发生反应),请完成300~350℃时的化学方程式。已知:
① 在空气中加热时的气体产物为
在空气中加热时的气体产物为 。
。
②固体失重率=对应温度下样品失重的质量/样品的初始质量。
③ 相对分子质量为183。
相对分子质量为183。
(5)已知常温下 的溶度积常数
的溶度积常数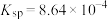 ,该温度下将浓度为0.021mol/L的
,该温度下将浓度为0.021mol/L的 和浓度为0.02mol/L的
和浓度为0.02mol/L的 溶液等体积混合,则溶液中的
溶液等体积混合,则溶液中的 浓度为
浓度为___________ mol/L。
 )电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
)电池是一种应用广泛的新型电源,电池中含有少量的铝、铁、碳等单质。实验室尝试对废旧钴酸锂电池回收再利用。实验过程如下:
已知:①还原性:
 ;
;②
 和
和 结合生成较稳定的
结合生成较稳定的 ,在强酸性条件下分解重新生成
,在强酸性条件下分解重新生成 。
。(1)基态
 的简化电子排布式为
的简化电子排布式为(2)碱浸泡时铝转化为[Al(OH)4]- 的离子方程式为
(3)
 和HCl反应时的物质的量之比为
和HCl反应时的物质的量之比为(4)在空气中加热一定质量的
 固体样品时,其固体失重率数据见下表(其中220~300℃不发生反应),请完成300~350℃时的化学方程式。已知:
固体样品时,其固体失重率数据见下表(其中220~300℃不发生反应),请完成300~350℃时的化学方程式。已知:①
 在空气中加热时的气体产物为
在空气中加热时的气体产物为 。
。②固体失重率=对应温度下样品失重的质量/样品的初始质量。
③
 相对分子质量为183。
相对分子质量为183。| 序号 | 温度范围/℃ | 化学方程式 | 固体失重率 |
| I | 120~220 | 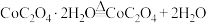 | 19.67% |
| II | 300~350 | 59.02% |
(5)已知常温下
 的溶度积常数
的溶度积常数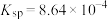 ,该温度下将浓度为0.021mol/L的
,该温度下将浓度为0.021mol/L的 和浓度为0.02mol/L的
和浓度为0.02mol/L的 溶液等体积混合,则溶液中的
溶液等体积混合,则溶液中的 浓度为
浓度为
您最近一年使用:0次
解题方法
4 . 能正确表示下列变化的离子方程式是
| A.向酸性FeCl2溶液中滴加H2O2溶液:2Fe2++H2O2+2H+=2Fe3++2H2O |
| B.向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+ |
C.将SO2通入过量氨水中:SO2+NH3∙H2O= + + |
| D.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应:Fe2++2OH-=Fe(OH)2↓ |
您最近一年使用:0次
名校
5 . 下表为八种短周期主族元素的部分性质(已知铍的原子半径为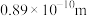 ):
):
(1)元素Z在元素周期表中的位置为_______ 。
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:_______ 。
(3)R与T相比,非金属性较强的是_______ (填元素符号),下列事实能证明这一结论的是_______ (填标号)。
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性: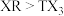
c.最高价氧化物对应水化物的酸性:
(4)J与Q相比,金属性较强的是_______ (填元素符号),能证明这一结论的依据是_______ 。
(5)根据表中数据推测,M的原子半径的最小范围是_______ 。
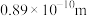 ):
):| 元素代号 | X | Y | Z | M | R | J | Q | T |
原子半径 | 0.74 | 0.75 |  | 0.99 | 1.86 | 1.43 | 1.10 | |
| 主要化合价 |  |  、 、 |  、 、 |  、 、 |  |  |  、 、 | |
| 其他 | 原子核内无中子 | 重要的半导体材料 | 有两种氧化物 |
(2)写出Q与J两种元素最高价氧化物对应的水化物之间反应的离子方程式:
(3)R与T相比,非金属性较强的是
a.常温下T的单质呈固态,R的单质呈气态
b.稳定性:
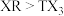
c.最高价氧化物对应水化物的酸性:

(4)J与Q相比,金属性较强的是
(5)根据表中数据推测,M的原子半径的最小范围是
您最近一年使用:0次
2024-03-20更新
|
131次组卷
|
2卷引用:江西省庐山市第一中学2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
6 . 下列离子方程式书写正确的个数是
①少量 通入
通入 溶液中:
溶液中:
② 溶于氢碘酸:
溶于氢碘酸:
③过量的铁粉在 中燃烧:
中燃烧: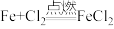
④ 溶液与等物质的量
溶液与等物质的量 反应:
反应: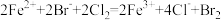
⑤向小苏打溶液中加入过量的澄清石灰水:
⑥硫酸氢钠溶液与足量氢氧化钡溶液混合:
⑦ 与
与 反应制备
反应制备 :
:
①少量
 通入
通入 溶液中:
溶液中:
②
 溶于氢碘酸:
溶于氢碘酸:
③过量的铁粉在
 中燃烧:
中燃烧: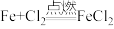
④
 溶液与等物质的量
溶液与等物质的量 反应:
反应: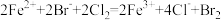
⑤向小苏打溶液中加入过量的澄清石灰水:

⑥硫酸氢钠溶液与足量氢氧化钡溶液混合:

⑦
 与
与 反应制备
反应制备 :
:
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
名校
解题方法
7 . 下列离子方程式书写正确的是
A.向 溶液中通入少量 溶液中通入少量 : : |
B.向酸性 溶液中滴加 溶液中滴加 溶液: 溶液: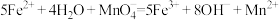 |
C. 溶液中滴加 溶液中滴加 至溶液呈中性: 至溶液呈中性: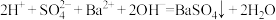 |
D.用醋酸除水垢: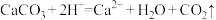 |
您最近一年使用:0次
解题方法
8 . 以冶炼铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为 (含少量杂质
(含少量杂质 、FeO、
、FeO、 ),其制备实验流程如下:(已知:
),其制备实验流程如下:(已知: 不与硫酸反应)
不与硫酸反应)

(1)写出铝灰与硫酸反应涉及的所有离子方程式______ 、______ 、______ 。
(2)图中“滤渣”的主要成分为______ (填化学式)。
(3)加30% 溶液发生的离子反应方程式为
溶液发生的离子反应方程式为____________ 。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
 ,将产生的气体通过下图所示的装置。
,将产生的气体通过下图所示的装置。

①集气瓶中收集到的气体是______ 。
②足量饱和 溶液吸收的物质除大部分
溶液吸收的物质除大部分 外还有
外还有______ 。
③ 溶液褪色(
溶液褪色(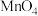 被还原为
被还原为 ),发生的离子反应方程式为
),发生的离子反应方程式为__________________ 。
 (含少量杂质
(含少量杂质 、FeO、
、FeO、 ),其制备实验流程如下:(已知:
),其制备实验流程如下:(已知: 不与硫酸反应)
不与硫酸反应)
(1)写出铝灰与硫酸反应涉及的所有离子方程式
(2)图中“滤渣”的主要成分为
(3)加30%
 溶液发生的离子反应方程式为
溶液发生的离子反应方程式为(4)煅烧硫酸铝铵晶体,发生的主要反应为:

 ,将产生的气体通过下图所示的装置。
,将产生的气体通过下图所示的装置。
①集气瓶中收集到的气体是
②足量饱和
 溶液吸收的物质除大部分
溶液吸收的物质除大部分 外还有
外还有③
 溶液褪色(
溶液褪色(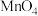 被还原为
被还原为 ),发生的离子反应方程式为
),发生的离子反应方程式为
您最近一年使用:0次
解题方法
9 . 含氯化合物的应用越来越广泛,请完成下列有关问题:
(1)亚氯酸钠( )是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为
)是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为_______ ,其水溶液显碱性的原因为_______ ,其水溶液中离子浓度由大到小的顺序为_______ 。
(2)亚氯酸钠在碱性溶液中稳定,在酸性溶液中生成 和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式
和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式_______ 。
(3) 是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为
是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为 通入
通入 中可得
中可得 ,其氧化剂与还原剂的物质的量之比为
,其氧化剂与还原剂的物质的量之比为_______ 。
(4)一定条件下, 与硫酸酸化的草酸(
与硫酸酸化的草酸( )溶液反应可制备
)溶液反应可制备 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(5) 溶液可以用来检验水溶液中的
溶液可以用来检验水溶液中的 或
或 。若向
。若向 悬浊液中加入
悬浊液中加入 溶液,可把
溶液,可把 转化为
转化为 ,已知
,已知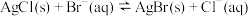 达到平衡时,
达到平衡时, ,已知
,已知 ,则
,则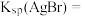
_______ 。(保留两位有效数字,不写单位)
(1)亚氯酸钠(
 )是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为
)是一种漂白织物的漂白剂,具有较强的氧化性。亚氯酸钠中氯元素的化合价为(2)亚氯酸钠在碱性溶液中稳定,在酸性溶液中生成
 和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式
和氯元素的另一种稳定离子,写出亚氯酸钠在酸性条件下反应的离子方程式(3)
 是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为
是一种新型安全多功能型杀菌剂,其制备方法有多种,其中一种为 通入
通入 中可得
中可得 ,其氧化剂与还原剂的物质的量之比为
,其氧化剂与还原剂的物质的量之比为(4)一定条件下,
 与硫酸酸化的草酸(
与硫酸酸化的草酸( )溶液反应可制备
)溶液反应可制备 ,该反应的离子方程式为
,该反应的离子方程式为(5)
 溶液可以用来检验水溶液中的
溶液可以用来检验水溶液中的 或
或 。若向
。若向 悬浊液中加入
悬浊液中加入 溶液,可把
溶液,可把 转化为
转化为 ,已知
,已知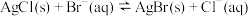 达到平衡时,
达到平衡时, ,已知
,已知 ,则
,则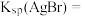
您最近一年使用:0次
解题方法
10 . 下列项目涉及反应的离子方程式错误的是
A.工程师用 腐蚀铜电路板: 腐蚀铜电路板: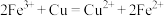 |
B.消防员使用泡沫灭火器灭火: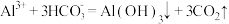 |
C.船舶工程师在船体上镶嵌锌块,防止反应: |
D.药剂师用 作抗胃酸药: 作抗胃酸药: |
您最近一年使用:0次



