1 . 化学是一门实用性很强的学科,请根据要求完成下列问题。
(1)钠有多种化合物,其中俗称“纯碱”的是___________ (填“ ”或“
”或“ ”)。
”)。
(2)铁有多种氧化物,其中为黑色且具有磁性的是___________ (填“ ”或“
”或“ ”)。
”)。
(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了___________ [填“ ”或“
”或“ ”],保护内层金属。
”],保护内层金属。
(4)铝与氢氧化钠溶液反应的离子方程式为___________ 。
(5)铁与水蒸气反应的化学方程式为___________ 。
(6)简述检验 的实验操作
的实验操作___________ 。
(1)钠有多种化合物,其中俗称“纯碱”的是
 ”或“
”或“ ”)。
”)。(2)铁有多种氧化物,其中为黑色且具有磁性的是
 ”或“
”或“ ”)。
”)。(3)日常生活中,活泼的铝在空气中能稳定存在的原因是表层的铝在空气中反应生成了
 ”或“
”或“ ”],保护内层金属。
”],保护内层金属。(4)铝与氢氧化钠溶液反应的离子方程式为
(5)铁与水蒸气反应的化学方程式为
(6)简述检验
 的实验操作
的实验操作
您最近一年使用:0次
解题方法
2 . 回答下列问题。
(1)氢氧化亚铁与氧气、水的反应方程式为:___________ 。
(2)钠通常保存在___________ 中,加热时,钠可以在空气中燃烧发出___________ 火焰,生成___________ 色固体。
(3)写出氯气和水反应的化学方程式:___________ 。
(4)电离:电解质溶于水或受热熔化时,形成___________ 的过程。
(5) 、
、 、
、 、
、 、
、 、
、 中,
中,___________ 和___________ 互为同位素,___________ 和___________ 的中子数相等,但质子数不等,所以不是同一种元素。
(6)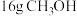 的物质的量是
的物质的量是___________ ,含H原子的数目为___________ 。
(1)氢氧化亚铁与氧气、水的反应方程式为:
(2)钠通常保存在
(3)写出氯气和水反应的化学方程式:
(4)电离:电解质溶于水或受热熔化时,形成
(5)
 、
、 、
、 、
、 、
、 、
、 中,
中,(6)
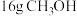 的物质的量是
的物质的量是
您最近一年使用:0次
解题方法
3 . 下列关于离子共存或离子反应的说法正确的是
A.某无色溶液中可能大量存在 、 、 、 、 、 、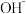 |
B.碱性的溶液中可能大量存在 、 、 、 、 、 、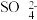 |
C.锌与稀硫酸反应: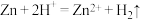 |
D.过量的硫酸氢钠与 溶液的反应: 溶液的反应: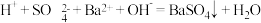 |
您最近一年使用:0次
名校
解题方法
4 . 铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4•7H2O)和氧化铝,其工艺流程如图:
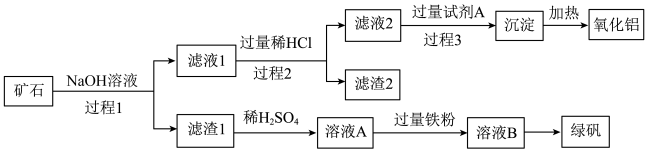
回答下列问题:
(1)滤渣1的成分是_______ ,举例说明滤渣2的用途 _______ 。
(2)用离子方程式表示溶液A加入过量铁粉的目的是_______ 。
(3)写出由滤液1生成滤液2的离子方程式_______ 。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有_______ 。
(5)过程3需要加入的试剂A是_______ ,写出此过程的离子方程式 _______ 。

回答下列问题:
(1)滤渣1的成分是
(2)用离子方程式表示溶液A加入过量铁粉的目的是
(3)写出由滤液1生成滤液2的离子方程式
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有
(5)过程3需要加入的试剂A是
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式书写错误的是
| A.石灰石与稀盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
| B.过氧化钠与稀硫酸反应:2Na2O2+4H+=4Na++O2↑+2H2O |
C.澄清石灰水与过量碳酸氢钠溶液反应:Ca2++2HCO +2OH﹣=CaCO3↓+CO +2OH﹣=CaCO3↓+CO +2H2O +2H2O |
D.氢氧化钡溶液中滴加稀硫酸:Ba2++OH﹣+H++SO =BaSO4↓+H2O =BaSO4↓+H2O |
您最近一年使用:0次
名校
6 . 铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋矿(主要成分为 ,含FeS、CuO、
,含FeS、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
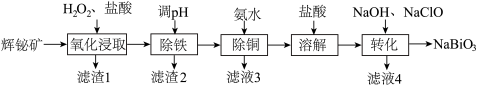
已知:
ⅰ. 难溶于冷水;滤渣1含S;
难溶于冷水;滤渣1含S;
ⅱ.“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质;
,硫元素转化为硫单质;
iii.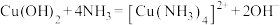 。
。
回答下列问题。
(1)“氧化浸取”步骤中温度升高可以增大速率,但高于50 ℃时浸取速率会下降,其可能的原因是_______ 。
(2)“氧化浸取”时,FeS发生反应的离子方程式为_______ 。
(3)“除铁”步骤中调节pH最好选用的试剂为_______(填字母)。
(4)“转化”时,生成 的反应中氧化剂与氧化产物的物质的量之比为
的反应中氧化剂与氧化产物的物质的量之比为_______ 。
(5) 产品纯度的测定。取
产品纯度的测定。取 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液10 mL使其完全反应(Bi被还原为+3价),再用
稀溶液10 mL使其完全反应(Bi被还原为+3价),再用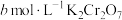 标准溶液滴定溶液中剩余的
标准溶液滴定溶液中剩余的 ,恰好消耗
,恰好消耗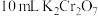 标准溶液。该产品的纯度为
标准溶液。该产品的纯度为_______ (用含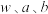 的代数式表示)。
的代数式表示)。
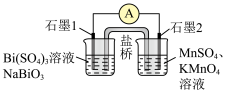
(6)组装为下图装置后发现导线中电流方向为石墨1→石墨2,则该装置的负极为_______ ,石墨2电极上的电极反应式为_______ 。
 ,含FeS、CuO、
,含FeS、CuO、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:
ⅰ.
 难溶于冷水;滤渣1含S;
难溶于冷水;滤渣1含S;ⅱ.“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质;
,硫元素转化为硫单质;iii.
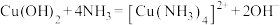 。
。回答下列问题。
(1)“氧化浸取”步骤中温度升高可以增大速率,但高于50 ℃时浸取速率会下降,其可能的原因是
(2)“氧化浸取”时,FeS发生反应的离子方程式为
(3)“除铁”步骤中调节pH最好选用的试剂为_______(填字母)。
| A.稀硫酸 | B.碳酸钠 | C.三氧化二铋 | D.氨水 |
(4)“转化”时,生成
 的反应中氧化剂与氧化产物的物质的量之比为
的反应中氧化剂与氧化产物的物质的量之比为(5)
 产品纯度的测定。取
产品纯度的测定。取 产品
产品 ,加入足量稀硫酸和
,加入足量稀硫酸和 稀溶液10 mL使其完全反应(Bi被还原为+3价),再用
稀溶液10 mL使其完全反应(Bi被还原为+3价),再用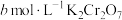 标准溶液滴定溶液中剩余的
标准溶液滴定溶液中剩余的 ,恰好消耗
,恰好消耗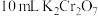 标准溶液。该产品的纯度为
标准溶液。该产品的纯度为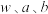 的代数式表示)。
的代数式表示)。(6)组装为下图装置后发现导线中电流方向为石墨1→石墨2,则该装置的负极为

您最近一年使用:0次
名校
解题方法
7 . 下列物质在水溶液中的电离方程式书写正确的是
A. | B. |
C. | D.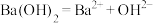 |
您最近一年使用:0次
2024-02-14更新
|
134次组卷
|
2卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
8 . 利用废铝箔(主要成分为Al,含少量Mg、Fe等)制明矾[KAl(SO4)2•12H2O]的一种工艺流程如图:

下列说法中,不正确的是

下列说法中,不正确的是
| A.①中加NaOH溶液,发生反应的离子方程式是2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ |
| B.操作a是过滤 |
C.乙溶液中含有的离子是Al3+、SO |
| D.由④可推测,室温下明矾的溶解度小于Al2(SO4)3和K2SO4的溶解度 |
您最近一年使用:0次
2024-02-14更新
|
155次组卷
|
3卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
9 . 下列应用及对应化学反应的离子方程式均正确的是
A.工业制取漂白粉: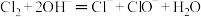 |
B.利用酸抑制 水解: 水解: |
C.用纯碱溶液处理水垢( 型): 型):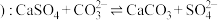 |
D.电解饱和 溶液制取金属镁: 溶液制取金属镁: |
您最近一年使用:0次
2024-02-14更新
|
148次组卷
|
2卷引用:新疆 乌鲁木齐市实验学校2023-2024学年高二上学期1月期末化学试题
名校
10 . 下列相关条件下的离子方程式书写不正确的是
A. 溶液中通入适量氯气产生沉淀: 溶液中通入适量氯气产生沉淀: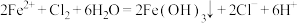 |
B.钢铁发生电化学腐蚀的负极反应: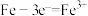 |
C.泡沫灭火器的灭火原理:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
D.氢氧酸性燃料电池的正极反应: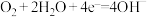 |
您最近一年使用:0次
2024-02-14更新
|
75次组卷
|
2卷引用:新疆乌鲁木齐市第101中学2023-2024学年高二上学期1月期末化学试题



