解题方法
1 . 下列能正确解释现象或事实的离子方程式是
A.向NaOH溶液中通入过量CO2: |
B.不能用排水法收集NO2: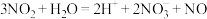 |
C.CuSO4和 反应生成沉淀: 反应生成沉淀: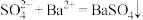 |
D.将Cu片放入稀HNO3中有气泡产生: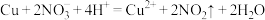 |
您最近一年使用:0次
名校
2 . 下列离子方程式不正确的是
A.石灰石与稀盐酸反应制二氧化碳: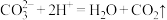 |
B.稀盐酸除去铁制品表面的铁锈: |
C.硝酸银溶液与盐酸生成白色沉淀: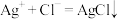 |
D.铜粉与浓硝酸生成红棕色气体: |
您最近一年使用:0次
3 . 新型绿色水处理剂高铁酸钾( )的制备方法如下图所示(部分步骤已略去)。
)的制备方法如下图所示(部分步骤已略去)。

下列说法不正确的是
 )的制备方法如下图所示(部分步骤已略去)。
)的制备方法如下图所示(部分步骤已略去)。
下列说法不正确的是
A. 中Fe元素价态为+6价 中Fe元素价态为+6价 |
B.过程I中发生 |
C.由过程Ⅱ可知,在碱性溶液中的溶解度: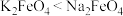 |
D. 可将氨氮废水中的 可将氨氮废水中的 转化为 转化为 除去,过程中 除去,过程中 被还原 被还原 |
您最近一年使用:0次
名校
解题方法
4 . 硫酸渣是硫酸生产过程中产生的固体废料,主要化学成分有 、
、 、
、 等。
等。
I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:
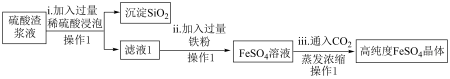
已知: 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。
(1)操作1是______ 。
(2)步骤ii中涉及反应的离子方程式有_______ 、_________ 。
(3)步骤iii中的 的作用是
的作用是______ 。
(4)取少量高纯度 晶体配成溶液,
晶体配成溶液,_______ (操作和现象),证明该晶体中不含 。
。
Ⅱ.研究人员还可利用硫酸渣与含氯废气( 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
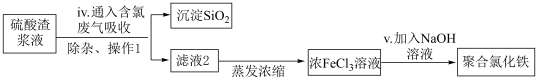
已知:聚合氯化铁的一种形式为 。
。
(5)写出以下物质中加点元素 的化合价: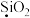
_____ ,
_____ 。
(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是___________ 。
a.盐酸中 作用是使FeO、
作用是使FeO、 溶解
溶解
b.氯气参与反应的离子方程式为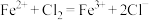
c.盐酸与氯气中的氯元素均转移到 中
中
(7)补全步骤v中涉及到反应的化学方程式______ 。
 。
。
 、
、 、
、 等。
等。I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:

已知:
 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。(1)操作1是
(2)步骤ii中涉及反应的离子方程式有
(3)步骤iii中的
 的作用是
的作用是(4)取少量高纯度
 晶体配成溶液,
晶体配成溶液, 。
。Ⅱ.研究人员还可利用硫酸渣与含氯废气(
 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
已知:聚合氯化铁的一种形式为
 。
。(5)写出以下物质中
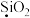

(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是
a.盐酸中
 作用是使FeO、
作用是使FeO、 溶解
溶解b.氯气参与反应的离子方程式为
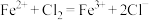
c.盐酸与氯气中的氯元素均转移到
 中
中(7)补全步骤v中涉及到反应的化学方程式
 。
。
您最近一年使用:0次
5 . 为探究  与
与  的反应,某小组同学选用三种不同的铁盐溶液(
的反应,某小组同学选用三种不同的铁盐溶液( 均约为1)进行了如下实验。
均约为1)进行了如下实验。
【查阅资料】
ⅰ.氯化亚铜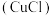 是难溶于水的白色固体。
是难溶于水的白色固体。
ⅱ. 与
与 可发生反应,生成棕色的
可发生反应,生成棕色的 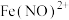 。
。
【分析解释】
(1)实验Ⅰ中发生反应的离子方程式是___________ 。
(2)为探究实验Ⅱ中白色固体的组成,小组同学设计并完成了以下实验。
步骤1:取少量洗涤后的白色固体于试管中,向其中滴加稀硝酸,观察到固体溶解,溶液变为蓝色,液面上方有少量红棕色气体生成。
步骤2:向步骤1所得溶液中滴加 溶液,生成白色沉淀。
溶液,生成白色沉淀。
①能证明实验Ⅱ白色固体中含有+1价铜的现象是___________
②步骤2中滴加 溶液的目的是
溶液的目的是___________ 。
通过以上实验,证明了实验Ⅱ中白色固体为 。
。
(3)小组同学对实验Ⅲ中的氧化剂进行了探究和分析。
①甲同学取少量棕色溶液,向其中滴加2滴 溶液,溶液变为红色,由此推断
溶液,溶液变为红色,由此推断 没有参与氧化反应。乙同学认为该推断不合理,理由是
没有参与氧化反应。乙同学认为该推断不合理,理由是___________
②乙同学认为溶液呈棕色与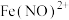 有关,
有关, 和
和 均参与了氧化反应,请设计简单实验进行验证
均参与了氧化反应,请设计简单实验进行验证___________
【反思评价】
(4)综合上述实验,说明 与
与  的反应与
的反应与___________ 等因素有关。
 与
与  的反应,某小组同学选用三种不同的铁盐溶液(
的反应,某小组同学选用三种不同的铁盐溶液( 均约为1)进行了如下实验。
均约为1)进行了如下实验。| 序号 | 实验操作 | 实验现象 |
| Ⅰ | 向盛有 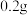 铜片的试管中加入 铜片的试管中加入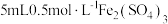 溶液 溶液 | 铜片部分溶解,溶液变为蓝色 |
| Ⅱ | 向盛有 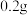 铜片的试管中加入 铜片的试管中加入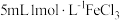 溶液 溶液 | 铜片部分溶解,溶液黄色变浅,铜片表面有白色固体出现 |
| Ⅲ | 向盛有 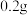 铜片的试管中加入 铜片的试管中加入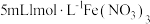 溶液 溶液 | 铜片部分溶解,溶液变为棕色,实验过程中未见气泡产生 |
ⅰ.氯化亚铜
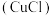 是难溶于水的白色固体。
是难溶于水的白色固体。ⅱ.
 与
与 可发生反应,生成棕色的
可发生反应,生成棕色的 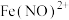 。
。【分析解释】
(1)实验Ⅰ中发生反应的离子方程式是
(2)为探究实验Ⅱ中白色固体的组成,小组同学设计并完成了以下实验。
步骤1:取少量洗涤后的白色固体于试管中,向其中滴加稀硝酸,观察到固体溶解,溶液变为蓝色,液面上方有少量红棕色气体生成。
步骤2:向步骤1所得溶液中滴加
 溶液,生成白色沉淀。
溶液,生成白色沉淀。①能证明实验Ⅱ白色固体中含有+1价铜的现象是
②步骤2中滴加
 溶液的目的是
溶液的目的是通过以上实验,证明了实验Ⅱ中白色固体为
 。
。(3)小组同学对实验Ⅲ中的氧化剂进行了探究和分析。
①甲同学取少量棕色溶液,向其中滴加2滴
 溶液,溶液变为红色,由此推断
溶液,溶液变为红色,由此推断 没有参与氧化反应。乙同学认为该推断不合理,理由是
没有参与氧化反应。乙同学认为该推断不合理,理由是②乙同学认为溶液呈棕色与
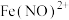 有关,
有关, 和
和 均参与了氧化反应,请设计简单实验进行验证
均参与了氧化反应,请设计简单实验进行验证【反思评价】
(4)综合上述实验,说明
 与
与  的反应与
的反应与
您最近一年使用:0次
6 . 阅读下面一段材料并回答问题。
 俗称纯碱,通常为白色粉末,易溶于水,热稳定性较强,但高温下也可以分解为
俗称纯碱,通常为白色粉末,易溶于水,热稳定性较强,但高温下也可以分解为  和
和  。
。

 有着广泛的用途。高温下可与石英砂
有着广泛的用途。高温下可与石英砂 反应生产玻璃。也可用于烟气脱硫,
反应生产玻璃。也可用于烟气脱硫, 水溶液吸收
水溶液吸收  ,再通入空气,最终可得到
,再通入空气,最终可得到  和
和 。在冶金工业中也可以与
。在冶金工业中也可以与  等金属硫化物反应,生成
等金属硫化物反应,生成 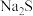 、
、 和
和  等金属氧化物。在食品工业、国防、医药等领域亦有广泛应用。
等金属氧化物。在食品工业、国防、医药等领域亦有广泛应用。
工业上有多种制备 的方法。我国化学家侯德榜先生提出了氨碱法制取
的方法。我国化学家侯德榜先生提出了氨碱法制取  和合成氨联合起来生产的工艺,可同时获得
和合成氨联合起来生产的工艺,可同时获得  和
和 两种物质,再煅烧
两种物质,再煅烧  获得
获得  ,原盐的利用率也得到了提升。侯氏制碱法对我国纯碱工业和国民经济发展做出了巨大贡献。
,原盐的利用率也得到了提升。侯氏制碱法对我国纯碱工业和国民经济发展做出了巨大贡献。
(1)根据 的性质可知它属于
的性质可知它属于___________ 类(填字母)。
a.酸 b.碱 c.盐
(2) 用于烟气脱硫发生反应的离子方程式是
用于烟气脱硫发生反应的离子方程式是___________ 。
(3)判断下列说法是否正确(填“对”或“错”)
a. 和
和  受热均易分解。
受热均易分解。___________
b. 与
与  的反应不是氧化还原反应。
的反应不是氧化还原反应。___________
c.侯氏制碱法除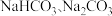 外还能获得
外还能获得  。
。___________
 俗称纯碱,通常为白色粉末,易溶于水,热稳定性较强,但高温下也可以分解为
俗称纯碱,通常为白色粉末,易溶于水,热稳定性较强,但高温下也可以分解为  和
和  。
。
 有着广泛的用途。高温下可与石英砂
有着广泛的用途。高温下可与石英砂 反应生产玻璃。也可用于烟气脱硫,
反应生产玻璃。也可用于烟气脱硫, 水溶液吸收
水溶液吸收  ,再通入空气,最终可得到
,再通入空气,最终可得到  和
和 。在冶金工业中也可以与
。在冶金工业中也可以与  等金属硫化物反应,生成
等金属硫化物反应,生成 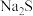 、
、 和
和  等金属氧化物。在食品工业、国防、医药等领域亦有广泛应用。
等金属氧化物。在食品工业、国防、医药等领域亦有广泛应用。工业上有多种制备
 的方法。我国化学家侯德榜先生提出了氨碱法制取
的方法。我国化学家侯德榜先生提出了氨碱法制取  和合成氨联合起来生产的工艺,可同时获得
和合成氨联合起来生产的工艺,可同时获得  和
和 两种物质,再煅烧
两种物质,再煅烧  获得
获得  ,原盐的利用率也得到了提升。侯氏制碱法对我国纯碱工业和国民经济发展做出了巨大贡献。
,原盐的利用率也得到了提升。侯氏制碱法对我国纯碱工业和国民经济发展做出了巨大贡献。(1)根据
 的性质可知它属于
的性质可知它属于a.酸 b.碱 c.盐
(2)
 用于烟气脱硫发生反应的离子方程式是
用于烟气脱硫发生反应的离子方程式是(3)判断下列说法是否正确(填“对”或“错”)
a.
 和
和  受热均易分解。
受热均易分解。b.
 与
与  的反应不是氧化还原反应。
的反应不是氧化还原反应。c.侯氏制碱法除
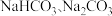 外还能获得
外还能获得  。
。
您最近一年使用:0次
解题方法
7 . 下列方程式与所给事实不相符 的是
A.铁与氯化铁溶液反应: |
B.用稀盐酸除去铁锈:  |
C.用小苏打缓解胃酸过多: |
D.铜与浓硝酸反应: |
您最近一年使用:0次
名校
8 . 用含有 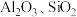 和少量
和少量 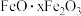 的铝灰制备
的铝灰制备  ,工艺流程如下(部分操作和条件略):
,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀 ,过滤;
,过滤;
Ⅱ.向滤液中加入过量 溶液,调节溶液的
溶液,调节溶液的  约为3,生成红褐色沉淀;
约为3,生成红褐色沉淀;
Ⅲ.静置,上层溶液呈紫红色;
Ⅳ.加入 至紫红色消失,过滤;
至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
资料: 是酸性氧化物,能与碱反应,不与酸反应。
是酸性氧化物,能与碱反应,不与酸反应。
(1) 溶解铝灰涉及的离子反应方程式有
溶解铝灰涉及的离子反应方程式有_________________ 、_________________ 。
(2)将 氧化
氧化  离子方程式补充完整:
离子方程式补充完整:_________________
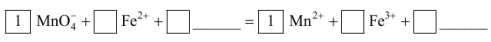
(3)已知:一定条件下, 可与
可与  反应生成
反应生成  。
。
①向Ⅲ的沉淀中加入浓 并加热,能说明沉淀中存在
并加热,能说明沉淀中存在  的现象是
的现象是_____________________________________ 。
②Ⅳ中加入 的目的是
的目的是_____________________________________ 。
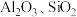 和少量
和少量 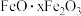 的铝灰制备
的铝灰制备  ,工艺流程如下(部分操作和条件略):
,工艺流程如下(部分操作和条件略):Ⅰ.向铝灰中加入过量稀
 ,过滤;
,过滤;Ⅱ.向滤液中加入过量
 溶液,调节溶液的
溶液,调节溶液的  约为3,生成红褐色沉淀;
约为3,生成红褐色沉淀;Ⅲ.静置,上层溶液呈紫红色;
Ⅳ.加入
 至紫红色消失,过滤;
至紫红色消失,过滤;Ⅴ.浓缩、结晶、分离,得到产品。
资料:
 是酸性氧化物,能与碱反应,不与酸反应。
是酸性氧化物,能与碱反应,不与酸反应。(1)
 溶解铝灰涉及的离子反应方程式有
溶解铝灰涉及的离子反应方程式有(2)将
 氧化
氧化  离子方程式补充完整:
离子方程式补充完整: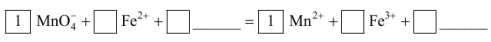
(3)已知:一定条件下,
 可与
可与  反应生成
反应生成  。
。①向Ⅲ的沉淀中加入浓
 并加热,能说明沉淀中存在
并加热,能说明沉淀中存在  的现象是
的现象是②Ⅳ中加入
 的目的是
的目的是
您最近一年使用:0次
名校
解题方法
9 . 我国是世界上最早冶炼锌的国家之一,有独立的炼锌发展史。现代炼锌主要采取湿法工艺,以闪锌矿(主要成分为 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
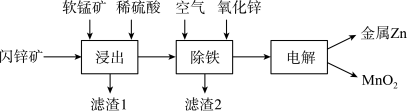
(1)浸出:加入 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:
ⅰ:
ⅱ:……
①写出ⅱ的离子方程式:_______ 。
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。
b._______ 。
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是_______ 。
(3)电解:总反应(未配平): 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子?_______ (填“ ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
 ,还含铁等元素)、软锰矿(主要成分为
,还含铁等元素)、软锰矿(主要成分为 )为原料联合生产锌和高纯度二氧化锰的一种流程如下:
)为原料联合生产锌和高纯度二氧化锰的一种流程如下:
(1)浸出:加入
 能促进
能促进 的溶解,提高锌的浸出率,同时生成硫单质。
的溶解,提高锌的浸出率,同时生成硫单质。 的作用类似催化剂,“催化”过程可表示为:
的作用类似催化剂,“催化”过程可表示为:ⅰ:

ⅱ:……
①写出ⅱ的离子方程式:
②下列实验方案可证实上述“催化”过程。将实验方案补充完整。
a.向酸化的
 溶液中加入
溶液中加入 溶液,溶液几乎无色,再加入少量
溶液,溶液几乎无色,再加入少量 ,溶液变红。
,溶液变红。b.
(2)除铁:已知①进入除铁工艺的溶液的pH约为3;②控制溶液pH为2.5~3.5,使铁主要以
 沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量
沉淀的形式除去。结合离子方程式说明,通入空气需同时补充适量 的理由是
的理由是(3)电解:总反应(未配平):
 。若不考虑副反应,为了使溶液中的
。若不考虑副反应,为了使溶液中的 、
、 均恰好完全反应,理论上需要再添加哪种离子?
均恰好完全反应,理论上需要再添加哪种离子? ”、“
”、“ ”或“都不需要”)。
”或“都不需要”)。
您最近一年使用:0次
名校
解题方法
10 . 高效净水剂高铁酸钾 制备流程如图所示,下列离子方程式正确的是
制备流程如图所示,下列离子方程式正确的是

 制备流程如图所示,下列离子方程式正确的是
制备流程如图所示,下列离子方程式正确的是
A. 净水原理: 净水原理: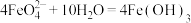 (胶体) (胶体) |
B.用 溶液吸收尾气 溶液吸收尾气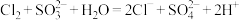 |
C.反应Ⅱ: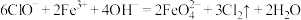 |
D.反应Ⅲ: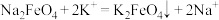 |
您最近一年使用:0次



