解题方法
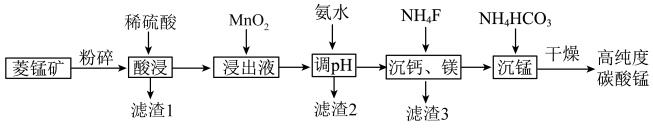
1 . 碳酸钛用作脱硫的催化剂,瓷釉、涂料和清漆的颜料,是合成二氧化锰和制造其他锰盐的原料。工业上制备高纯度碳酸锰的工艺流程如下:
②该工艺下,0.1mol/L的金属离子形成氢氧化物沉淀的pH如下:
③常温下,Ksp(CaF2)=1.60×10-10,Ksp(MgF2)=6.40×10-11.回答下列问题:
(1)基态Mn2+价电子的轨道表示式为___________ 。
(2)滤渣1的主要成份是:___________ ,其附着在矿粉颗粒表面会阻碍菱锰矿与酸的反应,若此时加入H2O2,利用其迅速分解产生的大量气泡可消除其不利影响,导致H2O2分解的因素是___________ 。
(3)在“浸出液”中加入“MnO2”所发生反应的离子方程式为___________ 。
(4)加入氨水调节溶液pH的范围___________ 。
(5)常温下,当溶液中Ca2+、Mg2+完全除去时,则c(F-)≥___________ mol/L。
(6)沉锰步骤发生主要反应的离子方程式为:___________ 。
(7)已知:5 +2Mn2++8H2O=16H++10
+2Mn2++8H2O=16H++10 +2
+2 ,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?___________ 。
②该工艺下,0.1mol/L的金属离子形成氢氧化物沉淀的pH如下:
| 金属离子Mn+ | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 1.9 | 3.4 | 7.0 | 8.1 | 9.1 |
| 沉淀完全的pH[c(Mn2+)≤1.0×10-5mol/L] | 3.2 | 4.7 | 9.0 | 10.1 | 11.1 |
(1)基态Mn2+价电子的轨道表示式为
(2)滤渣1的主要成份是:
(3)在“浸出液”中加入“MnO2”所发生反应的离子方程式为
(4)加入氨水调节溶液pH的范围
(5)常温下,当溶液中Ca2+、Mg2+完全除去时,则c(F-)≥
(6)沉锰步骤发生主要反应的离子方程式为:
(7)已知:5
 +2Mn2++8H2O=16H++10
+2Mn2++8H2O=16H++10 +2
+2 ,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
您最近一年使用:0次
解题方法
2 . 宏观辨识与微观探析是化学学科核心素养之一,下列方程式不能正确解释相应事实的是
A.SO2气体通入足量NaClO溶液中:SO2+H2O+3ClO-=Cl-+ +2HClO +2HClO |
B.亚硫酸氢钠水解方程式: +H2O +H2O H2SO3+OH- H2SO3+OH- |
C.向加碘食盐(含碘酸钾)中加入碘化钾溶液和稀硫酸: +5I-+6H+=3I2+3H2O +5I-+6H+=3I2+3H2O |
| D.常用稀H2SO4和Fe2+为原料处理废旧铅酸蓄电池中的PbO2:2Fe2++PbO2+4H+=2Fe3++Pb2++2H2O |
您最近一年使用:0次
3 . 化学必修一人教版在检验氯离子时有如下操作:在三支试管中分别加入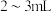 稀盐酸、NaCl溶液、Na2CO3溶液,然后各滴入几滴AgNO3溶液,观察现象;再分别加入足量稀硝酸,观察现象。回答下列问题:
稀盐酸、NaCl溶液、Na2CO3溶液,然后各滴入几滴AgNO3溶液,观察现象;再分别加入足量稀硝酸,观察现象。回答下列问题:
(1)Na2CO3的电离方程式为___________ 。
(2)滴入AgNO3溶液后三种溶液中都能观察到的现象是___________ 。
(3)在盛Na2CO3溶液的试管中,滴入几滴AgNO3溶液后,再加入足量稀硝酸的离子方程式有___________ 。
(4)某实验室暂时无Na2CO3溶液,可用___________ (填化学式)与NaHCO3溶液反应制备Na2CO3溶液。
(5)现欲配制100 mL 0.6 mol/L NaCl溶液。
①使用托盘天平称量NaCl的质量为___________ g。
②在配制过程中,下列实验操作可能导致配制的NaCl溶液浓度偏高的是___________ (填序号)。
A.定容时俯视观察容量瓶刻度线
B.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
C.往容量瓶转移时,有少量液体溅出
D.转移溶液后未洗涤烧杯
 稀盐酸、NaCl溶液、Na2CO3溶液,然后各滴入几滴AgNO3溶液,观察现象;再分别加入足量稀硝酸,观察现象。回答下列问题:
稀盐酸、NaCl溶液、Na2CO3溶液,然后各滴入几滴AgNO3溶液,观察现象;再分别加入足量稀硝酸,观察现象。回答下列问题:(1)Na2CO3的电离方程式为
(2)滴入AgNO3溶液后三种溶液中都能观察到的现象是
(3)在盛Na2CO3溶液的试管中,滴入几滴AgNO3溶液后,再加入足量稀硝酸的离子方程式有
(4)某实验室暂时无Na2CO3溶液,可用
(5)现欲配制100 mL 0.6 mol/L NaCl溶液。
①使用托盘天平称量NaCl的质量为
②在配制过程中,下列实验操作可能导致配制的NaCl溶液浓度偏高的是
A.定容时俯视观察容量瓶刻度线
B.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
C.往容量瓶转移时,有少量液体溅出
D.转移溶液后未洗涤烧杯
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式书写正确的是
A.用湿润的淀粉 试纸检验 试纸检验 : : |
B.铁粉与浓盐酸反应: |
C.将硫酸铜溶液与氢氧化钠溶液混合 |
D.等浓度等体积的 溶液与 溶液与 溶液混合: 溶液混合: |
您最近一年使用:0次
2024-02-20更新
|
164次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
5 . 下列离子方程式中,正确的是
A. 溶液中通入少量 溶液中通入少量 : : |
B. 通入石灰乳中: 通入石灰乳中: |
C.饱和 溶液中通入过量 溶液中通入过量 : : |
D.Al放入 溶液中: 溶液中: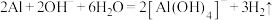 |
您最近一年使用:0次
名校
6 . 碘元素在海带中主要以I-的形式存在,加碘食盐中主要以IO 的形式存在,几种微粒之间的转化关系如图所示。下列说法中,不正确的是
的形式存在,几种微粒之间的转化关系如图所示。下列说法中,不正确的是
 的形式存在,几种微粒之间的转化关系如图所示。下列说法中,不正确的是
的形式存在,几种微粒之间的转化关系如图所示。下列说法中,不正确的是 
| A.三种途径中的转化反应均属于氧化还原反应 |
B.氧化性的强弱顺序为:Cl2>IO >I2 >I2 |
C.途径Ⅱ中发生反应的离子方程式:5HSO +2IO +2IO +2H+=I2+5HSO +2H+=I2+5HSO +H2O +H2O |
D.溶液中I-与一定量Cl2反应,生成物质的量相同的I2和IO ,则反应的I-和Cl2的物质的量的比为3:4 ,则反应的I-和Cl2的物质的量的比为3:4 |
您最近一年使用:0次
2024-02-08更新
|
60次组卷
|
2卷引用:重庆市长寿区八校联考2023-2024学年高一上学期1月期末化学试题
名校
解题方法
7 . 下列反应的离子方程式书写正确的是
A. 与 与 反应: 反应: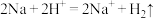 |
B.溴化亚铁溶液中加入少量 : : |
C. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
D.漂白粉溶液中通少量二氧化碳: |
您最近一年使用:0次
8 . Ⅰ.某工业废水中含有大量的 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程,回答下列问题。(提示:为充分除去杂质,所加试剂⑤和⑦均为过量)
和金属铜。请根据以下流程,回答下列问题。(提示:为充分除去杂质,所加试剂⑤和⑦均为过量)

(1)③所代表的物质是___________ (用化学式表示)。⑥和⑧中的操作方法是___________ 。
(2)向②中溶液中加入 ,观察到白色沉淀迅速变为灰绿色,最后变为红褐色,此过程中涉及的氧化还原反应的化学方程式是
,观察到白色沉淀迅速变为灰绿色,最后变为红褐色,此过程中涉及的氧化还原反应的化学方程式是___________ 。②溶液容易氧化变质,检验②溶液是否变质的操作和现象为___________ 。
II.甲、乙、丙、丁四种可溶性物质,均分别由 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的两种离子组成,四种物质中的离子各不相同,它们可以发生如下反应:
中的两种离子组成,四种物质中的离子各不相同,它们可以发生如下反应:
①甲 乙→红褐色沉淀
乙→红褐色沉淀
②甲 丙→A (白色沉淀)
丙→A (白色沉淀)
③甲 丁→B(白色沉淀)
丁→B(白色沉淀)
已知:白色沉淀A难溶于强酸
(3)丙化学式是___________ ,丁在水溶液中的电离方程式为___________ 。
(4)向三支含 甲溶液的试管中分别逐滴滴加等浓度的乙、丙、丁溶液。其溶液导电性变化如图所示的有
甲溶液的试管中分别逐滴滴加等浓度的乙、丙、丁溶液。其溶液导电性变化如图所示的有___________ 种。甲与过量的丁反应的离子方程式为___________ 。

 和较多的
和较多的 。为了减少污染并变废为宝,工厂计划从该废水中回收
。为了减少污染并变废为宝,工厂计划从该废水中回收 和金属铜。请根据以下流程,回答下列问题。(提示:为充分除去杂质,所加试剂⑤和⑦均为过量)
和金属铜。请根据以下流程,回答下列问题。(提示:为充分除去杂质,所加试剂⑤和⑦均为过量)
(1)③所代表的物质是
(2)向②中溶液中加入
 ,观察到白色沉淀迅速变为灰绿色,最后变为红褐色,此过程中涉及的氧化还原反应的化学方程式是
,观察到白色沉淀迅速变为灰绿色,最后变为红褐色,此过程中涉及的氧化还原反应的化学方程式是II.甲、乙、丙、丁四种可溶性物质,均分别由
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的两种离子组成,四种物质中的离子各不相同,它们可以发生如下反应:
中的两种离子组成,四种物质中的离子各不相同,它们可以发生如下反应:①甲
 乙→红褐色沉淀
乙→红褐色沉淀 ②甲
 丙→A (白色沉淀)
丙→A (白色沉淀) ③甲
 丁→B(白色沉淀)
丁→B(白色沉淀)已知:白色沉淀A难溶于强酸
(3)丙化学式是
(4)向三支含
 甲溶液的试管中分别逐滴滴加等浓度的乙、丙、丁溶液。其溶液导电性变化如图所示的有
甲溶液的试管中分别逐滴滴加等浓度的乙、丙、丁溶液。其溶液导电性变化如图所示的有
您最近一年使用:0次
解题方法
9 . 下列离子方程式书写正确的是
A.在沸水中滴加饱和氯化铁溶液加热: |
B.将酚酞溶液滴加到 溶液中,溶液变红色: 溶液中,溶液变红色: |
C.用饱和的 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 : :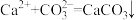 ; ; |
D.以铜为电极电解氯化钠溶液: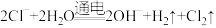 |
您最近一年使用:0次
名校
解题方法
10 . 废旧三元锂离子电池正极材料主要成分为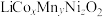 (含有铝箔、炭黑、有机物等杂质)。通过热处理、浸出、有价金属分离等过程回收钴、锰、镍、锂等金属的工艺流程如图所示:
(含有铝箔、炭黑、有机物等杂质)。通过热处理、浸出、有价金属分离等过程回收钴、锰、镍、锂等金属的工艺流程如图所示: 、
、 、
、 、
、 、
、 ;
;
②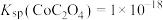 ,
,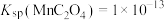 ,
,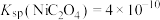
回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是__________________ 。
(2)“粉碎灼烧”的目的是____________________________________________________________ 。
(3)“碱浸”后滤液中的阴离子主要是__________________ (填化学式)。
(4)“酸浸”时加入 的目的是
的目的是____________________________________ (用离子方程式解释)。
(5)若“酸浸”后溶液中 、
、 、
、 的浓度均为
的浓度均为 ,欲使
,欲使 完全沉淀(离子浓度小于等于
完全沉淀(离子浓度小于等于 )而不使
)而不使 、
、 沉淀,需调节
沉淀,需调节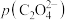 的范围为
的范围为________________________ 。[ ]
]
(6)“沉锰”时需控制溶液 ,发生反应的离子方程式为
,发生反应的离子方程式为________________________ 。
(7)对比“沉镍”“沉锂”两个步骤,若“沉镍”时只加入较高浓度 溶液即可得到
溶液即可得到 ,但最终选择加入
,但最终选择加入 和较低浓度
和较低浓度 的混合溶液的原因是
的混合溶液的原因是________________________________________________ 。
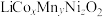 (含有铝箔、炭黑、有机物等杂质)。通过热处理、浸出、有价金属分离等过程回收钴、锰、镍、锂等金属的工艺流程如图所示:
(含有铝箔、炭黑、有机物等杂质)。通过热处理、浸出、有价金属分离等过程回收钴、锰、镍、锂等金属的工艺流程如图所示: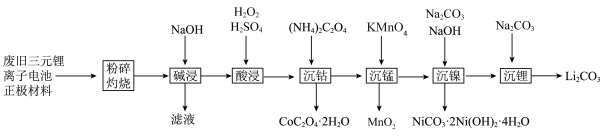
 、
、 、
、 、
、 、
、 ;
;②
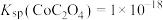 ,
,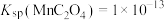 ,
,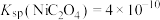
回答下列问题:
(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)“粉碎灼烧”的目的是
(3)“碱浸”后滤液中的阴离子主要是
(4)“酸浸”时加入
 的目的是
的目的是(5)若“酸浸”后溶液中
 、
、 、
、 的浓度均为
的浓度均为 ,欲使
,欲使 完全沉淀(离子浓度小于等于
完全沉淀(离子浓度小于等于 )而不使
)而不使 、
、 沉淀,需调节
沉淀,需调节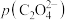 的范围为
的范围为 ]
](6)“沉锰”时需控制溶液
 ,发生反应的离子方程式为
,发生反应的离子方程式为(7)对比“沉镍”“沉锂”两个步骤,若“沉镍”时只加入较高浓度
 溶液即可得到
溶液即可得到 ,但最终选择加入
,但最终选择加入 和较低浓度
和较低浓度 的混合溶液的原因是
的混合溶液的原因是
您最近一年使用:0次
2024-01-22更新
|
270次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题



