解题方法
1 . 碱式次氯酸镁[MgmClO(OH)n·H2O]微溶于水,不潮解,相对稳定,是一种有开发价值的无机抗菌剂,以菱镁矿(MgCO3,含少量FeCO3)为主要原料,制备碱式次氯酸镁的工艺流程如下,下列说法不正确的是
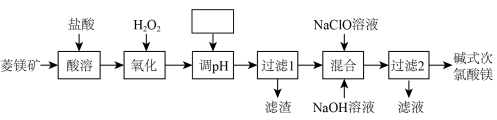
| A.流程中“酸溶”后溶液中含有Mg2+、Fe2+ |
| B.调pH时所选试剂可能是MgCO3 |
| C.“过滤1”所得的滤渣含有Fe(OH)3 |
| D.“混合”时反应的离子方程式只有Mg2++ClO-+OH-+H2O=MgClO(OH)·H2O↓ |
您最近一年使用:0次
解题方法
2 . 下列离子方程式书写正确的是
| A.Na与水反应:Na+2H2O=Na++2OH-+H2↑ |
B.过量NaOH溶液与NH4HCO3溶液反应:HC +OH-=H2O+C +OH-=H2O+C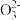 |
| C.FeO溶于稀硝酸:FeO+2H+=Fe2++H2O |
| D.向AgNO3溶液中滴加过量氨水:Ag++2NH3·H2O=[Ag(NH3)2]++2H2O |
您最近一年使用:0次
3 . (Ⅰ)有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同。
(1)①A与E形成的化合物的化学式是___________ 。
②B的最高价氧化物化学式为___________ 。
③C元素的名称为___________ 。
(2)D的单质与水反应的化学方程式为:___________ 。
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是___________ ,有关反应的离子方程式为:
___________ ,___________ 。
(Ⅱ) A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;常温下E是一种强氧化性气体。请回答:
(4)用化学符号表示上述5种微粒:A___________ ,B___________ ,C___________ ,D___________ ,E___________ 。
(5)在水溶液中A跟B反应的离子方程式是___________ 。
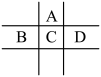
(1)①A与E形成的化合物的化学式是
②B的最高价氧化物化学式为
③C元素的名称为
(2)D的单质与水反应的化学方程式为:
(3)向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是
(Ⅱ) A、B、C、D、E分别代表5种微粒,每种微粒中都含有18个电子。其中A和C都是由单原子形成的阴离子,B、D和E都是分子;又知在水溶液中A跟B反应可生成C和D;常温下E是一种强氧化性气体。请回答:
(4)用化学符号表示上述5种微粒:A
(5)在水溶液中A跟B反应的离子方程式是
您最近一年使用:0次
4 . 下列反应的离子方程式书写正确的是
| A.将鸡蛋壳在醋酸中溶解有气泡产生:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.向CuSO4溶液中加入NaOH溶液:Cu2++2OH-=Cu(OH)2↓ |
| C.将Cu丝插入AgNO3溶液中:Cu+Ag+=Cu2++Ag |
D.向Ba(OH)2溶液中逐滴加入KHSO4溶液至溶液呈中性:H++SO +Ba2++OH-=H2O+BaSO4↓ +Ba2++OH-=H2O+BaSO4↓ |
您最近一年使用:0次
解题方法
5 . 下列反应的离子方程式书写错误的是
| A.氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
| B.稀硫酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C.氢氧化钠溶液与稀硫酸反应:H++OH-=H2O |
D.碳酸钠溶液与足量盐酸反应:2H++CO =H2O+CO2↑ =H2O+CO2↑ |
您最近一年使用:0次
解题方法
6 . 下列过程中的化学反应,相应的离子方程式正确的是
A.用醋酸处理水垢中的碳酸钙:2CH3COOH + CO = H2O + CO2↑+ 2CH3COO- = H2O + CO2↑+ 2CH3COO- |
| B.氯化铁溶液刻蚀覆铜板:2Fe3+ + Cu = 2Fe2+ +Cu2+ |
| C.硫酸铝溶液中滴加氨水:Al3+ + 3OH-= Al(OH)3↓ |
| D.氯化铜溶液中通入硫化氢:Cu2+ +S2-= CuS↓ |
您最近一年使用:0次
解题方法
7 . 下列离子方程式中,正确的是
| A.铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B.氯化铁溶液与铁反应:Fe3++Fe=2Fe2+ |
C.大理石与盐酸反应:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
D.将稀盐酸与碳酸氢钠溶液混合:HCO +H+=H2O+CO2↑ +H+=H2O+CO2↑ |
您最近一年使用:0次
8 . 现有下列10种物质:①铝,②纯碱,③CO2,④稀H2SO4,⑤Ba(OH)2固体,⑥红褐色的氢氧化铁胶体,⑦稀盐酸,⑧NaHSO4固体,⑨碳酸钙固体,⑩乙醇。
(1)上述物质中属于电解质的有___________ ,属于混合物的有___________ (填序号),属于盐的有___________ 。(填序号)
(2)写出⑧在水中的电离方程式为___________ 。
(3)少量③通入⑤的溶液中发生反应的离子反应方程式为___________ 。
(4)⑦和⑨混合反应的离子反应方程式为___________ 。
(5)④和⑤的稀溶液混合至中性时的离子方程式___________ 。
(1)上述物质中属于电解质的有
(2)写出⑧在水中的电离方程式为
(3)少量③通入⑤的溶液中发生反应的离子反应方程式为
(4)⑦和⑨混合反应的离子反应方程式为
(5)④和⑤的稀溶液混合至中性时的离子方程式
您最近一年使用:0次
9 . 化学与生活、生产息息相关。请回答下列问题:
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有______ (填序号,下同),属于非电解质的有______ 。
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为____________ 。
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为_________ 。
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式:______ 。
______C+______K2Cr2O7+______H2SO4=______K2SO4+______CO2↑+______Cr2(SO4)3+______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为______ 。
③H2SO4在上述反应中表现出来的性质是______ (填选项编号)。
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
(1)以下为中学化学中常见的几种物质:①二氧化碳;②熔融KCl;③NaHSO4固体;④铜;⑤H2SO4溶液;⑥澄清石灰水,其中属于电解质的有
(2)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。用小苏打片治疗胃酸过多的离子方程式为
(3)工业上制备漂白粉常将氯气通入冷的石灰乳中,发生反应的化学方程式为
(4)储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,发生的化学反应如下:
①配平化学方程式:
______C+______K2Cr2O7+______H2SO4=______K2SO4+______CO2↑+______Cr2(SO4)3+______H2O。
②在上述反应中生成标准状况下的11.2LCO2,转移电子数为
③H2SO4在上述反应中表现出来的性质是
A.氧化性 B.氧化性和酸性 C.酸性 D.还原性和酸性
您最近一年使用:0次
10 . 下列离子方程式书写正确的是
| A.向CaCl2溶液中通入CO2:Ca2++H2O+CO2=CaCO3↓+2H+ |
B.碳酸钡与醋酸溶液反应: +2CH3COOH=2CH3COO-+H2O+CO2↑ +2CH3COOH=2CH3COO-+H2O+CO2↑ |
| C.向氢氧化钡溶液中加入盐酸:H++OH-=H2O |
| D.氯化铝溶液中加入过量NaOH溶液:Al3++3OH-=Al(OH)3↓ |
您最近一年使用:0次



