1 . 三氯化六氨合钴(Ⅲ) 是制备其它三价钴配合物的重要试剂。实验室制备
是制备其它三价钴配合物的重要试剂。实验室制备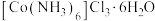 的装置如图所示,具体步骤如下:
的装置如图所示,具体步骤如下: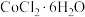 和
和 溶解后转入三颈烧瓶中,加入活性炭作催化剂和吸附剂。
溶解后转入三颈烧瓶中,加入活性炭作催化剂和吸附剂。
II.向三颈烧瓶中滴加过量氨水,充分反应后,搅拌下逐滴加入 溶液,水浴加热至50~60℃充分反应,生成的
溶液,水浴加热至50~60℃充分反应,生成的 吸附在活性炭上。
吸附在活性炭上。
III.经过“一系列”操作,得到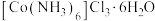 晶体。
晶体。
已知:① 不易被氧化,
不易被氧化, 具有强氧化性;
具有强氧化性; 具有较强还原性,
具有较强还原性, 性质稳定。
性质稳定。
②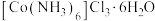 在水中的溶解度随温度的升高而增大,加入浓盐酸有利于
在水中的溶解度随温度的升高而增大,加入浓盐酸有利于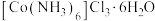 晶体析出。
晶体析出。
回答下列问题:
(1)步骤I中“溶解”需要的主要玻璃仪器为___________ , 有利于步骤II中
有利于步骤II中 与
与 的配位反应,其原理是
的配位反应,其原理是___________ 。
(2)步骤II中加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为___________ ,向三颈烧瓶中先滴加氨水后滴加 溶液的原因是
溶液的原因是___________ 。
(3)稀盐酸可将吸附在活性炭上的 溶解。请补充完整步骤III的“一系列”操作:将三颈烧瓶中所得混合物过滤,向滤渣中加入
溶解。请补充完整步骤III的“一系列”操作:将三颈烧瓶中所得混合物过滤,向滤渣中加入___________ 溶解,趁热过滤,冷却后向滤液中加入少量___________ ,边加边搅拌,充分静置后过滤,用___________ 洗涤2~3次,低温干燥。(可选用试剂:稀盐酸、浓盐酸、无水乙醇)
(4)测定产品中钴的含量,进行如下实验:
称取3.5400g产品,加入足量 溶液蒸出
溶液蒸出 ,再加入稀硫酸,将
,再加入稀硫酸,将 全部转化为
全部转化为 ,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入指示剂和过量的
,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入指示剂和过量的 溶液,用
溶液,用
 标准溶液滴定至终点,消耗标准溶液12.00mL。加入的指示剂为
标准溶液滴定至终点,消耗标准溶液12.00mL。加入的指示剂为___________ ,产品中钴元素的质量分数为___________ 。(已知: 、
、 )
)
 是制备其它三价钴配合物的重要试剂。实验室制备
是制备其它三价钴配合物的重要试剂。实验室制备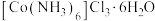 的装置如图所示,具体步骤如下:
的装置如图所示,具体步骤如下: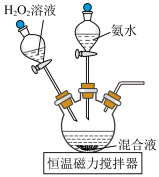
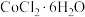 和
和 溶解后转入三颈烧瓶中,加入活性炭作催化剂和吸附剂。
溶解后转入三颈烧瓶中,加入活性炭作催化剂和吸附剂。II.向三颈烧瓶中滴加过量氨水,充分反应后,搅拌下逐滴加入
 溶液,水浴加热至50~60℃充分反应,生成的
溶液,水浴加热至50~60℃充分反应,生成的 吸附在活性炭上。
吸附在活性炭上。III.经过“一系列”操作,得到
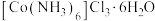 晶体。
晶体。已知:①
 不易被氧化,
不易被氧化, 具有强氧化性;
具有强氧化性; 具有较强还原性,
具有较强还原性, 性质稳定。
性质稳定。②
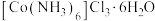 在水中的溶解度随温度的升高而增大,加入浓盐酸有利于
在水中的溶解度随温度的升高而增大,加入浓盐酸有利于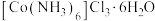 晶体析出。
晶体析出。回答下列问题:
(1)步骤I中“溶解”需要的主要玻璃仪器为
 有利于步骤II中
有利于步骤II中 与
与 的配位反应,其原理是
的配位反应,其原理是(2)步骤II中加入
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为 溶液的原因是
溶液的原因是(3)稀盐酸可将吸附在活性炭上的
 溶解。请补充完整步骤III的“一系列”操作:将三颈烧瓶中所得混合物过滤,向滤渣中加入
溶解。请补充完整步骤III的“一系列”操作:将三颈烧瓶中所得混合物过滤,向滤渣中加入(4)测定产品中钴的含量,进行如下实验:
称取3.5400g产品,加入足量
 溶液蒸出
溶液蒸出 ,再加入稀硫酸,将
,再加入稀硫酸,将 全部转化为
全部转化为 ,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入指示剂和过量的
,然后将溶液配制成250mL,取25.00mL于锥形瓶中,加入指示剂和过量的 溶液,用
溶液,用
 标准溶液滴定至终点,消耗标准溶液12.00mL。加入的指示剂为
标准溶液滴定至终点,消耗标准溶液12.00mL。加入的指示剂为 、
、 )
)
您最近一年使用:0次
解题方法
2 . 下列有关电极反应式或离子方程式正确的是
A.向氢氧化钠溶液中加入少量铝粉: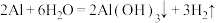 |
B.向次氯酸钙溶液通入少量二氧化碳: |
C.向 溶液中加入足量稀硝酸: 溶液中加入足量稀硝酸: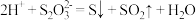 |
D.向氯化亚铁溶液中滴加氯水: |
您最近一年使用:0次
解题方法
3 . 下列离子方程式书写错误的是
| A.Cu和AgNO3溶液反应:Cu+Ag+=Cu2++Ag |
| B.石灰石溶于盐酸中:CaCO3+2H+=Ca2++CO2↑+H2O |
C.NaHCO3溶液与盐酸反应: +H+=H2O+CO2↑ +H+=H2O+CO2↑ |
| D.氧化铁与稀硫酸反应:Fe2O3+6H+=2Fe3++3H2O |
您最近一年使用:0次
4 . 下列化学方程式书写正确的是
A.少量的 通入 通入 溶液中: 溶液中: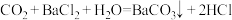 |
B.少量的NaOH溶液滴加到 溶液中: 溶液中: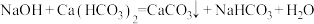 |
C.少量的KOH溶液滴加到 溶液中: 溶液中: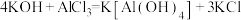 |
D.少量的稀盐酸滴加到 溶液中: 溶液中: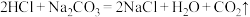 |
您最近一年使用:0次
5 . 验证次氯酸光照分解的产物可以设计成数字化实验(同时开始采集数据),此实验可以测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数的变化。三者变化趋势如图所示,回答下列问题:
(1)如图所示:
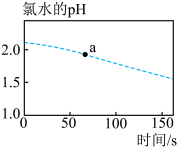
①新制氯水中所含微粒的种类有___________ 种。
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为___________ 。
③0~150s的过程中,氯水的pH逐渐减小的原因为___________ (用离子方程式表示)。
(2)如图所示:
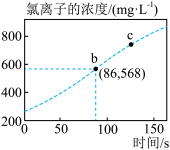
①b点对应的溶液中,所含氯离子的浓度为___________  。
。
②c点对应的溶液中,加入少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(3)如图所示:
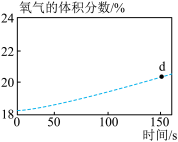
①写出一种 的用途:
的用途:___________ 。
②相同原子个数的 与
与 的质量之比为
的质量之比为___________ 。
③标准状况下,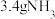 与
与___________ g 所含的电子总数相同。
所含的电子总数相同。
(1)如图所示:

①新制氯水中所含微粒的种类有
②往a点对应的溶液中滴入淀粉碘化钾溶液,可能观察到的现象为
③0~150s的过程中,氯水的pH逐渐减小的原因为
(2)如图所示:

①b点对应的溶液中,所含氯离子的浓度为
 。
。②c点对应的溶液中,加入少量的
 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为(3)如图所示:

①写出一种
 的用途:
的用途:②相同原子个数的
 与
与 的质量之比为
的质量之比为③标准状况下,
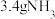 与
与 所含的电子总数相同。
所含的电子总数相同。
您最近一年使用:0次
解题方法
6 . 镁及其合金是用途很广泛的金属材料。大量的镁是从海水中提取的,从海水中提取镁的主要步骤如图所示。

回答下列问题:
(1) 在水中的电离方程式为
在水中的电离方程式为___________ 。
(2)氯化钠属于________ (填“离子”或“共价”)化合物,其形成过程可表示为_________ 。
(3) 与盐酸反应的离子方程式为
与盐酸反应的离子方程式为___________ 。
(4)在 、NaCl、NaOH的混合溶液中:
、NaCl、NaOH的混合溶液中:
①验证该混合溶液中含有 的方法及现象为
的方法及现象为___________ 。
②NaOH中存在的化学键为___________ 。
③将少量的氧化铝投入该混合溶液中,发生反应的化学方程式为___________ 。
(5)电解熔融氯化镁时,每生成1.2gMg,同时转移的电子数为____  。
。

回答下列问题:
(1)
 在水中的电离方程式为
在水中的电离方程式为(2)氯化钠属于
(3)
 与盐酸反应的离子方程式为
与盐酸反应的离子方程式为(4)在
 、NaCl、NaOH的混合溶液中:
、NaCl、NaOH的混合溶液中:①验证该混合溶液中含有
 的方法及现象为
的方法及现象为②NaOH中存在的化学键为
③将少量的氧化铝投入该混合溶液中,发生反应的化学方程式为
(5)电解熔融氯化镁时,每生成1.2gMg,同时转移的电子数为
 。
。
您最近一年使用:0次
7 . 下列反应的离子方程式中,正确的是
| A.钠与水反应:Na+2H2O=Na++2OH﹣+H2↑ |
| B.氧化铝与盐酸:O2﹣+2H+=H2O |
C.NaOH溶液与小苏打溶液反应: + OH﹣= + OH﹣= +H2O +H2O |
D.氯气通入水中:Cl2+H2O 2H++Cl﹣+ClO﹣ 2H++Cl﹣+ClO﹣ |
您最近一年使用:0次
解题方法
8 . 下图是元素①~⑤在元素周期表中的位置。
(1)⑤在周期表中的位置是第_______ 周期第_______ 族,其最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(2)③的一种核素的中子数是9,表示该核素的符号是_______ 。
(3)非金属性:④_______ ⑤(填“>”或“<”),从原子结构角度解释其原因:_______ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程_______ 。
(5)下列关于①的说法正确的是_______ (填字母)。
a.原子结构示意图为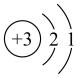
b.其单质可以和水反应生成
c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
下列说法中,正确的是_______(填字母)。
| ① | ③ | ④ | |||||
| ② | ⑤ | ||||||
(1)⑤在周期表中的位置是第
(2)③的一种核素的中子数是9,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a.原子结构示意图为

b.其单质可以和水反应生成

c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
| 实验 | ||
| 装置 | 液体a | 现象 |
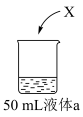 | 蒸馏水 | Ⅰ.X浮在液面上,剧烈反应,产生少量白雾 |
 盐酸 盐酸 | Ⅱ.X浮在液面上,反应比Ⅰ中剧烈,产生白雾 | |
| 浓盐酸 | Ⅲ.X浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白色固体 | |
| A.Ⅰ中现象说明X与水反应放热 |
B.Ⅱ中反应的离子方程式为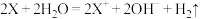 |
| C.Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多 |
D.推测Ⅲ中反应缓慢可能与 以及生成的白色固体有关 以及生成的白色固体有关 |
您最近一年使用:0次
解题方法
9 . 为研究节约资源、保护环境的路径。某化学兴趣小组利用工厂的旧金属废弃物(主要成分为 、
、 和
和 ,其他成分不溶于酸和碱)在实验室回收金属。工艺流程如图所示:
,其他成分不溶于酸和碱)在实验室回收金属。工艺流程如图所示:

回答下列问题:
(1)实验初期用 溶解废弃物时发生反应的离子方程式为
溶解废弃物时发生反应的离子方程式为___________ ,为增加溶解速率,可采取的措施有___________ (任意答一条)。
(2)固体试剂X为___________ ,操作Ⅲ为___________ (填操作名称)操作。
(3)生成固体D的离子反应方程式为___________ 。
(4)该回收流程可获得的副产品有___________ (填化学式)。
(5)下列说法正确的是___________ (填字母)。
A.实际生产中,可以用过量盐酸代替通入
B.通过类比可知固体C的成分应为
C.工业上由固体E制备Fe,常在高炉中进行
 、
、 和
和 ,其他成分不溶于酸和碱)在实验室回收金属。工艺流程如图所示:
,其他成分不溶于酸和碱)在实验室回收金属。工艺流程如图所示:
回答下列问题:
(1)实验初期用
 溶解废弃物时发生反应的离子方程式为
溶解废弃物时发生反应的离子方程式为(2)固体试剂X为
(3)生成固体D的离子反应方程式为
(4)该回收流程可获得的副产品有
(5)下列说法正确的是
A.实际生产中,可以用过量盐酸代替通入

B.通过类比可知固体C的成分应为

C.工业上由固体E制备Fe,常在高炉中进行
您最近一年使用:0次
解题方法
10 . 下列反应能发生且离子方程式书写正确的是
A.用稀硫酸溶解铜粉: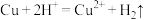 |
B.用稀盐酸除去铁锈: |
C.用三氯化铁溶液蚀刻覆铜板: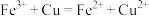 |
D.用小苏打治疗胃酸(盐酸)过多: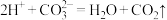 |
您最近一年使用:0次



