19-20高一·全国·期末
解题方法
1 . 下列离子方程式书写正确的是
| A.向水中通入氯气:Cl2+H2O═2H++ClO-+Cl- |
| B.向Ca(HCO3)2溶液中滴加足量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
| C.向明矾溶液中加过量氨水:Al3++4NH3⋅H2O═AlO2-+4NH4++2H2O |
| D.将Fe2O3溶解与足量HI溶液:Fe2O3+6H+═2Fe3++3H2O |
您最近一年使用:0次
19-20高一·全国·期末
解题方法
2 . 下列离子方程式书写正确的是
| A.碳酸钠溶液中滴加少量醋酸溶液:CO32-+H+=HCO3⁻ |
| B.氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| C.碳酸氢钠溶液中滴加氢氧化钡溶液:HCO3⁻+OH⁻=CO32-+H2O |
| D.氯化亚铁溶液中滴加H2O2溶液:2Fe2++H2O2+2H+=2Fe3++2H2O |
您最近一年使用:0次
19-20高一·全国·期末
解题方法
3 . 下列离子方程式表达正确的是
| A.SO2通入溴水中:SO2+2H2O+Br2=2H++SO42-+2HBr |
| B.往明矾中加入Ba(OH)2溶液,使沉淀质量最大的离子方程式为:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| C.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
您最近一年使用:0次
19-20高一·全国·期末
解题方法
4 . 下列关于离子方程式书写或说法不正确的是
| A.碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| B.向次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
| C.酸性硫酸亚铁溶液在空气中被氧化:4Fe2++O2+4H+=4Fe3++2H2O |
| D.将CO2通入饱和碳酸钠溶液中直至过量的离子方程式:2Na++CO2+CO32-+H2O=2NaHCO3↓ |
您最近一年使用:0次
19-20高一·全国·期末
解题方法
5 . 博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
铁器在具有O2、_______ 等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为Fe2+。
Ⅱ.Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为______ 。
Ⅲ..FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是_______ 。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ.Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀。
_______ Fe3O4+_____ O2+______ H2O=__________ FeO(OH)(将反应补充完整)
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5 mol/L Na2SO3、0.5 mol/L NaOH溶液的容器中,缓慢加热至60~90℃。一段时间,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是_______ 。
②脱氯反应:FeOCl+OH- =FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl 与FeO(OH)溶解度的大小:S(FeOCl)_______ S[FeO(OH)]。(填“>”、“<”、“=”)
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是___________________________ 。
(1)检测锈蚀产物
| 主要成分的化学式 | |||
| Fe3O4 | Fe2O3·H2O | FeO(OH) | FeOCl |
铁器在具有O2、
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为Fe2+。
Ⅱ.Fe2+在自然环境中形成FeO(OH),该物质中铁元素的化合价为
Ⅲ..FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ.Fe3O4保护层被氧化为FeO(OH),如此往复腐蚀。
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5 mol/L Na2SO3、0.5 mol/L NaOH溶液的容器中,缓慢加热至60~90℃。一段时间,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是
②脱氯反应:FeOCl+OH- =FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl 与FeO(OH)溶解度的大小:S(FeOCl)
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是
您最近一年使用:0次
名校
6 . 下列离子方程式或化学方程式正确的是
A. 通入少量NaClO溶液中: 通入少量NaClO溶液中: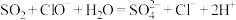 |
B.足量的 通入 通入 溶液中: 溶液中: |
C.铁与硫混合加热: |
D.浓硫酸与FeS混合: 浓 浓 |
您最近一年使用:0次
2020-02-20更新
|
420次组卷
|
5卷引用:河南省安阳市第三十五中学2016-2017学年高二下学期期末考试化学试题
河南省安阳市第三十五中学2016-2017学年高二下学期期末考试化学试题(已下线)专题01 硫及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)2020届高三化学化学二轮复习——高考常考题:与量有关的离子方程式书写【精编25题】湖北省黄梅国际育才高级中学2020-2021学年高一下学期3月月考化学试题河南省林州市第一中学2022-2023学年高二上学期开学考试化学试题
名校
解题方法
7 . 按要求回答下列问题:
(1)KMnO4作为强氧化剂,其氧化性随溶液的酸性增强而增大,在酸性介质中还原产物是Mn2+,在中性或碱性介质中还原产物主要是MnO2,试写出在酸性条件下氧化H2O2的离子方程式:___________ 。
(2)工业上可用KClO3溶液与Na2SO3溶液在稀H2SO4存在下制得ClO2气体,试写出该反应的离子方程式:___________ 。
(3)在强酸性混合稀土溶液中加入H2O2,可以将溶液中Ce3+氧化成Ce(OH)4沉淀得以分离,试写出该反应的离子方程式___________ 。
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:___________ 。
(1)KMnO4作为强氧化剂,其氧化性随溶液的酸性增强而增大,在酸性介质中还原产物是Mn2+,在中性或碱性介质中还原产物主要是MnO2,试写出在酸性条件下氧化H2O2的离子方程式:
(2)工业上可用KClO3溶液与Na2SO3溶液在稀H2SO4存在下制得ClO2气体,试写出该反应的离子方程式:
(3)在强酸性混合稀土溶液中加入H2O2,可以将溶液中Ce3+氧化成Ce(OH)4沉淀得以分离,试写出该反应的离子方程式
(4)FeCl3与KClO在强碱性条件下反应可生成K2FeO4和KCl,写出该反应的离子方程式:
您最近一年使用:0次
解题方法
8 . 下列离子方程式中,错误的是( )
| A.氢氧化钡溶液和稀硫酸反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.纯碱溶液和过量硝酸反应:CO32-+2H+=H2O+CO2↑ |
| C.硝酸银溶液与食盐水反应:Ag++Cl-=AgCl↓ |
| D.醋酸溶液与氨水反应:CH3COOH+NH3·H2O=NH4++CH3COO-+H2O |
您最近一年使用:0次
名校
解题方法
9 . 为了探究铁及其化合物的氧化性和还原性,某同学设计了如下实验方案,其中符合实验要求且完全正确的是( )
| 选项 | 实验操作 | 实验现象 | 离子反应 | 实验结论 |
| A | 向氯化亚铁溶液中通入氯气 | 浅绿色溶液变成棕黄色溶液 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| B | 在氯化亚铁溶液中加入锌片 | 浅绿色溶液变成无色溶液 | Fe2++Zn=Fe+Zn2+ | Fe2+具有还原性 |
| C | 在氯化铁溶液中加入铁粉 | 棕黄色溶液变成浅绿色溶液 | Fe3++Fe=2Fe2+ | 铁单质具有还原性 |
| D | 在氯化铁溶液中加入铜粉 | 蓝色溶液变成棕黄色溶液 | 2Fe3++Cu=2Fe2++Cu2+ | Fe2+具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-05更新
|
475次组卷
|
6卷引用:【南昌新东方】外国语2019-2020 高一(上)期末
(已下线)【南昌新东方】外国语2019-2020 高一(上)期末江西省南昌市外国语学校2019-2020学年高一上学期期末考试化学试题鲁科版必修一2019—2020学年第三章检测试题(已下线)考点12 常见金属元素单质及其重要化合物3——铁、铜-2020年【衔接教材·暑假作业】新高三一轮复习化学(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)黑龙江省大庆市肇州县肇州中学2020-2021学年高一下学期第一次月考化学试题
10 . 下列离子反应方程式正确的是( )
①碳酸氢钙溶液与过量烧碱溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O
②碳酸镁与稀硫酸:MgCO3+2H+=H2O+CO2↑+Mg2+
③醋酸与大理石:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑
④向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全:H++SO42-+Ba2++OH-=H2O+BaSO4↓
⑤向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+=CO2↑+H2O
⑥Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+=2Fe3++2H2O
①碳酸氢钙溶液与过量烧碱溶液混合:Ca2++HCO3-+OH-=CaCO3↓+H2O
②碳酸镁与稀硫酸:MgCO3+2H+=H2O+CO2↑+Mg2+
③醋酸与大理石:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑
④向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全:H++SO42-+Ba2++OH-=H2O+BaSO4↓
⑤向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+=CO2↑+H2O
⑥Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+=2Fe3++2H2O
| A.①②③④⑥ | B.②③④⑥ |
| C.②③④ | D.①③④⑤ |
您最近一年使用:0次



