名校
1 . 向含有 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: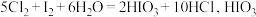 为强酸,)忽略溶液体积的改变,下列说法中错误的是
为强酸,)忽略溶液体积的改变,下列说法中错误的是
 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: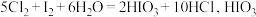 为强酸,)忽略溶液体积的改变,下列说法中错误的是
为强酸,)忽略溶液体积的改变,下列说法中错误的是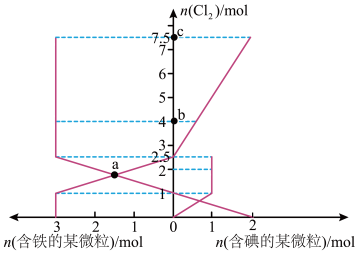
A.还原性: |
| B.b点溶液中I2物质的量为0.7mol |
C.a点时已通入标准状况下氯气的总体积为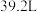 |
| D.c点溶液中阴离子的个数为17NA |
您最近一年使用:0次
2 . 根据下列实验操作和现象所得出的结论或解释一定正确的是
| 选项 | 实验操作和现象 | 结论或解释 |
| A | 向淀粉-KI溶液中通入Cl2,再通入SO2,溶液先出现蓝色,后蓝色褪去 | 还原性:SO2>I->Cl- |
| B | 检验SO2气体中是否混有SO3(g):将气体通入Ba(NO3)2溶液,有白色沉淀生成 | 混有SO3(g) |
| C | 取少量铁与水蒸气反应后的固体于试管中,加足量稀盐酸溶解再滴加KSCN溶液,溶液未变血红色 | 固体产物中不存在三价铁 |
| D | 用大理石和盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中,出现白色沉淀 | 元素非金属性:C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-21更新
|
746次组卷
|
5卷引用:湖北省武汉市第十二中学2023-2024学年高一下学期3月月考化学试题
3 . 某学习小组通过下列装置探究MnO2与FeCl3•6H2O能否反应产生Cl2。

实验操作:点燃酒精灯,加热
实验现象:ⅰ.A中部分固体溶解,上方出现白雾
ⅱ.稍后,产生黄色气体,管壁附着黄色液滴
ⅲ.B中溶液变蓝
已知:①溴水为橙色;
②三氯化铁常温下为固体,熔点为282℃,300℃以上易升华,易溶于水。
(1)现象ⅰ中的白雾主要成分是______ (化学式)的水溶液。
(2)分析现象ⅰ和ⅱ,推测黄色气体的成分,有以下三种可能:
甲.同时存在Cl2和FeCl3 乙.FeCl3 丙.Cl2
①为检验黄色气体中是否存在氯化铁,应将黄色气体通入______ 溶液,溶液变红。黄色气体中存在氯化铁说明氯化铁具有的性质为______ 。
结论:甲或乙成立。
氯化铁可使B中溶液变蓝,反应的离子方程式是____________________ 。
②为进一步确认黄色气体中存在氯气,该小组提出以下2个方案:
Ⅰ.在A、B间增加盛有某种试剂的洗气瓶C除去FeCl3,观察到B中溶液变为蓝色。C中盛放的试剂是______ (填字母序号)
A.饱和NaHCO3溶液 B.NaOH溶液 C.饱和NaCl溶液
D.浓硫酸 E.Na2SO3溶液
Ⅱ.将B中KI—淀粉溶液替换为NaBr溶液,B中溶液呈橙色;并检验反应后不存在 。检验
。检验 的原因是
的原因是____________________ 。
选择NaBr溶液是由氧化剂氧化性的强弱决定,则 、Cl2、Br2的氧化性由强到弱的顺序为
、Cl2、Br2的氧化性由强到弱的顺序为______ 。
结论:甲成立。
(3)使用NaOH溶液处理尾气中存在的Cl2所对应的离子反应方程式为____________________ 。

实验操作:点燃酒精灯,加热
实验现象:ⅰ.A中部分固体溶解,上方出现白雾
ⅱ.稍后,产生黄色气体,管壁附着黄色液滴
ⅲ.B中溶液变蓝
已知:①溴水为橙色;
②三氯化铁常温下为固体,熔点为282℃,300℃以上易升华,易溶于水。
(1)现象ⅰ中的白雾主要成分是
(2)分析现象ⅰ和ⅱ,推测黄色气体的成分,有以下三种可能:
甲.同时存在Cl2和FeCl3 乙.FeCl3 丙.Cl2
①为检验黄色气体中是否存在氯化铁,应将黄色气体通入
结论:甲或乙成立。
氯化铁可使B中溶液变蓝,反应的离子方程式是
②为进一步确认黄色气体中存在氯气,该小组提出以下2个方案:
Ⅰ.在A、B间增加盛有某种试剂的洗气瓶C除去FeCl3,观察到B中溶液变为蓝色。C中盛放的试剂是
A.饱和NaHCO3溶液 B.NaOH溶液 C.饱和NaCl溶液
D.浓硫酸 E.Na2SO3溶液
Ⅱ.将B中KI—淀粉溶液替换为NaBr溶液,B中溶液呈橙色;并检验反应后不存在
 。检验
。检验 的原因是
的原因是选择NaBr溶液是由氧化剂氧化性的强弱决定,则
 、Cl2、Br2的氧化性由强到弱的顺序为
、Cl2、Br2的氧化性由强到弱的顺序为结论:甲成立。
(3)使用NaOH溶液处理尾气中存在的Cl2所对应的离子反应方程式为
您最近一年使用:0次
2024-03-13更新
|
130次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高一下学期3月联考化学试卷
解题方法
4 . 氧化还原反应是一类非常重要的反应.回答下列问题:
(1)按如图所示操作,充分反应后.

①Ⅰ中发生反应的离子方程式为:____________________________________ 。
②Ⅱ中溶液中观察到的现象是:____________________________________ 。
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为:____________________ 。
(2)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应: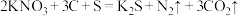 ,其中氧化产物是
,其中氧化产物是_______ .
(3)人体内的铁元素以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有_______ (填“氧化性”或“还原性”)。
(4)市场上出售的某种麦片中含有微量铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成Fe2+。用单线桥法标出该化学方程式反应电子转移数目为_____________ 。
(5)写出氢气还原氧化铜的化学方程式,用双线桥法表示电子转移的方向数目:___________________________ .
(6)在 的反应中,每有1个Fe参加反应,被还原的HNO3为
的反应中,每有1个Fe参加反应,被还原的HNO3为_______ 个。
(1)按如图所示操作,充分反应后.

①Ⅰ中发生反应的离子方程式为:
②Ⅱ中溶液中观察到的现象是:
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为:
(2)火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下反应:
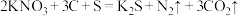 ,其中氧化产物是
,其中氧化产物是(3)人体内的铁元素以Fe2+和Fe3+的形式存在。Fe2+易被人体吸收,服用维生素C,可使Fe3+转化成Fe2+,有利于人体吸收,说明维生素C具有
(4)市场上出售的某种麦片中含有微量铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成Fe2+。用单线桥法标出该化学方程式反应电子转移数目为
(5)写出氢气还原氧化铜的化学方程式,用双线桥法表示电子转移的方向数目:
(6)在
 的反应中,每有1个Fe参加反应,被还原的HNO3为
的反应中,每有1个Fe参加反应,被还原的HNO3为
您最近一年使用:0次
名校
5 .  气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:①
溶液,发生如下反应:①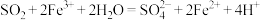 ;②
;② 。下列说法正确的是
。下列说法正确的是
 气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下反应:①
溶液,发生如下反应:①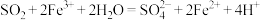 ;②
;② 。下列说法正确的是
。下列说法正确的是A.氧化性: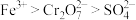 |
B.若有6.72L 完全反应,最终消耗0.2mol 完全反应,最终消耗0.2mol |
C.反应①中被还原的物质是 |
D.反应②中,1mol 参加反应,转移电子的数目为 参加反应,转移电子的数目为 |
您最近一年使用:0次
2024-02-03更新
|
164次组卷
|
3卷引用:湖北省黄冈市黄梅县晋梅高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
6 . 已知有下列四个反应:
①Cl2+2Fe2+=2Fe3++2Cl-
②
③Br2+2Fe2+=2Fe3++2Br-
④Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列有关说法正确的是
①Cl2+2Fe2+=2Fe3++2Cl-
②

③Br2+2Fe2+=2Fe3++2Br-
④Co2O3+6HCl=2CoCl2+Cl2↑+3H2O
下列有关说法正确的是
| A.反应②③④中的氧化产物分别是I2、Fe3+、CoCl2 |
| B.根据①②③可以得到还原性:I->Fe2+>Br->Cl- |
| C.不能发生反应Cl2+FeBr2=FeCl2+Br2 |
| D.在反应④中参加反应的Co2O3和体现还原性的HCl个数比为1∶6 |
您最近一年使用:0次
7 . 下列实验仪器和药品配置合理,并且能达到相对应选项中实验目的是


| A.验证碳酸钠和碳酸氢钠的稳定性 | B.验证潮湿氯气与干燥氯气的漂白性 |
| C.制备氢氧化亚铁 | D.验证氧化性顺序: |
您最近一年使用:0次
名校
解题方法
8 . PbO2、KMnO4、Cl2、FeCl3、CuCl2的氧化性依次减弱。下列反应在水溶液中不可能发生的是
| A.Cu+2Fe3+=Cu2++2Fe2+ | B.10Cl-+2MnO +16H+=2Mn2++5Cl2↑+8H2O +16H+=2Mn2++5Cl2↑+8H2O |
| C.2Fe2++Cl2=2Fe3++2Cl- | D.5Pb2++2MnO +2H2O=5PbO2+2Mn2++4H+ +2H2O=5PbO2+2Mn2++4H+ |
您最近一年使用:0次
2024-01-06更新
|
172次组卷
|
62卷引用:湖北省巴东一中2020-2021学年高一上学期第五次月考化学试题
湖北省巴东一中2020-2021学年高一上学期第五次月考化学试题湖北省襄阳市第五中学2021-2022学年高一上学期10月考试化学试题四川省石室中学2017-2018学年高一上学期半期考试化学试题湖南省衡阳县第四中学2019-2020学年高一(菁华班)10月月考化学试题辽宁省阜新市海州高级中学2019-2020学年高一10月月考化学试题黑龙江省双鸭山市第一中学2020-2021学年高一10月月考化学试题(已下线)【新东方】【2020】【高一上】【第一次月考】【JTX】【化学】河北省石家庄市辛集市第二中学2020-2021学年高一上学期10月月考化学试题山东省济南市商河县第一中学2020-2021学年高一上学期10月月考化学试题黑龙江省绥化市第一中学2020-2021学年高一上学期第二次月考化学试题四川省绵阳三台县芦溪中学2020-2021学年高一上学期第三次月考化学试题重庆实验中学2020-2021学年高一上学期第一阶段测试化学试题新疆乌鲁木齐市第八中学2019-2020学年高一上学期第二次月考化学试题北京市朝阳区中国人民大学附属中学朝阳学校2019-2020学年高一上学期10月月考化学试卷宁夏银川唐徕回民中学2021-2022学年高一11月月考化学试题河北省石家庄市第四中学2022-2023学年高一上学期10月月考化学试题湖南省怀化市中方县第一中学2022-2023学年高一上学期9月份月考化学试题广东省广州市番禺区洛城中学2022-2023学年高一上学期第一次月考化学试题宁夏石嘴山市第三中学2023-2024学年高一9月月考化学试题广东省江门市第一中学2023-2024学年高一上学期第二次段考化学试题江西省宜春市上高二中2023-2024学年高一上学期第三次月考化学试题 湖南省永州市蓝山县第二中学2023-2024学年高一上学期第三次月考化学试卷湖南省泸溪县第二中学2023-2024学年高一上学期第一次月考化学试题湖南省衡阳市耒阳市正源学校2023-2024学年高一下学期3月月考化学试题山西省大同市浑源县第七中学校2023-2024学年高一上学期第二次月考化学试题 2016届河北省冀州中学高三上学期期中测试化学试卷2016届广西钦州市钦南区高三上学期期中质量调研测试化学试卷2016-2017学年新疆生产建设兵团二中高一上期中化学卷2016-2017学年安徽省六安市第一中学高一下学期开学考试化学试卷内蒙古包头市第一中学2017-2018学年高一上学期期中考试化学试题河北省衡水市安平中学2017-2018学年高一上学期期中考试(普通班)化学试题云南省玉溪市新平县第一中学2018-2019学年高二入学分班考试化学试题【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期中考试化学试题吉林省白城市第一中学2018-2019学年高二下学期期末考试化学试题吉林省蛟河市友好学校2019-2020学年高一上学期期中联考化学试题(已下线)【新东方】高中化学5037河北省承德第一中学2019-2020学年高一上学期期中考试化学试题云南省普洱市孟连县第一中学2019—2020学年高一上学期期末考试化学试题(已下线)衔接点07 氧化剂和还原剂-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)4.2.2 氧化还原方程式的配平练习(2)——《高中新教材同步备课》(苏教版 必修第一册)人教版(2019)高一必修第一册第一章 物质及其变化 第三节 氧化还原反应 课时2 氧化剂和还原剂人教版(2019)高一必修第一册 第一章 第三节综合训练鲁科版(2019)高一必修第一册第2章 元素与物质世界 第3节 氧化还原反应 综合训练四川省江油市第一中学2020-2021学年高一上学期期中考试化学试题广东省广州市天河区广州中学2020-2021学年高一上学期期中考试化学试题吉林省辽源五中2020-2021学年高一上学期期中考试化学试题(已下线)衔接点07 氧化剂和还原剂-2021年初升高化学无忧衔接第3课时 氧化还原反应的基本规律和配平(课后)——课前、课中、课后同步专题精编(人教版2019必修第一册)广东省深圳市福田区外国语高级中学2021-2022学年高一上学期期中考试化学试题(已下线)衔接点12 氧化剂和还原剂-2022年初升高化学无忧衔接?黑龙江哈尔滨师范大学附属中学2021-2022学年高二下学期期末测试化学试题安徽省六安第一中学2022-2023学年高一上学期期中考试化学试题广东省广州市第六中学2022-2023学年高一上学期 (线上)期中考试化学试题海南省海口市第一中学2022-2023学年高一上学期期中考试化学试题江西省万载中学创新班2022-2023学年高一下学期期中考试化学试题广东省惠州市实验中学2022-2023学年高一上学期期中考试化学试题作业(六) 氧化剂和还原剂广东省江门市培英高级中学2023-2024学年高一上学期期中考试化学试题浙江省钱塘联盟2023-2024学年高一上学期期中联考化学试卷陕西省汉中市校际2023-2024学年高一上学期期中联考化学试题江西省南昌市第一中学2022-2023学年高一上学期11月期中考试化学试题四川省广安市岳池中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
9 . 下图横坐标、纵坐标分别表示一定条件下氧化剂的氧化性、还原剂的还原性由弱到强的变化,1、2、3点表示了横纵坐标对应微粒在水溶液中反应的产物,下列说法不正确的是
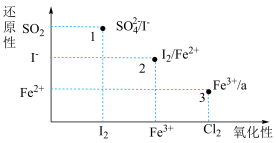
A.反应1中 为氧化产物 为氧化产物 |
B.反应2的离子方程式为: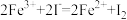 |
C.由图可知: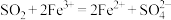 |
D.从图可推得 能氧化 能氧化 、 、 |
您最近一年使用:0次
2023-12-21更新
|
202次组卷
|
4卷引用:湖北省云学联盟2023-2024学年高一上学期12月月考化学试题
名校
10 . 高铜酸钾(KCuO2)是一种难溶于水的黑色粉末状固体(其中氧元素的化合价为-2价),与高铁酸钾(K2FeO4)性质相似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①K2[Cu(OH)4]+HBrO→KCuO2+KBr+KBrO+H2O(未配平)。高铜酸钾在酸性条件下不稳定:②KCuO2+H2SO4→O2↑+CuSO4+H2O+K2SO4(未配平)。下列说法错误的是
| A.①中还原剂和氧化剂的数量之比为2:1 |
| B.②若有32gO2生成,则生成72gH2O |
| C.②中KCuO2既表现氧化性,又表现还原性 |
| D.由①、②可知氧化性强弱顺序为HBrO>KCuO2>O2 |
您最近一年使用:0次



