名校
解题方法
1 . 某化学兴趣小组设计如图实验装置(夹持装置已省略),探究 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是__________ 。
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。
①装置A中制备 的离子方程式为
的离子方程式为__________ 。
②证明 的氧化性大于
的氧化性大于 的现象是
的现象是__________ 。
③装置C的作用是__________ ,装置D中所盛试剂为__________ (填化学式)溶液。
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。
① 发生反应的化学方程式为
发生反应的化学方程式为__________ 。
②实验完成后,打开弹簧夹,持续通入 的目的是
的目的是__________ 。
(4)淀粉 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(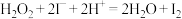 ,
, )。
)。
①滴定终点现象是__________ 。
②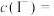
__________  。
。
 、
、 和
和 的氧化性强弱。
的氧化性强弱。
(1)玻璃管a的作用是
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞
 ,关闭活塞
,关闭活塞 ,通入
,通入 。
。①装置A中制备
 的离子方程式为
的离子方程式为②证明
 的氧化性大于
的氧化性大于 的现象是
的现象是③装置C的作用是
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞
 ,打开
,打开 ,通入
,通入 气体,验证
气体,验证 的氧化性比
的氧化性比 强。
强。①
 发生反应的化学方程式为
发生反应的化学方程式为②实验完成后,打开弹簧夹,持续通入
 的目的是
的目的是(4)淀粉
 溶液中
溶液中 的测定:取10.00mL淀粉
的测定:取10.00mL淀粉 溶液,加入足量的硫酸酸化的
溶液,加入足量的硫酸酸化的 溶液,然后加入少量的
溶液,然后加入少量的 粉末除去
粉末除去 ,然后用
,然后用 的
的 标准溶液滴定,达到滴定终点时三次测量平均消耗
标准溶液滴定,达到滴定终点时三次测量平均消耗 标准溶液的体积为25.00mL(
标准溶液的体积为25.00mL(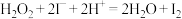 ,
, )。
)。①滴定终点现象是
②
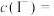
 。
。
您最近一年使用:0次
2024-04-10更新
|
197次组卷
|
3卷引用:河北省2024届普通高中高三学业水平选择性考试仿真模拟化学卷(三)
解题方法
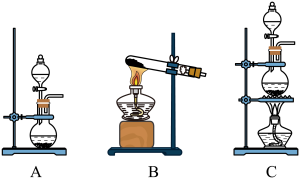
2 . 探究是创新的源泉,某化学兴趣小组进行了制备氯气并探究卤素性质的实验。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是_______ (填字母代号),该反应体现了浓盐酸的酸性和_______ (填“氧化性”或“还原性”)。
①甲中反应的离子方程式为_______ ,向反应后的橙黄色溶液中滴加 KI-淀粉溶液,溶液变为蓝色,通过上述实验_______ (填“能”或“不能”)得出氧化性:Cl2>Br2>I2。
②乙装置中 NaOH 溶液的作用为_______ ,其主要反应的化学方程式为_______ 。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是
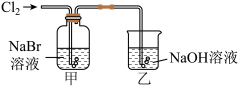
①甲中反应的离子方程式为
②乙装置中 NaOH 溶液的作用为
您最近一年使用:0次
3 . 元素在周期表中的位置,反映了元素的原子结构和性质。某学习小组以氯、溴、碘三种元素为例。通过实验探究同主族元素非金属性的递变规律,设计如下方案并进行实验。
已知:本实验条件下,溴水呈黄色,碘水呈棕黄色。
回答下列问题:
【实验I】取两支大小相同的试管,分别进行如图所示实验。

(1)A试管中溶液变为黄色,反应的离子方程式是________ ,由此证明氧化性:Cl2________ Br2(填“>”或“<”)。
(2)B试管中观察到的现象是________ ,由此证明氧化性:Cl2>I2。
【实验II】取少量A试管中的黄色溶液于另一支试管中,先加入足量KBr固体,充分振荡,再加入少量KI溶液,最后滴入几滴淀粉溶液,溶液变为蓝色。
(3)“先加入足量KBr固体”的目的:除去溶液中可能含有的________ 。
(4)上述实验证明:氯、溴、碘三种元素的非金属性由强到弱的顺序是________ 。
已知:本实验条件下,溴水呈黄色,碘水呈棕黄色。
回答下列问题:
【实验I】取两支大小相同的试管,分别进行如图所示实验。

(1)A试管中溶液变为黄色,反应的离子方程式是
(2)B试管中观察到的现象是
【实验II】取少量A试管中的黄色溶液于另一支试管中,先加入足量KBr固体,充分振荡,再加入少量KI溶液,最后滴入几滴淀粉溶液,溶液变为蓝色。
(3)“先加入足量KBr固体”的目的:除去溶液中可能含有的
(4)上述实验证明:氯、溴、碘三种元素的非金属性由强到弱的顺序是
您最近一年使用:0次
解题方法
4 . 某化学课外小组用海带为原料制取少量单质,实验流程如下:

请回答下列问题:
(1)①实验步骤Ⅰ会用到下列仪器中的_______ (填字母);
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②步骤Ⅲ所采用的分离方法是_______ (填“过滤”或“蒸馏”);
③步骤Ⅳ说明氧化性:Cl2_______ (填“>”或“<”)I2。
(2)一定条件下,工业上可利用H2和I2反应生成HI,反应的化学方程式为H2(g)+I2(g) 2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
①用I2(g)表示该反应的速率为_______ mol·L-1·min-1;
②其他条件不变时,再通入1mol H2,该反应的速率将_______ (填“增大”“不变”或“减小”)。

请回答下列问题:
(1)①实验步骤Ⅰ会用到下列仪器中的
a.酒精灯 b.漏斗 c.坩埚 d.泥三角
②步骤Ⅲ所采用的分离方法是
③步骤Ⅳ说明氧化性:Cl2
(2)一定条件下,工业上可利用H2和I2反应生成HI,反应的化学方程式为H2(g)+I2(g)
 2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:
2HI(g)。将1mol I2(g)和1mol H2置于1L的密闭容器中,10min后测得I2(g)为0.3 mol。则:①用I2(g)表示该反应的速率为
②其他条件不变时,再通入1mol H2,该反应的速率将
您最近一年使用:0次
5 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
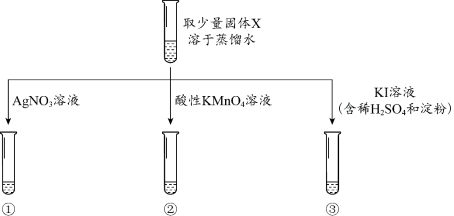
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
283次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
6 . 海水是一个巨大的化学资源宝库。实验室模拟从海水中提取溴,设计实验流程如下:
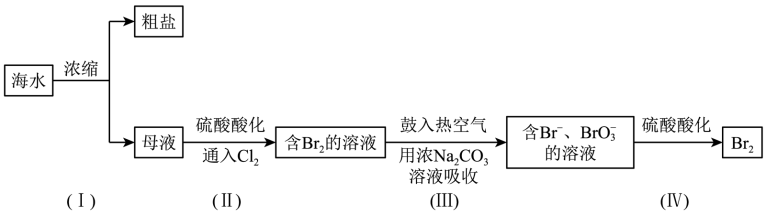
(1)海水中的溴元素存在形式是___________ (填“游离态”或“化合态”)。
(2)步骤(Ⅰ)中分离粗盐和母液的操作名称是___________ ,该操作使用的玻璃仪器有烧杯、玻璃棒和___________ 。
(3)写出步骤(Ⅱ)中 和
和 反应的离子方程式:
反应的离子方程式:___________ ,可推断氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(4)步骤(Ⅲ)中鼓入热空气可将溴单质分离出来,是利用溴单质的___________ 性。
(5)步骤(Ⅳ)中主要反应的离子方程式为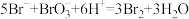 ,该反应的还原剂是
,该反应的还原剂是___________ 。

(1)海水中的溴元素存在形式是
(2)步骤(Ⅰ)中分离粗盐和母液的操作名称是
(3)写出步骤(Ⅱ)中
 和
和 反应的离子方程式:
反应的离子方程式:
 (填“>”或“<”)。
(填“>”或“<”)。(4)步骤(Ⅲ)中鼓入热空气可将溴单质分离出来,是利用溴单质的
(5)步骤(Ⅳ)中主要反应的离子方程式为
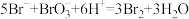 ,该反应的还原剂是
,该反应的还原剂是
您最近一年使用:0次
2022-01-01更新
|
543次组卷
|
3卷引用:2021年6月福建省普通高中学业水平合格性考试化学试题
解题方法
7 . 为验证氧化性:Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中的加热装置已略,气密性已经检验完毕)实验过程如图:
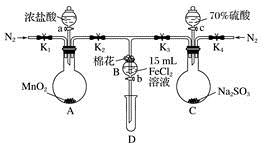
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是________________________ 。
(2)棉花中浸润的溶液为_____________ 。作用是___________________ 。
(3)A中发生反应的化学方程式:______________________________________ 。
(4)导致步骤Ⅲ中溶液变黄的离子反应是______________________________ 。用______________ (写试剂化学式)检验氧化产物,现象是____________ 。
(5)能说明氧化性Fe3+>SO2的离子方程式是__________________________ 。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是________________ (填“甲”“乙”或“丙”)。
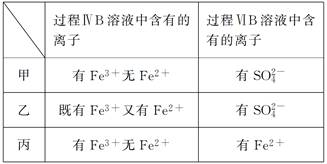

Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T形导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的阳离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)棉花中浸润的溶液为
(3)A中发生反应的化学方程式:
(4)导致步骤Ⅲ中溶液变黄的离子反应是
(5)能说明氧化性Fe3+>SO2的离子方程式是
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是

您最近一年使用:0次
2018-06-28更新
|
540次组卷
|
4卷引用:云南省西双版纳州2017-2018学年高一学年学业达标测试化学试题
13-14高一下·北京西城·期末
名校
8 . 为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
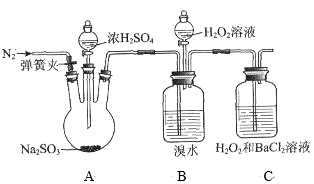
(1)A中发生反应的化学方程式是____ 。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是____ 。
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是___ 。
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是________ 。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是____ 。

| 实验操作 | 实验现象 |
| ⅰ.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ⅱ.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| ⅲ.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是
②丙同学认为还应该在B和C之间增加洗气瓶D,D中盛放的试剂是
③将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)ⅲ中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br―
观点2:B中有未反应的H2SO3
为验证观点2,应进行的实验操作及现象是
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是
您最近一年使用:0次
2016-12-09更新
|
1151次组卷
|
9卷引用:北京市2019年普通高中学业水平合格性考试模拟化学试题
北京市2019年普通高中学业水平合格性考试模拟化学试题北京市朝阳区2021-2022学年高一年级下学期合格考模拟检测化学试题(已下线)2013-2014北京市西城区下学期高一年级期末考试化学试卷(已下线)2015届河南省洛阳市高三上学期期中考试化学试卷2014-2015学年湖北省部分重点高中高二下期末考试化学试卷(已下线)北京市第四中学2016-2017学年高一下学期期中考试化学试题四川省眉山市彭山区第一中学2019-2020学年高二上学期开学考试化学试题(人教版2019)必修第二册 模块学业水平合格性测评江西省省重点校联盟2022-2023学年高二上学期入学联考化学试题
2014·北京东城·零模
名校
解题方法
9 . 某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置:(部分夹持装置已略去)

(1)写出A中反应的离子方程式________________________________________ 。
(2)B中出现黄色浑浊现象,产生此现象的离子方程式___________________________ 。
(3)试从原子结构角度解释氯的氧化性大于硫的原因____________________________________ 。
(4)D中干燥管中出现的现象及化学方程式__________________________________________ 。
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请画出其装置图______ (并注明盛装试剂)。
(6)还有什么方法能证明氧化性Cl2> S,用一种相关事实说明_____________________________ 。

(1)写出A中反应的离子方程式
(2)B中出现黄色浑浊现象,产生此现象的离子方程式
(3)试从原子结构角度解释氯的氧化性大于硫的原因
(4)D中干燥管中出现的现象及化学方程式
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,请画出其装置图
(6)还有什么方法能证明氧化性Cl2> S,用一种相关事实说明
您最近一年使用:0次
2016-12-09更新
|
661次组卷
|
7卷引用:2018届高三一轮复习化学:微考点26-氯水和常见漂白剂性质探究
2018届高三一轮复习化学:微考点26-氯水和常见漂白剂性质探究(已下线)2014届北京市东城区高三下学期零模诊断理综化学试卷(已下线)2014高考名师推荐化学化学平衡图像福建2020届高三化学总复习专题训练——化学综合实验题安徽省芜湖市2021届高三第二次月考化学试题(已下线)易错22 气体实验装置的设计-备战2021年高考化学一轮复习易错题福建省连城县第一中学2020-2021学年高一下学期第一次月考化学试题



