1 . 高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为:2Fe(OH)3 + 3ClO- + 4OH- = 2 + 3Cl- + 2H2O。下列有关说法不正确的是
+ 3Cl- + 2H2O。下列有关说法不正确的是
A.由上述反应可知,C1O- 的氧化性强于FeO |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2:3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
解题方法
2 . 下列离子方程式正确的是
| A.FeBr2溶液中通入过量氯气:2Fe2++Cl2=2Fe3++2Cl- |
| B.石灰石溶于醋酸:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O |
C.铜与浓硝酸反应:3Cu+8H++2NO =3Cu2++2NO↑+4H2O =3Cu2++2NO↑+4H2O |
D.碳酸氢铵与足量的NaOH溶液反应:HCO +OH-=CO2↑+H2O +OH-=CO2↑+H2O |
您最近一年使用:0次
名校
3 . 硫化氢(H2S)是一种无色、有臭鸡蛋气味的有毒气体。处理某废气中的 H2S,是将废气与空气混合通入 FeCl2,CuCl2、FeCl3的混合液中,其转化的流程如图所示。下列说法正确的是
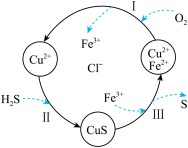

| A.转化过程中参与循环的离子只有 Cu2+、Fe2+ |
| B.转化过程有两种元素的化合价发生了变化 |
| C.氧化性由强到弱的顺序:S>Fe3+>O2 |
| D.过程Ⅲ中发生反应的离子方程式为 CuS+2Fe3+=S+2Fe2++Cu2+ |
您最近一年使用:0次
2023-11-01更新
|
456次组卷
|
12卷引用:云南会泽县实验高级中学校2023-2024学年高一上学期10月月考化学试题
云南会泽县实验高级中学校2023-2024学年高一上学期10月月考化学试题广东省清远市名校2023-2024学年高一上学期期中调研联考化学试题吉林省长春市第二实验中学2023-2024学年高一上学期期中考试化学试题安徽省阜阳市临泉第一中学2023-2024学年高一上学期10月月考化学试题安徽省合肥市第三中学2023-2024学年高一上学期12月份学情调研化学试题重庆市2021-2022学年高一上学期期末联合检测化学试题广东省广州市第五中学2022-2023学年高一上学期段考试化学试题陕西省西安市铁一中2022-2023学年高一上学期第一次月考化学试题广东省广州市第五中学2022-2023学年高一上学期期中考试化学试题湖北省麻城市实验高级中学2021-2022学年高一下学期2月迎春考化学试题四川省达州天立学校2022-2023学年高一上学期第一次月考选科摸底测试学试题【2022】【高一上】【长河高级中学】【期中考】【高中化学】
10-11高三上·福建南平·阶段练习
4 . 将 SO2气体与足量 Fe2 (SO4)3溶液完全反应后, 再加入K2Cr2O7溶液, 发生如下两个化学反应: SO2+2Fe3++2H2O= +2Fe2++4H⁺, Cr2O
+2Fe2++4H⁺, Cr2O +6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是
 +2Fe2++4H⁺, Cr2O
+2Fe2++4H⁺, Cr2O +6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是
+6Fe2++14H⁺=2Cr3++6Fe3++7H2O,有关说法正确的是A.还原性 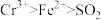 | B.氧化性  |
| C.两个反应中 Fe2(SO4)3均作还原剂 | D.Cr2O 能将 Na2SO3氧化成Na2SO4 能将 Na2SO3氧化成Na2SO4 |
您最近一年使用:0次
2023-10-17更新
|
660次组卷
|
26卷引用:云南省昆明市第八中学2023-2024学年高一上学期9月月考化学试卷题
云南省昆明市第八中学2023-2024学年高一上学期9月月考化学试卷题云南省华宁县第二中学2018-2019学年高一下学期开学考试化学试题四川省成都外国语学校2023-2024学年高一上学期10月月考化学试题宁夏回族自治区银川一中2023-2024学年高一上学期期中考试化学试题辽宁省沈阳市第十五中学2023-2024学年高一上学期10月月考化学试题陕西省安康中学2023-2024学年高一上学期10月月考化学试题四川省广安市华蓥中学2023-2024学年高一上学期12月月考化学试题重庆市黔江中学校2023-2024学年高一上学期11月月考化学试题湖南省娄底市新化县2023-2024学年高一上学期期末考试化学试题(已下线)福建省武夷山一中2011届高三上学期第一次月考物理试题江西省南康中学2017-2018学年高一上学期第三次月考化学试题河北省邢台市第一中学2017-2018学年高一下学期开学考试化学试题2018-2019学年人教版高中化学必修一:18-19 章末综合测评2 化学物质及其变化江西省南康中学2018-2019学年高一上学期第三次月考化学试题贵州省剑河县二中2018-2019学年高一上学期期末考试化学试题【校级联考】安徽省六安市毛坦厂中学、金安高级中学2018-2019学年高一上学期期末联考化学试题【全国百强校】山西省大同市第一中学2018-2019学年高二下学期期中考试化学试题步步为赢 高一化学寒假作业:作业十七 综合评估(一)江西省南康中学2019-2020学年高一上学期12月月考化学试题人教版(2019)高一必修第一册 第一章素养检测(已下线)【浙江新东方】25山东省青岛第五十八中学2020-2021学年高一上学期期中考试化学试题贵州省毕节市金沙县第一中学2020-2021学年高一上学期期末考试化学试题福建省南平市浦城县2021-2022学年高一上学期期中考试化学试题四川省遂宁市射洪中学2021-2022学年高一上学期第三次(12月)月考化学试题北京市中国人民大学附属中学2018-2019学年高一上学期期中考试化学试题
名校
解题方法
5 . 类比推理是化学中常用的思维方法。下列推理正确的是
| A.SO2、CO2是酸性氧化物,推测NO2也是酸性氧化物 |
| B.SiH4的沸点高于CH4,推测PH3的沸点高于NH3 |
| C.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3 |
| D.HCl是强酸,推测HBr也是强酸 |
您最近一年使用:0次
名校
解题方法
6 . 工业生产中除去电石渣浆(含CaO)中的S2-并制取硫酸盐的一种常用流程如图所示。下列说法正确的是


A.碱性条件下,氧化性:O2<MnO <S2O <S2O |
| B.过程 Ⅰ 中氧化剂和还原剂的物质的量之比为2∶1 |
C.过程 Ⅱ 中,反应的离子方程式为4MnO +2S2-+9H2O=S2O +2S2-+9H2O=S2O +4Mn(OH)2↓+10OH- +4Mn(OH)2↓+10OH- |
D.将1 mol S2-转化为SO 理论上需要O2的体积为22.4 L (标准状况) 理论上需要O2的体积为22.4 L (标准状况) |
您最近一年使用:0次
7 . 已知如下反应:①
②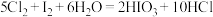
③
下列判断错误的是

②
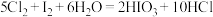
③

下列判断错误的是
| A.反应①中,HNO3起氧化作用和酸性作用 |
| B.反应①中,氧化剂与还原剂的物质的量之比为1∶8 |
| C.反应②中,每消耗1molCl2转移2mol电子 |
| D.反应③中,氧化性:Na2FeO4>NaClO |
您最近一年使用:0次
8 . 回答下列问题:
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是___________ (填元素符号),还原产物是___________ (填化学式)。
(2)K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是___________ ,若反应中发生氧化反应的HCl个数为12,则反应中转移的电子数为___________ 。
(3)下面三个方法都可以用来制氯气:
Ⅰ.4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
Ⅱ.KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
Ⅲ.KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
①反应Ⅱ中,氧化产物与还原产物的质量比为___________ 。
②已知反应Ⅳ:4HCl+O2 2Cl2+2H2O(g),该反应也能制得氯气;反应条件越简单反应越容易发生,说明性质越强烈,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气;反应条件越简单反应越容易发生,说明性质越强烈,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为___________ 。
(1)实验室制备氧气可以用加热高锰酸钾的方法实现,其发生的反应为2KMnO4
 K2MnO4+MnO2+O2↑,其中被氧化的元素是
K2MnO4+MnO2+O2↑,其中被氧化的元素是(2)K2Cr2O7+14HCl(浓)=2KCl+2CrCl3+3Cl2↑+7H2O中还原剂是
(3)下面三个方法都可以用来制氯气:
Ⅰ.4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2OⅡ.KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
Ⅲ.KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
根据以上三个反应,回答下列有关问题:
①反应Ⅱ中,氧化产物与还原产物的质量比为
②已知反应Ⅳ:4HCl+O2
 2Cl2+2H2O(g),该反应也能制得氯气;反应条件越简单反应越容易发生,说明性质越强烈,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气;反应条件越简单反应越容易发生,说明性质越强烈,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
您最近一年使用:0次
2023-07-22更新
|
162次组卷
|
2卷引用:云南省 景东彝族自治县第一中学2022-2023学年高一下学期期末考试化学试题
9 . 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 向 溶液中滴加过量氯水,再加入淀粉 溶液中滴加过量氯水,再加入淀粉 溶液 溶液 | 先变橙色,后变蓝色 | 氧化性: |
| B | 检验铁锈中是否含有二价铁 | 将铁锈溶于硫酸溶液,滴入少量 溶液,紫色褪去 溶液,紫色褪去 | 铁锈中含有二价铁 |
| C | 向蔗糖溶液中滴加稀硫酸,水浴加热加入新制的 悬浊液 悬浊液 | 无砖红色沉淀 | 蔗糖未发生水解 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . ClO2是常见的水处理剂。实验室利用以下反应制备:2KClO3+H2C2O4+H2SO4=2ClO2+K2SO4+2CO2↑+2H2O,下列说法正确的是
| A.还原性:H2C2O4大于ClO2 |
| B.KClO3 在反应中被氧化,失电子 |
| C.ClO2净水利用了ClO2的还原性 |
| D.反应中,每产生22.4 L气体,转移2 mol电子 |
您最近一年使用:0次
2023-07-11更新
|
178次组卷
|
3卷引用:云南省大理白族自治州普通高中2022-2023学年高一下学期质量监测化学试题



