名校
解题方法
1 . 下列选项描述与对应图像相符的是
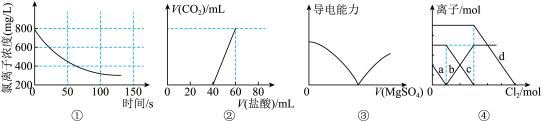
| A.图①为新制氯水在阳光直射时,溶液中Cl-浓度随着时间变化的图像 |
| B.图②为Na2CO3、NaHCO3混合液中滴加盐酸产生CO2的图像 |
| C.图③为向Ba(OH)2溶液中滴加MgSO4溶液的导电性变化图像 |
| D.图④为FeBr2、FeI2混合液中各离子物质的量随氯气通入的变化图像,曲线b代表的是Cl-(已知还原性:I->Fe2+>Br-) |
您最近一年使用:0次
2023-12-21更新
|
723次组卷
|
13卷引用:黑龙江省大庆铁人中学2023-2024学年高一上学期期中考试化学试卷
黑龙江省大庆铁人中学2023-2024学年高一上学期期中考试化学试卷黑龙江省实验中学2023-2024学年高一上学期第二次阶段测试化学试题浙江省台州市2022-2023学年高一上学期期末质量评估化学试题辽宁省东北育才学校2024届高三上学期高中学段联合考试化学试题甘肃省兰州第一中学2023-2024学年高一上学期11月期中考试化学试题吉林省吉林市第一中学2023--2024学年高一上学期第一次月考化学试题(创新班)山西省大同市2023-2024学年高一上学期12月月考化学试题吉林省延边第一中学2023-2024学年高三上学期第二次模考化学试题陕西省西安市长安区第一中学2023-2024学年高三上学期第二次教学质量检测化学试题山西省吕梁市孝义市联考2023-2024学年高一上学期12月月考化学试题北京市首都师范大学附属中学2023-2024学年高一上学期期末考试化学试题安徽省合肥市第一中学肥东分校2023-2024学年高一上学期期末考试化学试卷四川省眉山市仁寿第一中学校南校区2023-2024学年高一下学期开学化学试题
2 . 次氯酸钠具有强氧化性,强碱性溶液中可将Fe3+氧化为一种常见的高效水处理剂,离子方程式为2Fe(OH)3+3ClO−+4OH−=2FeO +3Cl−+5H2O。下列说法中
+3Cl−+5H2O。下列说法中错误 的是
 +3Cl−+5H2O。下列说法中
+3Cl−+5H2O。下列说法中| A.还原性:Fe(OH)3>Cl− |
| B.由反应可知每2molFe(OH)3完全反应时,反应中转移6mol电子 |
| C.Na2FeO4能杀菌消毒,是由于它有强氧化性 |
| D.反应中氧化剂与还原剂的物质的量之比为2:3 |
您最近一年使用:0次
2023-11-16更新
|
767次组卷
|
7卷引用:黑龙江省肇东市第四中学2023-2024学年高一上学期期末考试化学试卷
9-10高一·浙江·阶段练习
名校
解题方法
3 . 已知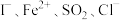 和
和 均有还原性,它们在酸性溶液中还原性的强弱顺序为
均有还原性,它们在酸性溶液中还原性的强弱顺序为 ,则下列反应不能发生的是
,则下列反应不能发生的是
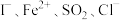 和
和 均有还原性,它们在酸性溶液中还原性的强弱顺序为
均有还原性,它们在酸性溶液中还原性的强弱顺序为 ,则下列反应不能发生的是
,则下列反应不能发生的是A. |
B. |
C. |
D.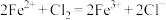 |
您最近一年使用:0次
2023-11-11更新
|
334次组卷
|
38卷引用:黑龙江省哈尔滨市第三中学校 2023-2024 学年高一上学期第一次验收考试化学试题
黑龙江省哈尔滨市第三中学校 2023-2024 学年高一上学期第一次验收考试化学试题(已下线)2010年黑龙江牡丹江一中高一上学期期中考试化学试卷黑龙江省大庆铁人中学2017-2018学年高一上学期期中考试化学试题1黑龙江省大庆铁人中学2017-2018学年高一上学期期中考试化学试题2黑龙江省大庆中学2020—2021学年高一下学期开学考试化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高一上学期期末考试化学试题上海市进才中学2022-2023学年高一上学期期末考试化学试题第一章 化学物质及其变化 第4讲 氧化还原反应湖北省宜昌市长阳土家族自治县第一高级中学2023-2024学年高一上学期9月月考化学试题广东省深圳市龙华中学2023-2024学年高一上学期12月期中考试化学试题山西省太原市第四十八中学校2023-2024学年高一上学期第一次月考化学试题福建省厦门双十中学2023-2024学年高一上学期期中考试化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷(已下线)09-10年瑞安中学高一提前招阶段性检测化学卷(已下线)2010年江苏省灌南县第二高级中学高二下学期期末考试化学试题(已下线)2010—2011学年福建省安溪一中、养正中学高二下学期期末联考化学试卷(理)(已下线)2012届甘肃省天水市二中高三模拟(5月)考试化学试卷(已下线)2013-2014学年辽宁省抚顺市六校联合体高二下学期期末考试化学试卷2016届内蒙古巴彦淖尔市第一中学高三上学期9月月考化学试卷2017届广东省仲元中学高三上9月月考化学试卷江西省九江市第一中学2017-2018学年高一上学期期中考试化学试题【全国百强校】内蒙古自治区集宁一中2018-2019学年高一上学期12月月考化学试题四川省广元市川师大万达中学2018-2019学年高一上学期11月月考化学试题【全国百强校】云南省云天化中学2018-2019学年高一上学期期末考试化学试题云南省弥勒市第四中学2019-2020学年高二上学期开学考试化学试题山东省滨州市邹平双语学校2019年高一上学期《氧化还原专题》检测广东省深圳市实验中学2019-2020学年高一上学期期中考试化学试题江西省山江湖协作体2019-2020学年高一上学期第三次月考(统招班)化学试题云南省红河州泸西一中2019-2020学年高一上学期期中考试化学试题广东省梅州市兴宁市第一中学2019-2020学年高一上学期第二次月考化学试题山西省怀仁市重点中学2019-2020学年高一上学期期末考试化学试题鲁教版高中化学必修1第二章《元素与物质世界》测试卷1人教版高中化学必修1第二章《化学物质及其变化》测试卷5云南省普洱市墨江第二中学2019-2020学年高一上学期期末考试化学试题人教版(2019)高一必修第一册第一章 物质及其变化 素养拓展区甘肃省天水市一中2020-2021学年高一下学期开学考试化学试题安徽省合肥市第六中学2021-2022学年高一上学期第一次月考化学试题云南省曲靖市会泽县实验高级中学校2022-2023学年高一上学期12月月考化学(理)试题
10-11高三·山东聊城·阶段练习
名校
解题方法
4 . 高铁酸钾(K2FeO4)是一种既能杀菌消毒又能絮凝净水的水处理剂。工业制备高铁酸钾反应的离子方程式为Fe(OH)3+ClO-+OH-→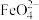 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是
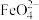 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量之比为3:2 |
| B.高铁酸钾中铁显+6价 |
C.由上述反应可知,Fe(OH)3的氧化性强于FeO |
| D.K2FeO4处理水时,不仅能杀菌消毒,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
您最近一年使用:0次
2023-08-23更新
|
430次组卷
|
26卷引用:黑龙江省黑河市第九中学2023-2024学年高三上学期摸底考试化学试题
黑龙江省黑河市第九中学2023-2024学年高三上学期摸底考试化学试题【全国百强校】黑龙江省哈尔滨市第三中学校2019届高三上学期第二次调研考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期12月月考化学试题(已下线)第二章 单元测试卷河北省衡水市武强中学2023-2024学年高一上学期期中考试化学试题河北省石家庄精英中学2023-2024学年高一上学期期中考试化学试题福建省福州高新区第一中学(闽侯县第三中学)2023-20024学年高三上学期第一次月考化学试题河南省郑州市第四高级中学2023-2024学年高一上学期第二次月考 化学试题陕西省兴平市南郊高级中学2023-2024学年高一上学期第三次化学质量检测题(已下线)2012届山东莘县实验高中高三第三次月考化学试卷2016届北京市通州区潞河中学高三上学期期中测试化学试卷2017届四川省泸州市泸化中学高三上10月月考化学卷新疆生产建设兵团第二中学2017-2018学年高一上学期期中考试化学试题福建省龙海市第二中学2019届高三年级上学期开学考化学试题广东省佛山市第一中学2020届高三10月月考化学试题甘肃省武威市第六中学2019-2020学年高一上学期第二次段考化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应福建省永春第一中学2018-2019学年高二下学期期末考试化学试题内蒙古包钢第一中学2020届高三上学期10月月考化学试题山东省潍坊第四中学2021-2022学年高三上学期10月月考化学试题山东省潍坊市昌乐二中2021-2022学年高三10月月考化学试题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)辽宁省沈阳市新民市第一高级中学2021-2022学年高三上学期第二次阶段测试化学试题浙江省杭州地区(含周边)重点中学2022-2023学年高一上学期期中考试化学试卷【2022】【高一上】【杭师大附中】【期中考】【高中化学】【徐外兰收集】(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)
5 . 铅元素位于周期表ⅣA族,其氧化物铅丹(Pb3O4)可作防锈涂料,围绕铅丹的制备与性质有如下流程。下列有关说法错误的是
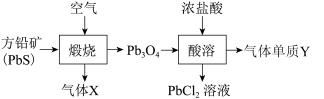

| A.Pb3O4可表示为2PbO·PbO2 |
| B.“煅烧”时PbS只作还原剂,Cl2的氧化性强于Pb3O4 |
| C.气体X既是氧化产物又是还原产物,气体Y为氧化产物 |
| D.“酸溶”时0.1 mol Pb3O4与足量的浓盐酸反应,生成0.1 mol Cl2 |
您最近一年使用:0次
2023-08-11更新
|
103次组卷
|
2卷引用:黑龙江省哈尔滨市第四中学校2023-2024学年高一上学期11月月考化学试题
6 . 中华文化源远流长、博大精深。下列说法不正确的是
| A.“欲试药金(铜锌合金),烧火有五色气起”,通过焰色试验可检验金属元素 |
| B.《中医药典》记载木耳具有“和血养营”(治疗贫血症)功效,黑木耳富含铁元素 |
| C.《淮南万毕术》记载“曾青(CuSO4)得铁,则化为铜,外化而内不化”,说明铁的氧化性强于铜 |
| D.“蜡炬成灰泪始干”、“爆竹声中一岁除”中均涉及氧化还原反应 |
您最近一年使用:0次
2023-07-28更新
|
297次组卷
|
7卷引用:黑龙江省大庆铁人中学2023-2024学年高一上学期期末考试化学试题
黑龙江省大庆铁人中学2023-2024学年高一上学期期末考试化学试题(已下线)专项01 化学与生产、生活、科技和环保-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)湖南省湘潭凤凰中学2023-2024学年高一上学期12月月考化学试题黑龙江省实验中学2023-2024学年高一下学期开学测试化学试题陕西省咸阳市2022-2023学年高一上学期期末考试化学试题陕西省西安市高陵区第三中学2023-2024学年高一上学期期末化学试卷安徽省淮北市龙兴中学2023-2024学年高一上学期期末化学试卷
名校
解题方法
7 . 以某含钴废料(主要成分为 ,含有少量铁的氧化物、
,含有少量铁的氧化物、 和NiO)为原料制备碳酸钴和黄钠铁矾
和NiO)为原料制备碳酸钴和黄钠铁矾 的工艺流程如下。下列说法错误的是
的工艺流程如下。下列说法错误的是

 ,含有少量铁的氧化物、
,含有少量铁的氧化物、 和NiO)为原料制备碳酸钴和黄钠铁矾
和NiO)为原料制备碳酸钴和黄钠铁矾 的工艺流程如下。下列说法错误的是
的工艺流程如下。下列说法错误的是
A.还原性: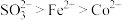 |
B.可用 溶液检验“氧化”是否完全 溶液检验“氧化”是否完全 |
C.“调pH”时反应的离子方程式: |
D.“沉钴”时若用 代替 代替 ,将有 ,将有 放出污染环境 放出污染环境 |
您最近一年使用:0次
2023-06-02更新
|
236次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2023-2024学年高三上学期开学考试化学试题
名校
解题方法
8 . 下列实验操作、现象及相应的结论,表述均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 溶液先变橙色,后变蓝色 | 氧化性: |
| B | 向某溶液中先滴加几滴新制氯水,再滴加几滴KSCN溶液,观察溶液颜色变化 | 溶液变血红色 | 原溶液中一定有 |
| C | 用镊子分别取绿豆粒大小的金属Na、K置于盛有水的烧杯中 | K与水反应更加剧烈 | 金属性: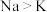 |
| D | 浓硫酸滴入蔗糖中,产生的气体通入品红溶液中 | 蔗糖变黑、体积膨胀、有刺激性气味气体产生、品红溶液褪色 | 浓硫酸具有脱水性、强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 下列离子反应方程式书写错误的是
A.AgCl浊液中通入 变黑: 变黑: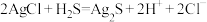 |
B.向硝酸银溶液中滴加过量稀氨水: |
C.向碳酸钠溶液中通入等物质的量的氯气: |
D.用亚硫酸钠溶液吸收过量氯气: |
您最近一年使用:0次
2023-03-31更新
|
340次组卷
|
2卷引用:黑龙江省 牡丹江市第二高级中学2023-2024学年高三上学期12月月考化学试题
10 . 二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3 或浓H2SO4反应生成 SeO2 以回收Se。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O=Se+2SO +4H+。
+4H+。
(1)Se 与浓 H2SO4 的反应中,氧化剂是_______ ,还原剂是_______ ,反应中被还原的元素是_______ 。当有标准状况下 22.4 L SO2 气体生成时,转移电子的物质的量是_______ mol。
(2)依据反应①、②判断 SeO2、浓 H2SO4、SO2的氧化性由强到弱的顺序是_______ 。
(3)用双线桥法标出反应②电子转移的方向和数目:_______ 。
已知:①Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O=Se+2SO
 +4H+。
+4H+。(1)Se 与浓 H2SO4 的反应中,氧化剂是
(2)依据反应①、②判断 SeO2、浓 H2SO4、SO2的氧化性由强到弱的顺序是
(3)用双线桥法标出反应②电子转移的方向和数目:
您最近一年使用:0次



