1 . 二氧化氯(ClO2)是国际公认的广谱、高效和安全的杀菌剂。
(1)制备C1O2的一种方法是在酸性条件下用草酸(碳的价态+3价)和氯酸钠反应,配平该反应的化学方程式,并标出电子转移的方向和数目:________ 。
_____H2C2O4+_____NaClO3+____H2SO4→_____ Na2SO4+___CO2↑+_____ClO2↑+___ H2O
(2)上述反应中被氧化的元素是____ ,氧化产物是_____ 。
(3)若反应中生成1.12L(标况) ClO2,转移电子数目为________ 。
(4)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,计算ClO2的消毒能力是等质量Cl2的_____ 倍(保留2位小数)。
(5)若以NaClO2为原料制备ClO2,需要加入具有____ (填“氧化性”或“还原性”)的物质。
(1)制备C1O2的一种方法是在酸性条件下用草酸(碳的价态+3价)和氯酸钠反应,配平该反应的化学方程式,并标出电子转移的方向和数目:
_____H2C2O4+_____NaClO3+____H2SO4→_____ Na2SO4+___CO2↑+_____ClO2↑+___ H2O
(2)上述反应中被氧化的元素是
(3)若反应中生成1.12L(标况) ClO2,转移电子数目为
(4)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,计算ClO2的消毒能力是等质量Cl2的
(5)若以NaClO2为原料制备ClO2,需要加入具有
您最近一年使用:0次
名校
2 . 某化学实验小组同学利用如图所示装置制备氨气,并探究氨气的性质(部分仪器已略去)。_______ 。
(2)干燥氨气常用的干燥剂是_______ 。
a. b.浓硫酸 c.
b.浓硫酸 c. d.碱石灰
d.碱石灰
(3)收集氨气时,请你选择氨气的进气口_______ (填“a”或“b”)。
(4)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是_______ 。
(5)用图C装置进行喷泉实验,上部烧瓶已装满氯化氢,引发水上喷的操作是_______ 。
(6)下列装置用于 尾气处理较合适的是
尾气处理较合适的是_______ 。 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是 催化还原氮氧化物技术。反应原理如图所示。当
催化还原氮氧化物技术。反应原理如图所示。当 与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有
与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有_______ 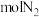 生成。
生成。
(2)干燥氨气常用的干燥剂是
a.
 b.浓硫酸 c.
b.浓硫酸 c. d.碱石灰
d.碱石灰(3)收集氨气时,请你选择氨气的进气口
(4)若观察到装置B中的烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(5)用图C装置进行喷泉实验,上部烧瓶已装满氯化氢,引发水上喷的操作是
(6)下列装置用于
 尾气处理较合适的是
尾气处理较合适的是
 等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是
等氮氧化物的尾气排出,为消除它们对环境的破坏作用,目前应用最广泛的烟气氮氧化物脱除技术是 催化还原氮氧化物技术。反应原理如图所示。当
催化还原氮氧化物技术。反应原理如图所示。当 与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有
与NO的物质的量之比为1:1时,与足量氨气在一定条件下发生反应。当有18mol电子发生转移时,将有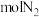 生成。
生成。
您最近一年使用:0次
名校
解题方法
3 . 离子化合物 和
和 与水的反应分别为①
与水的反应分别为①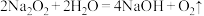 ;②
;②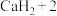
 。下列说法正确的是
。下列说法正确的是
 和
和 与水的反应分别为①
与水的反应分别为①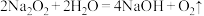 ;②
;②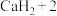
 。下列说法正确的是
。下列说法正确的是A. 、 、 中均有离子键和共价键 中均有离子键和共价键 |
| B.①中水发生氧化反应,②中水发生还原反应 |
C. 中阴、阳离子个数比为1∶2, 中阴、阳离子个数比为1∶2, 中阴、阳离子个数比为2∶1 中阴、阳离子个数比为2∶1 |
D.当反应①和②中转移的电子数相同时,产生的 和 和 的物质的量相同 的物质的量相同 |
您最近一年使用:0次
名校
4 . 一种处理温室气体二氧化碳的方法: ,
, 代表阿伏加德罗常数的值。下列说法
代表阿伏加德罗常数的值。下列说法不正确 的是
 ,
, 代表阿伏加德罗常数的值。下列说法
代表阿伏加德罗常数的值。下列说法A.标准状况下,2.24 L  中共用的电子对数为 中共用的电子对数为 |
B.0.1 mol 中含有的电子数为 中含有的电子数为 |
C.生成18 g 转移电子数为 转移电子数为 |
D.1 mol  和2 mol 和2 mol  充分反应生成 充分反应生成 的分子数为 的分子数为 |
您最近一年使用:0次
名校
解题方法
5 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加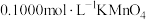 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗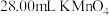 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: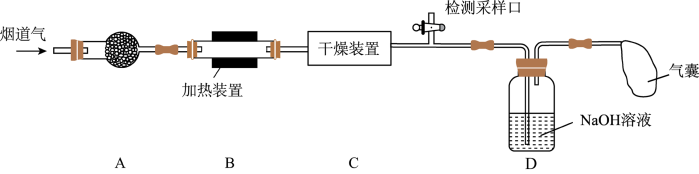
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: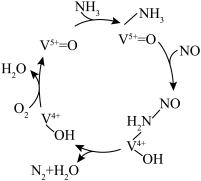
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: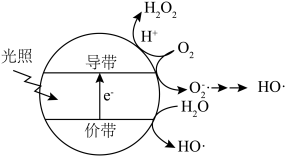
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加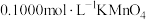 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗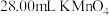 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近一年使用:0次
2024-05-03更新
|
220次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
6 . 化工厂用浓氨水检验氯气管道是否漏气,利用的反应如下: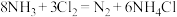
(1)作还原剂的物质是_________ ,氯元素的化合价_________ (填“升高”或“降低”)。
(2)若反应中每生成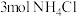 ,则消耗
,则消耗 的物质的量至少为
的物质的量至少为_________  ,转移电子的物质的量为
,转移电子的物质的量为_________  。
。
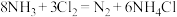
(1)作还原剂的物质是
(2)若反应中每生成
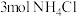 ,则消耗
,则消耗 的物质的量至少为
的物质的量至少为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近一年使用:0次
名校
7 .  恰好将
恰好将 氧化为
氧化为 ,则元素Z在还原产物中的化合价是
,则元素Z在还原产物中的化合价是
 恰好将
恰好将 氧化为
氧化为 ,则元素Z在还原产物中的化合价是
,则元素Z在还原产物中的化合价是| A.+6 | B.+4 | C.+3 | D.+2 |
您最近一年使用:0次
解题方法
8 . 对于反应:2Na2O2+2CO2=2Na2CO3+O2↑,下列说法正确的是
| A.Na2O2是氧化剂,CO2是还原剂 |
| B.该反应中电子转移的数目为4e- |
| C.Na2O2既是氧化剂,又是还原剂 |
| D.每有44gCO2与足量Na2O2反应,则固体增重56g |
您最近一年使用:0次
名校
9 . 4NH3+5O2 4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是
4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是
 4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是
4NO+6H2O是工业制备硝酸的重要反应之一、下列说法正确的是A.中子数为10的氧原子: |
| B.沸点:PH3>NH3 |
| C.4molNH3完全反应,转移5mol电子 |
| D.该反应为复分解反应 |
您最近一年使用:0次
10 . AgCl可溶于氨水生成Ag(NH3)2Cl,Ag(NH3)2Cl与NH3反应可生成Ag。反应如下:4Ag(NH3)2Cl + N2H4 + 4H2O = 4Ag↓ + N2↑ + 4NH4Cl + 4NH3·H2O。下列关于该反应说法正确的是
| A.Ag(NH3)2Cl发生氧化反应 |
| B.还原性:N2H4<Ag |
C.N2H4的结构式为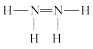 |
| D.每生成标准状况下11.2LN2,反应中转移2mol电子 |
您最近一年使用:0次



