名校
1 . NO、 、CO是常见的空气污染气体。在某分子筛的催化作用下,
、CO是常见的空气污染气体。在某分子筛的催化作用下, 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无害物质,其反应历程如图所示。下列说法不正确的是
,生成两种无害物质,其反应历程如图所示。下列说法不正确的是
 、CO是常见的空气污染气体。在某分子筛的催化作用下,
、CO是常见的空气污染气体。在某分子筛的催化作用下, 可脱除废气中的NO和
可脱除废气中的NO和 ,生成两种无害物质,其反应历程如图所示。下列说法不正确的是
,生成两种无害物质,其反应历程如图所示。下列说法不正确的是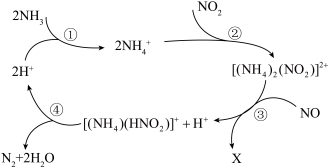
| A.历程中反应①②都是非氧化还原反应 |
B. 中不含有 中不含有 价的N 价的N |
C.X是 和 和 ,其中 ,其中 的电子式是 的电子式是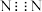 |
D.汽车尾气中的氮氧化合物主要是高温下气缸里的 、 、 反应产生的 反应产生的 |
您最近一年使用:0次
名校
2 . 一种利用含钴废料(主要成分为 ,还含有少量
,还含有少量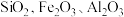 等杂质)制备
等杂质)制备 的工艺流程如下。
的工艺流程如下。 如下表:
如下表:
② 的
的 的
的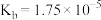 。
。
下列说法不正确的是
 ,还含有少量
,还含有少量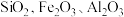 等杂质)制备
等杂质)制备 的工艺流程如下。
的工艺流程如下。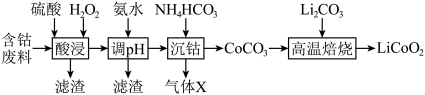
 如下表:
如下表:| 金属离子 |  |  |  |  |
开始沉淀的 | 8.5 | 2.2 | 3.4 | 7.8 |
完全沉淀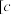 (金属离子) (金属离子)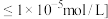 的的 的的 | 10.0 | 3.0 | 4.5 | 9.4 |
 的
的 的
的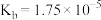 。
。下列说法不正确的是
A.由流程可知氧化性: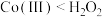 |
B.常温下加入的 溶液显碱性 溶液显碱性 |
C.气体 通入氨水至过量后所得溶液可循环利用 通入氨水至过量后所得溶液可循环利用 |
D.“高温焙烧”时的化学方程式: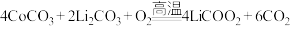 |
您最近一年使用:0次
名校
3 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。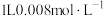 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
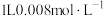 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.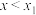 时, 时, 主要被氧化为 主要被氧化为 |
B.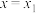 时,生成的 时,生成的 的物质的量为 的物质的量为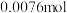 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次
名校
4 . 海水是巨大的资源宝库,以下是人类从海水中提取某些重要化工原料的简单流程示意图。下列说法错误的是
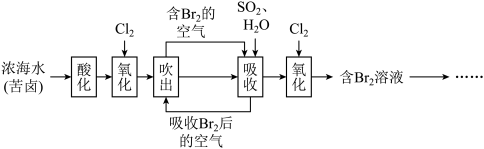
| A.“吹出”时,常采用热空气吹出溴,利用了溴单质的易挥发性 |
B.用 水溶液吸收 水溶液吸收 的离子方程式为 的离子方程式为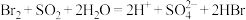 |
| C.流程中氧化→吸收→氧化的目的是富集溴单质 |
D.工业上也可用 溶液代替二氧化硫吸收 溶液代替二氧化硫吸收 ,会生成无色无味气体和 ,会生成无色无味气体和 ,则反应的化学方程式为 ,则反应的化学方程式为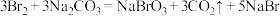 |
您最近一年使用:0次
2024-06-17更新
|
74次组卷
|
2卷引用:河南省名校联盟2023-2024学年高一下学期5月联考化学试题
名校
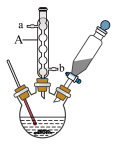
5 . 苯甲酸是一种重要原料。实验室可以用甲苯与高锰酸钾反应制得苯甲酸,反应装置图和有关数据如下:
合成步骤如下:
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时再迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
(1)仪器A的名称是____________ ,它的作用是____________ 。
(2)加入碎瓷片的作用是____________ 。
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为________________________ 。
(4)若得到的苯甲酸晶体产品不纯,则采用____________ 方法可得到纯度更高的产品。
(5)下列有关苯甲酸重结晶实验的说法正确的是_________ (填字母)。
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是____________ (保留一位小数)。
物质 | 熔点/℃ | 沸点/℃ | 水中溶解度/g(25℃) | 相对分子质量 | 密度/( |
甲苯 |
| 110.6 | 难溶 | 92 | 0.85 |
苯甲酸 | 122.13 | 249 | 0.344 | 122 | 1.27 |
①在三颈烧瓶中加入5.4mL甲苯和30mL稀硫酸,放入碎瓷片,加热至沸腾时再迅速加入12.8g高锰酸钾固体,继续加热到甲苯层消失,过滤;
②反应后的溶液仍呈紫色,在容器中加入适量亚硫酸氢钠溶液,振荡,直到溶液变为无色,搅拌下向容器中加入足量浓盐酸;待反应完全后,将反应容器放在冰水浴中冷却,析出晶体,过滤,洗涤,干燥,称量。
已知: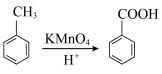 。
。
(1)仪器A的名称是
(2)加入碎瓷片的作用是
(3)加入亚硫酸氢钠溶液使紫色褪去时发生反应的离子方程式为
(4)若得到的苯甲酸晶体产品不纯,则采用
(5)下列有关苯甲酸重结晶实验的说法正确的是
A.粗苯甲酸溶解过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水
C.冷却结晶时,温度过低将析出杂质,故此时温度不是越低越好
(6)若最后得到纯净的苯甲酸质量为4.0g,则该反应的产率是
您最近一年使用:0次
名校
6 . 大连理工大学课题组通过CuO/ 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是
 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是A.标准状况下,1.12L NO中含有电子数为1.5 |
B.将 个 个 溶于100mL水中,所得溶液的质量分数约为29.9% 溶于100mL水中,所得溶液的质量分数约为29.9% |
C.生成22g  能消除NO的数目为0.2 能消除NO的数目为0.2 |
D.若NO和CO混合气体的平均相对分子质量为29,则含有CO的数目为0.5 |
您最近一年使用:0次
2024-03-13更新
|
308次组卷
|
4卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷
名校
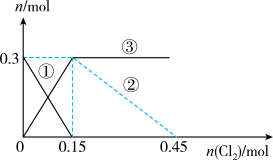
7 . 向100mL
 溶液中逐渐通入
溶液中逐渐通入 ,其中
,其中 、
、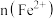 、
、 随通入
随通入 的物质的量
的物质的量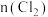 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是

 溶液中逐渐通入
溶液中逐渐通入 ,其中
,其中 、
、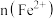 、
、 随通入
随通入 的物质的量
的物质的量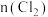 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
A.②代表 ,③代表 ,③代表 |
B.还原性强弱: |
C. 时,溶液中 时,溶液中 |
D.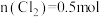 时,总的离子方程式为: 时,总的离子方程式为: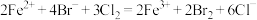 |
您最近一年使用:0次
2023-01-04更新
|
402次组卷
|
2卷引用:湖北省荆州市八县市2022-2023学年高一上学期期末联考化学试题
8 . Ⅰ.高铁酸钾(K2FeO4) 是一种高效、无毒的强氧化剂,常温下为紫色固体,微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH)3胶体。稳定性随pH的下降而减弱,酸性条件下易分解。
(1)下列有关铁及其化合物的性质与用途具有对应关系的是___________
Ⅱ.K2FeO4的净水原理如图所示:
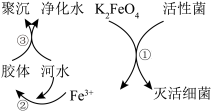
(2)下列说法错误的是___________
(3)写出K2FeO4与水反应的化学方程式___________ 。
Ⅲ.已知可用Cl2与Fe(NO3)3制备K2FeO4(含副产品KCl、KNO3),查阅资料得知高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:
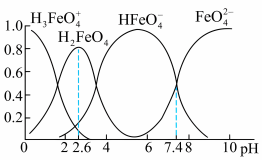
(4)①为获得尽可能纯净的高铁酸盐,pH应控制在___________ 。
②写出在此条件下,反应的离子方程式:___________ ;每生成39.6g K2FeO4,转移的电子数目为___________ ;
(5)已知溶液的酸碱性及离子浓度会对反应试剂的氧化性、还原性产生影响。
某实验小组研究不同反应试剂对K2FeO4产率的影响,对比实验如下:
注:上述实验中,溶液总体积、FeCl3和Fe(NO3)3的物质的量、Cl2的通入量均相同。
①由实验I、II的现象可知,Fe3+的还原性随溶液碱性的增强而___________ (填“增强”、“减弱”或“不变”);
②实验II中K2FeO4的产率比实验III低,试解释其可能的原因:___________ ;
③向实验II所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅,试解释其可能的原因:___________ 。
(6)实验室测定含少量杂质的K2FeO4样品的纯度:称取0.1500g K2FeO4样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用0.1000 mol·L−1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液25.00 mL。滴定时,发生反应的离子方程式:FeO + 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O
+ 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O = S4O
= S4O + 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
+ 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:___________ (写出计算过程)。
(1)下列有关铁及其化合物的性质与用途具有对应关系的是___________
| A.铁粉具有还原性,可防止食物氧化变质 | B.高铁酸钾能溶于水,可作氧化剂 |
| C.氢氧化铁胶体具有碱性,可用于净水 | D.纯铁无杂质,可用作建筑材料 |
Ⅱ.K2FeO4的净水原理如图所示:

(2)下列说法错误的是___________
| A.K2FeO4中铁元素显+6价 |
| B.过程①中K2FeO4被细菌还原 |
| C.过程②中的Fe(OH)3胶体粒子带正电荷 |
| D.过程③中聚沉是由于胶体发生了渗析 |
(3)写出K2FeO4与水反应的化学方程式
Ⅲ.已知可用Cl2与Fe(NO3)3制备K2FeO4(含副产品KCl、KNO3),查阅资料得知高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:

(4)①为获得尽可能纯净的高铁酸盐,pH应控制在
②写出在此条件下,反应的离子方程式:
(5)已知溶液的酸碱性及离子浓度会对反应试剂的氧化性、还原性产生影响。
某实验小组研究不同反应试剂对K2FeO4产率的影响,对比实验如下:
| 实验编号 | 反应试剂 | 实验现象 |
| Ⅰ | Cl2、FeCl3和少量KOH | 无明显现象 |
| Ⅱ | Cl2、FeCl3和过量KOH | 得到紫色溶液,无紫色固体 |
| Ⅲ | Cl2、Fe(NO3)3和过量KOH | 得到紫色溶液(颜色比Ⅱ深),有紫色固体 |
①由实验I、II的现象可知,Fe3+的还原性随溶液碱性的增强而
②实验II中K2FeO4的产率比实验III低,试解释其可能的原因:
③向实验II所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅,试解释其可能的原因:
(6)实验室测定含少量杂质的K2FeO4样品的纯度:称取0.1500g K2FeO4样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用0.1000 mol·L−1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液25.00 mL。滴定时,发生反应的离子方程式:FeO
 + 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O
+ 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O = S4O
= S4O + 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
+ 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
您最近一年使用:0次
名校
9 . 黄铁矿( )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
)在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
 )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
)在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是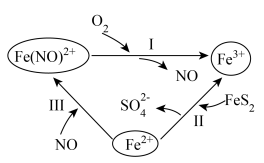
| A.反应Ⅰ、Ⅱ、Ⅲ均发生氧化还原反应 |
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为 |
C.反应Ⅱ的离子方程式为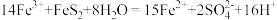 |
D.该过程的总反应为 |
您最近一年使用:0次
2024-05-16更新
|
230次组卷
|
3卷引用:重庆市荣昌永荣中学校2024届高三下学期模拟预测化学试题2
10 .  (铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是
(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是
等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是
 (铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是
(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是
等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是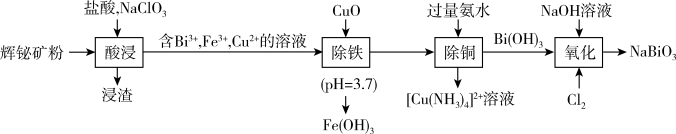
A.“酸浸”过程中,用硝酸代替“盐酸, ”更环保 ”更环保 |
B.“除铜”中涉及的离子方程式为: |
C.检验“酸浸”液中是否含有 ,可以选择“ ,可以选择“ 液”或“ 液”或“ 溶液和双氧水” 溶液和双氧水” |
D.“氧化”过程中,每消耗标准状况下5.6L ,生成70g ,生成70g |
您最近一年使用:0次
2023-11-15更新
|
226次组卷
|
2卷引用:江西省赣州中学(中学生标准学术能力诊断性测试)2023-2024学年高三上学期11月测试化学试题

 )
)