1 .  在酸性溶液中与
在酸性溶液中与 发生反应,反应产物为
发生反应,反应产物为 、
、 、
、 。已知反应中氧化剂与还原剂的个数之比为
。已知反应中氧化剂与还原剂的个数之比为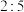 ,则x的值为
,则x的值为
 在酸性溶液中与
在酸性溶液中与 发生反应,反应产物为
发生反应,反应产物为 、
、 、
、 。已知反应中氧化剂与还原剂的个数之比为
。已知反应中氧化剂与还原剂的个数之比为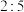 ,则x的值为
,则x的值为| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
2022-11-29更新
|
355次组卷
|
7卷引用:甘肃省兰州第一中学2023-2024学年高一上学期10月月考化学试题
名校
解题方法
2 . 对于下列实验,不能正确描述其反应的离子方程式是
A.铝溶于氢氧化钠溶液,有无色气体产生:2Al+2OH-+2H2O=2AlO +3H2↑ +3H2↑ |
| B.向硝酸银溶液中滴加少量碘化钾溶液:Ag++I-=AgI↓ |
C.SO2通入酸性KMnO4溶液中:5SO2+2H2O+2MnO =5SO =5SO +4H++2Mn2+ +4H++2Mn2+ |
D.向次氯酸钙溶液中通入少量二氧化碳气体:ClO-+CO2+H2O=HClO+HCO |
您最近一年使用:0次
名校
3 . 全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下:
_______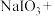 _______
_______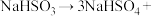 _______
_______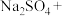 _______
_______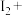 _______
_______ (未配平),
(未配平),
完成下列填空:
(1)配平上述反应_______ ,该反应实质是两步反应:①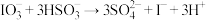 ,则第二步反应的离子方程式为②
,则第二步反应的离子方程式为②_______ ;若要使碘酸钠的利用率最高,碘酸钠在第一步和第二步反应中的用量之比是_______ 。
(2)过滤反应析出的碘沉淀得到粗碘,再用升华法即可得到99%左右的碘产品,碘升华克服的微粒间作用力为_______ 。
(3)能说明氯、碘两种元素非金属性相对强弱的依据是_______。(选填编号)
(4)检验亚硫酸钠固体是否氧化变质的方法是_______ 。
_______
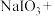 _______
_______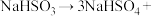 _______
_______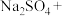 _______
_______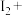 _______
_______ (未配平),
(未配平),完成下列填空:
(1)配平上述反应
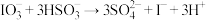 ,则第二步反应的离子方程式为②
,则第二步反应的离子方程式为②(2)过滤反应析出的碘沉淀得到粗碘,再用升华法即可得到99%左右的碘产品,碘升华克服的微粒间作用力为
(3)能说明氯、碘两种元素非金属性相对强弱的依据是_______。(选填编号)
| A.原子的最外层都有7个电子 |
| B.ICl中碘元素为+1价 |
C.酸性: |
| D.氯化钠、碘化钠与浓硫酸共热,分别生成氯化氢、单质碘 |
您最近一年使用:0次
名校
4 . 镧系金属铈(Ce)主要有+3、+4两种价态,地壳中常以氟碳铈矿( )存在。工业上利用氟碳铈矿提取
)存在。工业上利用氟碳铈矿提取 的一种工艺流程如图所示。下列有关说法错误的是
的一种工艺流程如图所示。下列有关说法错误的是

 )存在。工业上利用氟碳铈矿提取
)存在。工业上利用氟碳铈矿提取 的一种工艺流程如图所示。下列有关说法错误的是
的一种工艺流程如图所示。下列有关说法错误的是
A.加热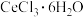 制备无水 制备无水 时,HCl的作用是抑制 时,HCl的作用是抑制 的水解 的水解 |
| B.在空气中焙烧氟碳铈矿时,发生的主要反应的氧化剂和还原剂的物质的量之比为1∶4 |
C.参与酸浸反应的 和 和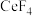 的物质的量之比为1∶3时,则需要 的物质的量之比为1∶3时,则需要 和HCl的物质的量之比也为1∶3 和HCl的物质的量之比也为1∶3 |
D.向 中加入KCl溶液的目的是将 中加入KCl溶液的目的是将 转化为 转化为 ,提高产率 ,提高产率 |
您最近一年使用:0次
名校
5 . 下列反应的离子方程式正确的是
A.红褐色固体 全部溶于氢碘酸溶液: 全部溶于氢碘酸溶液: |
B.用石墨电极电解 溶液: 溶液: |
C.将等浓度的 溶液与 溶液与 溶液按体积比2∶3混合: 溶液按体积比2∶3混合: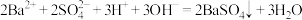 |
D.洁厕灵(含HCl)与“84”消毒液混合后产生氯气: |
您最近一年使用:0次
名校
解题方法
6 . 二氧化氯(ClO2)是一种优良的消毒剂,熔点为-59℃,沸点为 11℃,浓度过高时易发生分解,甚至爆炸。某课外兴趣小组通过氯气与 NaClO2 溶液反应来制取少量 ClO2,装置如图所示:

(1)甲装置中盛有浓盐酸的装置名称是___________ 。
(2)圆底烧瓶内发生反应的离子方程式是___________ 。
(3)Cl—存在时会催化 ClO2 的生成,若无乙装置,则丙装置内产生 ClO2 的速率明显加快。乙装置中试剂瓶内的液体是___________ ,实验过程中常需通入适量的 N2稀释 ClO2,其目的是___________ 。
(4)戊装置烧杯中 ClO2 被 NaOH 溶液吸收后,生成 ClO 和 ClO
和 ClO ,该反应的化方程式为
,该反应的化方程式为_____
(5)为了验证氯气的氧化性,将氯气通入 Na2SO3 溶液中,检验出反应后溶液中含有SO ,写出氯气与 Na2SO3 反应的离子方程式:
,写出氯气与 Na2SO3 反应的离子方程式:___________ 。

(1)甲装置中盛有浓盐酸的装置名称是
(2)圆底烧瓶内发生反应的离子方程式是
(3)Cl—存在时会催化 ClO2 的生成,若无乙装置,则丙装置内产生 ClO2 的速率明显加快。乙装置中试剂瓶内的液体是
(4)戊装置烧杯中 ClO2 被 NaOH 溶液吸收后,生成 ClO
 和 ClO
和 ClO ,该反应的化方程式为
,该反应的化方程式为(5)为了验证氯气的氧化性,将氯气通入 Na2SO3 溶液中,检验出反应后溶液中含有SO
 ,写出氯气与 Na2SO3 反应的离子方程式:
,写出氯气与 Na2SO3 反应的离子方程式:
您最近一年使用:0次
7 . 实验题
(1)全球一半左右的甸是以智力硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取相关反应如下,请配平该反应:_
___NaIO3 + _____NaHSO3 =_____ NaHSO4 + ____Na2SO4 +_____I2+ _____H2O
(2)实验探究-加碘盐中碘元素的检验
①加碘盐中碘元素的存在形式:__ 。
②检验原理:在酸性条件下,IO 与I- 反应的离子方程式
与I- 反应的离子方程式___ ,生成的单质碘用淀粉溶液检验,现象是______ 。
③用试纸和生活中的常见物质检验加碘盐中碘元素存在方案:
a.将食盐水溶解,加入适量___________ ,
b.蘸取少量溶液,滴在___________ 试纸上。
c.实验现象及结论:试纸___________ ,证明有碘元素存在。
(1)全球一半左右的甸是以智力硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取相关反应如下,请配平该反应:
___NaIO3 + _____NaHSO3 =_____ NaHSO4 + ____Na2SO4 +_____I2+ _____H2O
(2)实验探究-加碘盐中碘元素的检验
①加碘盐中碘元素的存在形式:
②检验原理:在酸性条件下,IO
 与I- 反应的离子方程式
与I- 反应的离子方程式③用试纸和生活中的常见物质检验加碘盐中碘元素存在方案:
a.将食盐水溶解,加入适量
b.蘸取少量溶液,滴在
c.实验现象及结论:试纸
您最近一年使用:0次
8 . 填空题
(1)制备Na2S2O3的实验一般控制在碱性条件下进行,否则产品发黄,用离子反应方程式表示其原因___________ 。
(2)+6价铬的化合物毒性很大,常用NaHSO3将废液中Cr2O 还原为Cr3+,该反应的离子方程式为
还原为Cr3+,该反应的离子方程式为___________ 。
(3)辉铜矿和铜蓝矿都是天然含硫铜矿,在地壳中常伴生存在。先取一份该伴生矿样品,经检测后确定仅含有Cu2S、CuS和惰性杂质。取样品,加入酸性KMnO4溶液,加热,写出Cu2S溶于酸性KMnO4溶液的离子方程式___________ 。
(4)ClO2可以用于纸浆蜂蜡等的精制和漂白,也可用于饮用水的杀菌消毒处理,已知在酸性条件下NaClO3可发生反应生成NaCl,并释放出ClO2,该反应的离子方程式___________ 。
(1)制备Na2S2O3的实验一般控制在碱性条件下进行,否则产品发黄,用离子反应方程式表示其原因
(2)+6价铬的化合物毒性很大,常用NaHSO3将废液中Cr2O
 还原为Cr3+,该反应的离子方程式为
还原为Cr3+,该反应的离子方程式为(3)辉铜矿和铜蓝矿都是天然含硫铜矿,在地壳中常伴生存在。先取一份该伴生矿样品,经检测后确定仅含有Cu2S、CuS和惰性杂质。取样品,加入酸性KMnO4溶液,加热,写出Cu2S溶于酸性KMnO4溶液的离子方程式
(4)ClO2可以用于纸浆蜂蜡等的精制和漂白,也可用于饮用水的杀菌消毒处理,已知在酸性条件下NaClO3可发生反应生成NaCl,并释放出ClO2,该反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . 某同学用如图装置(夹持装置略)探究铜丝与过量浓硫酸的反应,回答下列问题:

(1)写出铜与浓硫酸反应的化学方程式为____ 。
(2)B中观察到的现象为____ ;C中应加入的试剂为____ ;倒置漏斗的作用是____ 。
(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
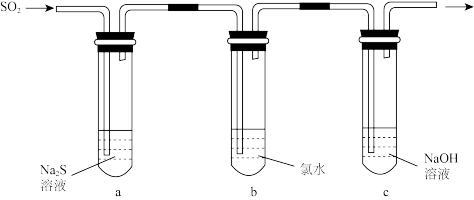
①能说明二氧化硫具有氧化性的实验现象为____ 。
②为验证二氧化硫的还原性,反应一段时间后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案合理的是____ (填I、II或III);试管b中发生反应的离子方程式为____ 。
(4)将铜丝与浓硫酸反应后的溶液冷却后加水稀释,取少许于试管中作为待测液,加____ (填化学式)溶液酸化,再取上层清液加____ (填化学式)溶液出现白色沉淀,即可确定存在SO 。写出产生白色沉淀的离子方程式
。写出产生白色沉淀的离子方程式____ 。

(1)写出铜与浓硫酸反应的化学方程式为
(2)B中观察到的现象为
(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,反应一段时间后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案合理的是
(4)将铜丝与浓硫酸反应后的溶液冷却后加水稀释,取少许于试管中作为待测液,加
 。写出产生白色沉淀的离子方程式
。写出产生白色沉淀的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有产物,用如图所示实验装置。
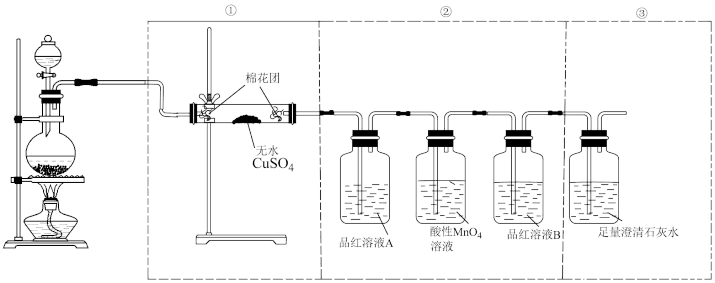
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式____ 。
(2)装置①中无水硫酸铜表面现象是____ ,作用是____ 。
(3)装置②中酸性KMnO4溶液的现象是____ ,作用是____ 。
(4)写出装置③中发生反应的方程式____ 。
(5)某校科学小组为探究浓硫酸与木炭反应中定会产生二氧化碳,将发生装置产生的混合气体从a端通入(按如图所示)①A中的现象____ ;②C中的现象____ ;③D中的现象____ ,由上述现象该小组同学就能确认该气体的成分为CO2。
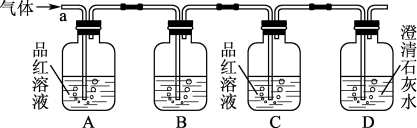
(6)利用SO2的还原性用KMnO4溶液可除去CO2混有SO2,写出发生反应的方程式____ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)装置①中无水硫酸铜表面现象是
(3)装置②中酸性KMnO4溶液的现象是
(4)写出装置③中发生反应的方程式
(5)某校科学小组为探究浓硫酸与木炭反应中定会产生二氧化碳,将发生装置产生的混合气体从a端通入(按如图所示)①A中的现象

(6)利用SO2的还原性用KMnO4溶液可除去CO2混有SO2,写出发生反应的方程式
您最近一年使用:0次



