名校
解题方法
1 . 已知常温下可用Co2O3制备Cl2,其反应方程式为Co2O3+HCl→CoCl2+Cl2↑+H2O (未配平),下列叙述错误的是
| A.氧化产物为Cl2,氧化性:Co2O3>Cl2 |
| B.H2O前面的计量数为3 |
| C.HCl在该反应中只表现还原性 |
| D.标准状况下,反应生成22.4L Cl2时,转移2mol电子 |
您最近一年使用:0次
2022-11-27更新
|
152次组卷
|
2卷引用:山东省淄博实验中学2022-2023学年高一上学期期中考试化学试题
名校
2 . 二氧化氯 是一种新型高效安全消毒剂,易溶于水,沸点为11℃,在空气中的体积分数超过
是一种新型高效安全消毒剂,易溶于水,沸点为11℃,在空气中的体积分数超过 时有爆炸性。工业上利用硫铁矿[主要成分为二硫化亚铁
时有爆炸性。工业上利用硫铁矿[主要成分为二硫化亚铁 ]还原氯酸钠
]还原氯酸钠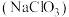 制取二氧化氯。某研究小组利用如图装置模拟工业制备
制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。
并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。
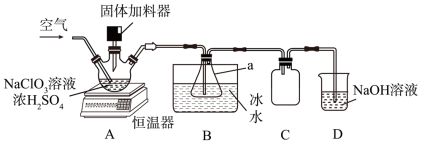
回答下列问题:
(1)通入空气的目的为①_______ ,②_______ 。
(2)装置D中 溶液用于吸收多余的
溶液用于吸收多余的 。某兴趣小组在一定条件下将一定量的
。某兴趣小组在一定条件下将一定量的 通入
通入

 溶液中,
溶液中, 恰好反应,得到的产物中含有
恰好反应,得到的产物中含有 、
、 和
和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为_______  。
。
(3)工业上可用 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中的
和盐酸,以除去水中的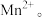 该反应的离子方程式为
该反应的离子方程式为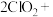 _______
_______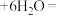 _______
_______ _______
_______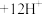 ;
;_______ 。若除去 的
的 ,反应消耗的
,反应消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。
 是一种新型高效安全消毒剂,易溶于水,沸点为11℃,在空气中的体积分数超过
是一种新型高效安全消毒剂,易溶于水,沸点为11℃,在空气中的体积分数超过 时有爆炸性。工业上利用硫铁矿[主要成分为二硫化亚铁
时有爆炸性。工业上利用硫铁矿[主要成分为二硫化亚铁 ]还原氯酸钠
]还原氯酸钠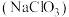 制取二氧化氯。某研究小组利用如图装置模拟工业制备
制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。
并通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。
回答下列问题:
(1)通入空气的目的为①
(2)装置D中
 溶液用于吸收多余的
溶液用于吸收多余的 。某兴趣小组在一定条件下将一定量的
。某兴趣小组在一定条件下将一定量的 通入
通入

 溶液中,
溶液中, 恰好反应,得到的产物中含有
恰好反应,得到的产物中含有 、
、 和
和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为 。
。(3)工业上可用
 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中的
和盐酸,以除去水中的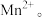 该反应的离子方程式为
该反应的离子方程式为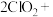 _______
_______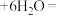 _______
_______ _______
_______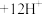 ;
; 的
的 ,反应消耗的
,反应消耗的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
名校
3 . 从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
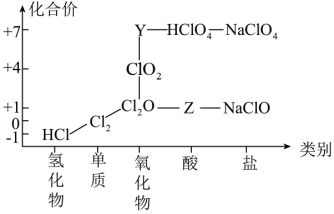
(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。
(2)已知高氯酸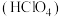 是强酸,写出高氯酸与铁反应的离子方程式
是强酸,写出高氯酸与铁反应的离子方程式_______ 。
(3)氯气既有氧化性又有还原性,结合上图说明理由_______ 。请举例证明氯气体现氧化性的化学方程式,并在方程式上用单线桥标出转移的电子数_______
(4)标况下,将
 气体溶于水形成
气体溶于水形成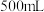 溶液,取出
溶液,取出 ,其中所含溶质的质量为
,其中所含溶质的质量为_______ g。

(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸
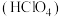 是强酸,写出高氯酸与铁反应的离子方程式
是强酸,写出高氯酸与铁反应的离子方程式(3)氯气既有氧化性又有还原性,结合上图说明理由
(4)标况下,将

 气体溶于水形成
气体溶于水形成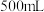 溶液,取出
溶液,取出 ,其中所含溶质的质量为
,其中所含溶质的质量为
您最近一年使用:0次
解题方法
4 . 下列离子方程式书写不正确的是
A.少量Cl2通入Na2SO3溶液中:Cl2+SO +H2O=2Cl-+2H++SO +H2O=2Cl-+2H++SO |
B.向明矾溶液中滴加Ba(OH)2溶液至沉淀物质的量最大:2Al3++3SO +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
C.将稀醋酸加入NaIO3和NaI的混合溶液中:5I-+IO +6H+=3I2+3H2O +6H+=3I2+3H2O |
D.将少量稀硝酸加入硫酸亚铁溶液中:3Fe2++NO +4H+=3Fe3++NO↑+2H2O +4H+=3Fe3++NO↑+2H2O |
您最近一年使用:0次
5 .  是一种消毒、杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:
是一种消毒、杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得: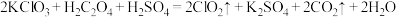 。试回答下列问题。
。试回答下列问题。
(1)若反应共产生了 气体(标准状况),则反应转移电子的物质的量为
气体(标准状况),则反应转移电子的物质的量为_______ 。
(2)标准状况下 的
的 气体恰好能与
气体恰好能与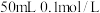 的
的 溶液完全反应生成
溶液完全反应生成 ,此过程所发生的离子方程式为
,此过程所发生的离子方程式为_______ 。
(3)常温下,可用氯酸钾固体与浓盐酸反应制备 ,写出反应的化学方程式
,写出反应的化学方程式_______ ,若氧化产物比还原产物多 ,则被氧化
,则被氧化 的物质的量为
的物质的量为_______  。
。
(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力,
的氧化能力, 的有效氯含量为
的有效氯含量为_______ 。(计算结果保留两位小数)
 是一种消毒、杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:
是一种消毒、杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得: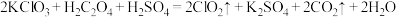 。试回答下列问题。
。试回答下列问题。(1)若反应共产生了
 气体(标准状况),则反应转移电子的物质的量为
气体(标准状况),则反应转移电子的物质的量为(2)标准状况下
 的
的 气体恰好能与
气体恰好能与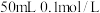 的
的 溶液完全反应生成
溶液完全反应生成 ,此过程所发生的离子方程式为
,此过程所发生的离子方程式为(3)常温下,可用氯酸钾固体与浓盐酸反应制备
 ,写出反应的化学方程式
,写出反应的化学方程式 ,则被氧化
,则被氧化 的物质的量为
的物质的量为 。
。(4)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
 的氧化能力,
的氧化能力, 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
6 .  是阿伏加德罗常数,完成下列问题。
是阿伏加德罗常数,完成下列问题。
(1)① ②
② ③
③ ④NaClO溶液⑤硫酸⑥乙醇⑦
④NaClO溶液⑤硫酸⑥乙醇⑦ ⑧
⑧ 溶液,上述物质属于强电解质的是
溶液,上述物质属于强电解质的是_______ ;14.9 g NaClO溶解在水中,要使 数与水分子数之比为1∶100,则需要水的个数为
数与水分子数之比为1∶100,则需要水的个数为_______ 。
(2) 可以通过下列反应制备:
可以通过下列反应制备: 。
。 是
是_______ (填“氧化产物”、“还原产物”或“氧化产物和还原产物”)。每生成1分子氧气,转移电子的数目为_______ 。
(3)砒霜低温下微溶于水,溶解的砒霜与水反应生成亚砷酸(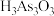 ),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀
),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀 生成,则石灰水与亚砷酸在溶液中反应的离子方程式为
生成,则石灰水与亚砷酸在溶液中反应的离子方程式为_______ 。
(4)次磷酸钙[ ,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______
,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______ _______
_______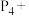 _______
_______ _______
_______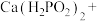 _______
_______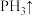 。配平该反应的化学方程式
。配平该反应的化学方程式_______ 。
 是阿伏加德罗常数,完成下列问题。
是阿伏加德罗常数,完成下列问题。(1)①
 ②
② ③
③ ④NaClO溶液⑤硫酸⑥乙醇⑦
④NaClO溶液⑤硫酸⑥乙醇⑦ ⑧
⑧ 溶液,上述物质属于强电解质的是
溶液,上述物质属于强电解质的是 数与水分子数之比为1∶100,则需要水的个数为
数与水分子数之比为1∶100,则需要水的个数为(2)
 可以通过下列反应制备:
可以通过下列反应制备: 。
。 是
是(3)砒霜低温下微溶于水,溶解的砒霜与水反应生成亚砷酸(
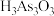 ),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀
),亚砷酸为三元弱酸。可用石灰水检验澄清溶液中是否含有砒霜,现象是有白色沉淀 生成,则石灰水与亚砷酸在溶液中反应的离子方程式为
生成,则石灰水与亚砷酸在溶液中反应的离子方程式为(4)次磷酸钙[
 ,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______
,P是+1价]可用作食品添加剂和动物营养剂,以氢氧化钙为原料制备次磷酸钙的反应为:_______ _______
_______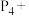 _______
_______ _______
_______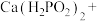 _______
_______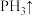 。配平该反应的化学方程式
。配平该反应的化学方程式
您最近一年使用:0次
名校
解题方法
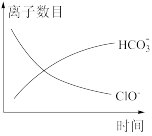
7 . 处理某废水时,反应过程中部分离子的数目与反应进程的关系如图所示,反应过程中主要存在 、
、 、
、 、
、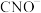 (C为+4价,N为-3价)、
(C为+4价,N为-3价)、 等微粒。下列说法
等微粒。下列说法不正确 的是
 、
、 、
、 、
、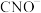 (C为+4价,N为-3价)、
(C为+4价,N为-3价)、 等微粒。下列说法
等微粒。下列说法
| A.该废水呈强酸性 |
| B.废水处理后转化为无害物质 |
C.反应的离子方程式为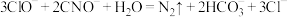 |
D.每处理1个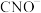 转移的电子数为3 转移的电子数为3 |
您最近一年使用:0次
2022-11-19更新
|
100次组卷
|
2卷引用:山东省青岛莱西市2022-2023学年高一上学期期中考试化学试题
名校
解题方法
8 . 元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。下图是钠的价类二维图:
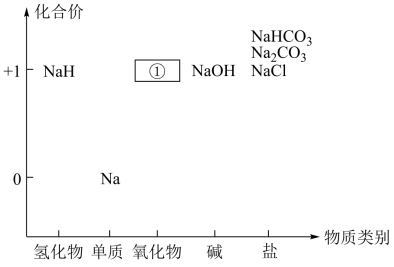
请回答以下问题:
(1) 在野外可用作生氢剂,其与水反应的化学方程式为
在野外可用作生氢剂,其与水反应的化学方程式为_______ 。
(2)写出二维图中缺失①中某种淡黄色固体的化学式_______ ,其阳离子与阴离子的个数比为_______ 。
(3) 溶液常因温度过高而分解,导致含有少量
溶液常因温度过高而分解,导致含有少量 ,除去杂质
,除去杂质 的方法为
的方法为_______ (用离子方程式表示)。
(4)向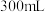 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 (忽略溶液体积的变化),充分反应。将上述所得溶液,逐滴滴加
(忽略溶液体积的变化),充分反应。将上述所得溶液,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
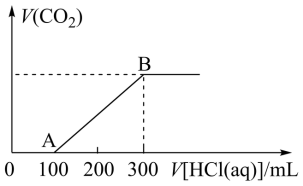
①原 溶液的浓度为
溶液的浓度为_______ 。
②AB段发生反应的离子方程式_______ 。
(5)我国科学家研发了一种室温下“可呼吸”的 充电电池。电池的总反应为:
充电电池。电池的总反应为: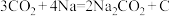 。
。
①该电池消耗 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为_______ (用 表示)。
表示)。
②该电池中不能存在水,否则可能引起电池爆炸,用离子方程式表示其原因_______ 。

请回答以下问题:
(1)
 在野外可用作生氢剂,其与水反应的化学方程式为
在野外可用作生氢剂,其与水反应的化学方程式为(2)写出二维图中缺失①中某种淡黄色固体的化学式
(3)
 溶液常因温度过高而分解,导致含有少量
溶液常因温度过高而分解,导致含有少量 ,除去杂质
,除去杂质 的方法为
的方法为(4)向
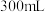 某物质的量浓度的
某物质的量浓度的 溶液中缓慢通入一定量的
溶液中缓慢通入一定量的 (忽略溶液体积的变化),充分反应。将上述所得溶液,逐滴滴加
(忽略溶液体积的变化),充分反应。将上述所得溶液,逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示:
①原
 溶液的浓度为
溶液的浓度为②AB段发生反应的离子方程式
(5)我国科学家研发了一种室温下“可呼吸”的
 充电电池。电池的总反应为:
充电电池。电池的总反应为: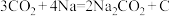 。
。①该电池消耗
 (标准状况)
(标准状况) 气体时,转移电子数为
气体时,转移电子数为 表示)。
表示)。②该电池中不能存在水,否则可能引起电池爆炸,用离子方程式表示其原因
您最近一年使用:0次
2022-11-17更新
|
219次组卷
|
2卷引用:山东省聊城市2022-2023学年高一上学期期中教学质量检测化学试题
9 . 用于杀灭新冠病毒的二氧化氯稳定性较差(纯 易分解爆炸),故用
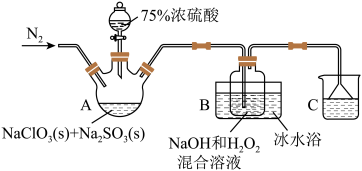
易分解爆炸),故用 和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如下装置(夹持装置略去)及试剂制备
和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如下装置(夹持装置略去)及试剂制备 。
。
已知:① 在碱性环境中发生反应:
在碱性环境中发生反应: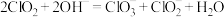
②温度高于60℃时, 分解成
分解成 和NaCl。
和NaCl。
回答下列问题:
(1)配制75%浓硫酸,所需要的仪器是_______ (填序号)。

(2)A为 的发生装置,生成
的发生装置,生成 的离子方程式为
的离子方程式为_______ 。
(3)实验过程中持续通入 的作用是
的作用是_______ 。
(4)装置B中 作
作_______ (填“氧化剂”或“还原剂”);此装置需要采用冰水浴,主要原因是_______ 。
(5)装置C烧杯中的试剂是_______ 。
(6)推测产品中可能含有的杂质为_______ (填化学式)。
 易分解爆炸),故用
易分解爆炸),故用 和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如下装置(夹持装置略去)及试剂制备
和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如下装置(夹持装置略去)及试剂制备 。
。
已知:①
 在碱性环境中发生反应:
在碱性环境中发生反应: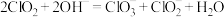
②温度高于60℃时,
 分解成
分解成 和NaCl。
和NaCl。回答下列问题:
(1)配制75%浓硫酸,所需要的仪器是

(2)A为
 的发生装置,生成
的发生装置,生成 的离子方程式为
的离子方程式为(3)实验过程中持续通入
 的作用是
的作用是(4)装置B中
 作
作(5)装置C烧杯中的试剂是
(6)推测产品中可能含有的杂质为
您最近一年使用:0次
10 . 某学习小组探究B及其化合物的性质。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。
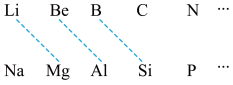
B在元素周期表中的位置是_______ 。其最高价氧化物的化学式为_______ ,与氢氧化钠溶液反应的化学方程式为_______ 。
(2)某科研团队研究发现硼氢化钠( )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
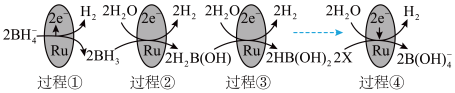
①上图中X的化学式为_______ 。
② 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用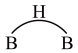 表示,则二聚物结构式为
表示,则二聚物结构式为_______ 。
③图中反应的总化学方程式为_______ 。
④_______ g 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
(1)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。

B在元素周期表中的位置是
(2)某科研团队研究发现硼氢化钠(
 )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
①上图中X的化学式为
②
 以二聚物的形式存在,分子结构中存在两个
以二聚物的形式存在,分子结构中存在两个 键共用一对共用电子的氢桥键,用
键共用一对共用电子的氢桥键,用 表示,则二聚物结构式为
表示,则二聚物结构式为③图中反应的总化学方程式为
④
 的还原能力与标准状况下22.4L
的还原能力与标准状况下22.4L 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
您最近一年使用:0次



