名校
1 . 氧化还原反应与生产、生活密切相关。
(1)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精( 的乙醇溶液)以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备
的乙醇溶液)以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备 有三种常用方法:
有三种常用方法:
a.
b.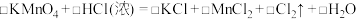
c.
①常温下,医用酒精、 、
、 固体、
固体、 固体、浓盐酸中,能导电的是
固体、浓盐酸中,能导电的是_______________ ,属于电解质的是_______________________ 。
②写出反应c对应的离子方程式:______________ [已知 (浓)可拆分为
(浓)可拆分为 和
和 ]。
]。
③配平反应b的方程式:____________________ 。
④若要制得相同质量的氯气,a、c反应中电子转移的数目之比为__________ 。
(2)法律规定小规模食品生产经营者不得购进、存放、使用亚硝酸盐等易滥用的食品添加剂。实验室中,亚硝酸钠 可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a.
b.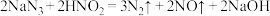
上述两个反应中,属于氧化还原反应的是___________ (填“a”或“b”)。用双线桥法表示该氧化还原反应中电子转移的方向和数目:______________________________________ 。
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中 转化为
转化为 而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于中毒、解毒过程的说法中,正确的是
而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于中毒、解毒过程的说法中,正确的是___________ (填字母)。
a.亚硝酸钠是还原剂 b.维生素C是氧化剂
c.维生素C能把 还原为
还原为 d.亚硝酸钠被还原
d.亚硝酸钠被还原
②含 的废水必须经处理后才能排放,可用铵盐来处理亚硝酸钠,反应生成一种无毒且空气中含量最多的气体,写出该反应的离子方程式:
的废水必须经处理后才能排放,可用铵盐来处理亚硝酸钠,反应生成一种无毒且空气中含量最多的气体,写出该反应的离子方程式:_______________________ 。
(1)为有效防止新冠病毒的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂有双氧水、医用酒精(
 的乙醇溶液)以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备
的乙醇溶液)以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验室制备 有三种常用方法:
有三种常用方法:a.

b.
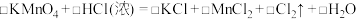
c.

①常温下,医用酒精、
 、
、 固体、
固体、 固体、浓盐酸中,能导电的是
固体、浓盐酸中,能导电的是②写出反应c对应的离子方程式:
 (浓)可拆分为
(浓)可拆分为 和
和 ]。
]。③配平反应b的方程式:
④若要制得相同质量的氯气,a、c反应中电子转移的数目之比为
(2)法律规定小规模食品生产经营者不得购进、存放、使用亚硝酸盐等易滥用的食品添加剂。实验室中,亚硝酸钠
 可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
可用来处理过量的叠氮化钠,有关反应的化学方程式如下:a.

b.
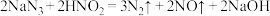
上述两个反应中,属于氧化还原反应的是
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中
 转化为
转化为 而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于中毒、解毒过程的说法中,正确的是
而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于中毒、解毒过程的说法中,正确的是a.亚硝酸钠是还原剂 b.维生素C是氧化剂
c.维生素C能把
 还原为
还原为 d.亚硝酸钠被还原
d.亚硝酸钠被还原②含
 的废水必须经处理后才能排放,可用铵盐来处理亚硝酸钠,反应生成一种无毒且空气中含量最多的气体,写出该反应的离子方程式:
的废水必须经处理后才能排放,可用铵盐来处理亚硝酸钠,反应生成一种无毒且空气中含量最多的气体,写出该反应的离子方程式:
您最近一年使用:0次
名校
2 . 二氧化氯( )消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。
)消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。
(1) 还原法:
还原法: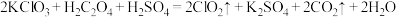 ,请用双线桥表示该反应电子转移的方向和数目
,请用双线桥表示该反应电子转移的方向和数目_______ 。
(2) 还原法:(
还原法:( 和
和 以物质的量之比
以物质的量之比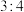 进行反应)
进行反应)
①配平该反应的离子方程式:_______ 。
_______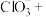 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
②还原产物为_______ 。
(3)盐酸法: ;当
;当 参加反应时,做酸性介质的HCl的物质的量为
参加反应时,做酸性介质的HCl的物质的量为_______ mol。
(4) 自氧化法:
自氧化法: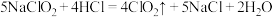 ;该反应中,氧化剂与还原剂的物质的量之比为
;该反应中,氧化剂与还原剂的物质的量之比为_______ ,若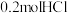 参加反应,则转移的电子数为
参加反应,则转移的电子数为_______ 。
 )消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。
)消毒剂是国际上公认的高效消毒灭菌剂,可以杀灭一切微生物。二氧化氯常温下为黄绿色或枯黄色气体,以下是二氧化氯的几种工业制备方法。(1)
 还原法:
还原法: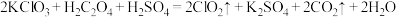 ,请用双线桥表示该反应电子转移的方向和数目
,请用双线桥表示该反应电子转移的方向和数目(2)
 还原法:(
还原法:( 和
和 以物质的量之比
以物质的量之比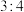 进行反应)
进行反应)①配平该反应的离子方程式:
_______
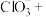 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
②还原产物为
(3)盐酸法:
 ;当
;当 参加反应时,做酸性介质的HCl的物质的量为
参加反应时,做酸性介质的HCl的物质的量为(4)
 自氧化法:
自氧化法: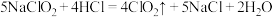 ;该反应中,氧化剂与还原剂的物质的量之比为
;该反应中,氧化剂与还原剂的物质的量之比为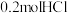 参加反应,则转移的电子数为
参加反应,则转移的电子数为
您最近一年使用:0次
解题方法
3 . N、O、Na、S、Cl的单质及其化合物在工农业生产中用途广泛,回答下列问题:
(1) 是一种淡黄色固体,其与
是一种淡黄色固体,其与 反应的化学方程式为
反应的化学方程式为_______ ,由该反应原理可知 的一种用途为
的一种用途为_______ 。
(2)大苏打( )具有较强的还原性,可用于除去棉织物中残留的氯气。将棉织物浸入水中,加入少量
)具有较强的还原性,可用于除去棉织物中残留的氯气。将棉织物浸入水中,加入少量 充分反应。取少量反应后的浸取液,滴入
充分反应。取少量反应后的浸取液,滴入 溶液,产生白色沉淀,再加入过量稀盐酸,白色沉淀不溶解。
溶液,产生白色沉淀,再加入过量稀盐酸,白色沉淀不溶解。 和
和 的反应中,二者的物质的量之比为
的反应中,二者的物质的量之比为_______ 。
(3)氮化钠(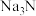 )是一种红色固体,常用作炸药及化学分析试剂。
)是一种红色固体,常用作炸药及化学分析试剂。
①当温度超过150℃时,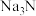 即分解为金属钠和氮气,对应的化学方程式为
即分解为金属钠和氮气,对应的化学方程式为_______ 。
②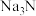 与水反应生成NaOH和一种碱性气体,检验该气体成分的试纸可以为
与水反应生成NaOH和一种碱性气体,检验该气体成分的试纸可以为_______ (填序号)。
A.湿润的淀粉-KI试纸 B.湿润的红色石蕊试纸 C.湿润的酚酞试纸
(4)氯及其化合物是重要的化工原料,在疫情防控、污水处理等方面发挥重要的作用。
①NaClO溶液能有效地灭杀新冠病毒,常用于环境的消毒,工业上制备NaClO溶液的化学方程式为_______ 。
②氨氮废水的处理是当前科学研究的热点问题之一,工业上常用 将酸性氨氮废水中
将酸性氨氮废水中 转化为无毒无害的气体和水,发生反应的离子方程式是
转化为无毒无害的气体和水,发生反应的离子方程式是_______ 。
(1)
 是一种淡黄色固体,其与
是一种淡黄色固体,其与 反应的化学方程式为
反应的化学方程式为 的一种用途为
的一种用途为(2)大苏打(
 )具有较强的还原性,可用于除去棉织物中残留的氯气。将棉织物浸入水中,加入少量
)具有较强的还原性,可用于除去棉织物中残留的氯气。将棉织物浸入水中,加入少量 充分反应。取少量反应后的浸取液,滴入
充分反应。取少量反应后的浸取液,滴入 溶液,产生白色沉淀,再加入过量稀盐酸,白色沉淀不溶解。
溶液,产生白色沉淀,再加入过量稀盐酸,白色沉淀不溶解。 和
和 的反应中,二者的物质的量之比为
的反应中,二者的物质的量之比为(3)氮化钠(
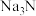 )是一种红色固体,常用作炸药及化学分析试剂。
)是一种红色固体,常用作炸药及化学分析试剂。①当温度超过150℃时,
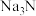 即分解为金属钠和氮气,对应的化学方程式为
即分解为金属钠和氮气,对应的化学方程式为②
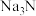 与水反应生成NaOH和一种碱性气体,检验该气体成分的试纸可以为
与水反应生成NaOH和一种碱性气体,检验该气体成分的试纸可以为A.湿润的淀粉-KI试纸 B.湿润的红色石蕊试纸 C.湿润的酚酞试纸
(4)氯及其化合物是重要的化工原料,在疫情防控、污水处理等方面发挥重要的作用。
①NaClO溶液能有效地灭杀新冠病毒,常用于环境的消毒,工业上制备NaClO溶液的化学方程式为
②氨氮废水的处理是当前科学研究的热点问题之一,工业上常用
 将酸性氨氮废水中
将酸性氨氮废水中 转化为无毒无害的气体和水,发生反应的离子方程式是
转化为无毒无害的气体和水,发生反应的离子方程式是
您最近一年使用:0次
名校
解题方法
4 . 硝酸是用途广泛的重要化工原料,自然乳和化工生产中合成硝酸各物质转化关系如下图所示,请结合你所学的知识回答以下问题:
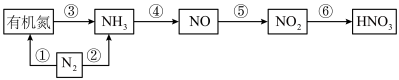
(1)上图①~⑥各步转化中,属于氮的固定的是_______ (填序号);
(2)氨的催化氧化是工业合成硝酸的重要步骤,其化学方程式为_______ 其中氧化剂与还原剂物质的量之比为_______ ;
(3)为提高NO→ 的转化率,可采取的措施是
的转化率,可采取的措施是_______ ;
(4)工业制硝酸时含有NO、 等大气污染物,可用尿素[CO(NH2)2]水溶液吸收氮氧化物,用尿素[CO(NH2)2]水溶液吸收体积比为1∶1的NO和
等大气污染物,可用尿素[CO(NH2)2]水溶液吸收氮氧化物,用尿素[CO(NH2)2]水溶液吸收体积比为1∶1的NO和 混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式为
混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式为_______ ;

(1)上图①~⑥各步转化中,属于氮的固定的是
(2)氨的催化氧化是工业合成硝酸的重要步骤,其化学方程式为
(3)为提高NO→
 的转化率,可采取的措施是
的转化率,可采取的措施是(4)工业制硝酸时含有NO、
 等大气污染物,可用尿素[CO(NH2)2]水溶液吸收氮氧化物,用尿素[CO(NH2)2]水溶液吸收体积比为1∶1的NO和
等大气污染物,可用尿素[CO(NH2)2]水溶液吸收氮氧化物,用尿素[CO(NH2)2]水溶液吸收体积比为1∶1的NO和 混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式为
混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式为
您最近一年使用:0次
5 . 国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,75%酒精、含氯消毒剂、过氧乙酸等可有效灭活病毒。回答下列问题:
(1) 是最早用于你用水消毒的物质,主要是利用
是最早用于你用水消毒的物质,主要是利用 溶于水生成的次氯酸灭活病毒。
溶于水生成的次氯酸灭活病毒。 与水反应的离子方程式为
与水反应的离子方程式为_______ 。氯水经光照后酸性增强,用化学方程式表示其原因为_______ 。
(2)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8g 中阴离子的物质的量为
中阴离子的物质的量为_______ ,当它与 完全反应时,转移的电子数目为
完全反应时,转移的电子数目为_______ 。
(3) 可用于杀菌、消毒。葡萄酒里含有微量
可用于杀菌、消毒。葡萄酒里含有微量 ,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了
,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了 的
的_______ 性。氯水和 都有漂白性,有人为了增强漂白效果,将
都有漂白性,有人为了增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为
混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为_______ 。
(1)
 是最早用于你用水消毒的物质,主要是利用
是最早用于你用水消毒的物质,主要是利用 溶于水生成的次氯酸灭活病毒。
溶于水生成的次氯酸灭活病毒。 与水反应的离子方程式为
与水反应的离子方程式为(2)过氧乙酸、过氧化氢和过氧化钠均有强氧化性,可用作杀菌剂、消毒剂、漂白剂和供氧剂等。7.8g
 中阴离子的物质的量为
中阴离子的物质的量为 完全反应时,转移的电子数目为
完全反应时,转移的电子数目为(3)
 可用于杀菌、消毒。葡萄酒里含有微量
可用于杀菌、消毒。葡萄酒里含有微量 ,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了
,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了 的
的 都有漂白性,有人为了增强漂白效果,将
都有漂白性,有人为了增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为
混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因为
您最近一年使用:0次
6 .  具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。
(1)实验室检验 的方法为
的方法为_______ 。 溶液对钢铁设备的腐蚀,除
溶液对钢铁设备的腐蚀,除 的腐蚀作用外,另一离子的腐蚀主要原因是
的腐蚀作用外,另一离子的腐蚀主要原因是_______ (用离子方程式表示)
(2)实验室可用NaClO氧化酸性 废液得到
废液得到 ,发生反应的离子方程式为
,发生反应的离子方程式为_______ 。若要制取1000mL2mol/L ,则需要NaClO的质量为
,则需要NaClO的质量为_______ g。
(3)通过控制条件, 溶液的水解产物聚合,生成聚合氯化铁,离子方程式为
溶液的水解产物聚合,生成聚合氯化铁,离子方程式为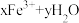
 。欲使平衡正向移动可采用的方法是_______(填字母)。
。欲使平衡正向移动可采用的方法是_______(填字母)。
(4)工业上可用废铁屑来制备 ,流程如下:
,流程如下:
废铁屑
 晶体
晶体 无水
无水
①在HCl气流中加热的原因是_______ 。
②若某废铁屑中铁的质量分数为84%,用1000g废铁屑反应,最后制取的 质量为1625g,则该制取过程中的产率为
质量为1625g,则该制取过程中的产率为_______ (精确到0.1%)
 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比
具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。(1)实验室检验
 的方法为
的方法为 溶液对钢铁设备的腐蚀,除
溶液对钢铁设备的腐蚀,除 的腐蚀作用外,另一离子的腐蚀主要原因是
的腐蚀作用外,另一离子的腐蚀主要原因是(2)实验室可用NaClO氧化酸性
 废液得到
废液得到 ,发生反应的离子方程式为
,发生反应的离子方程式为 ,则需要NaClO的质量为
,则需要NaClO的质量为(3)通过控制条件,
 溶液的水解产物聚合,生成聚合氯化铁,离子方程式为
溶液的水解产物聚合,生成聚合氯化铁,离子方程式为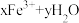
 。欲使平衡正向移动可采用的方法是_______(填字母)。
。欲使平衡正向移动可采用的方法是_______(填字母)。| A.降温 | B.加水稀释 | C.加入 | D.加入 |
 ,流程如下:
,流程如下:废铁屑

 晶体
晶体 无水
无水
①在HCl气流中加热的原因是
②若某废铁屑中铁的质量分数为84%,用1000g废铁屑反应,最后制取的
 质量为1625g,则该制取过程中的产率为
质量为1625g,则该制取过程中的产率为
您最近一年使用:0次
7 . 把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:______________ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式:_____________________ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中(用化学式表示,下同),还原产物为
②配平该反应的方程式:
您最近一年使用:0次
8 . 根据所学知识回答问题
(1)___________ molH2O中所含有的氧原子数与1.5 molCO2的氧原子数相同。
(2)质量为9.8g的H2SO4物质的量是___________ 。
(3)1.204×1024个H2的物质的量是___________ 。
(4)配制溶液时,称量5.85gNaCl固体,配制480mL溶液,则溶液物质的量浓度是___________ mol/L。
(5)标准状况下16gH2的体积是___________ L。
(6)100mL0.2mol·L-1的Na2SO4溶液中,取出10mL该溶液,c(Na+)=___________ ,将该10mL溶液加水稀释至100mL,则c( )=
)=___________ 。
(7) 的中子数是
的中子数是___________ 。
(8)写出方程式的系数____NaClO+___NaI=____NaIO3+____NaCl___________
(1)
(2)质量为9.8g的H2SO4物质的量是
(3)1.204×1024个H2的物质的量是
(4)配制溶液时,称量5.85gNaCl固体,配制480mL溶液,则溶液物质的量浓度是
(5)标准状况下16gH2的体积是
(6)100mL0.2mol·L-1的Na2SO4溶液中,取出10mL该溶液,c(Na+)=
 )=
)=(7)
 的中子数是
的中子数是(8)写出方程式的系数____NaClO+___NaI=____NaIO3+____NaCl
您最近一年使用:0次
9 . ClO2是一种消毒杀菌效率高、污染少的绿色消毒剂。可以通过下列两种途径得到:
方法一:
方法二:
(1)用双线桥法表示方法一反应中电子转移的方向和数目。____________________
(2)方法一中浓盐酸在反应中显示出来的性质是__________(填字母)。
(3)配平方法二中的化学方程式。______________________________________
(4)方法二中的氧化剂为__________ (填化学式),在反应中发生______________ (填“氧化”或“还原”)反应。还原产物为_________ (填化学式)。
(5)上述反应为氧化还原反应,氧化还原反应原理在生活中广泛应用。下列物质的用途中,利用了氧化还原反应原理的是______________(填字母)。
方法一:

方法二:

(1)用双线桥法表示方法一反应中电子转移的方向和数目。
(2)方法一中浓盐酸在反应中显示出来的性质是__________(填字母)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(4)方法二中的氧化剂为
(5)上述反应为氧化还原反应,氧化还原反应原理在生活中广泛应用。下列物质的用途中,利用了氧化还原反应原理的是______________(填字母)。
| A.用盐酸除铁锈 | B.用赤铁矿炼铁 |
| C.生石灰作食品干燥剂 | D.用熟石灰改良酸性土壤 |
您最近一年使用:0次
10 . 完成下列问题
(1)某同学设计如下实验研究 的性质:
的性质:
①从理论上看 既有氧化性又有还原性的原因是
既有氧化性又有还原性的原因是_______ 。
②能证明 具有还原性的实验是
具有还原性的实验是_______ (填序号)。可作为证据的实验现象是_______ (填字母序号)。
③配平方程式:______
_______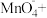 ______
______ _______
_______ _______
_______ _______
_______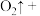 _______
_______
(2)某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生过程:
只发生过程: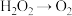 。该反应中,发生还原反应的过程是:
。该反应中,发生还原反应的过程是:_______ →_______ 。
(3)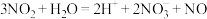 用单线桥表示反应电子转移方向和数目
用单线桥表示反应电子转移方向和数目_______ 。
(1)某同学设计如下实验研究
 的性质:
的性质:| 序号 | 实验 | 实验现象 |
| ⅰ | 向5% 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色褪去 b.有大量气泡产生 |
| ⅱ | 向5% 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 既有氧化性又有还原性的原因是
既有氧化性又有还原性的原因是②能证明
 具有还原性的实验是
具有还原性的实验是③配平方程式:
_______
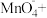 ______
______ _______
_______ _______
_______ _______
_______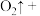 _______
_______
(2)某一反应体系有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生过程:
只发生过程: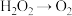 。该反应中,发生还原反应的过程是:
。该反应中,发生还原反应的过程是:(3)
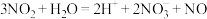 用单线桥表示反应电子转移方向和数目
用单线桥表示反应电子转移方向和数目
您最近一年使用:0次



