1 . 回答下列问题。
I.智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O。
(1)反应中___________ 元素被氧化,___________ (填化学式)是氧化剂。
(2)用单线桥标出电子转移方向和数目___________ 。
(3)反应产物中,所得氧化产物与还原产物微粒个数之比为___________ 。
Ⅱ.有一种“地康法”制取氯气的反应原理如图所示:
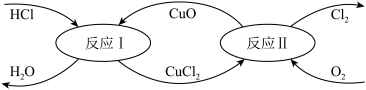
(4)反应Ⅱ的化学方程式为___________ 。
(5)在肉制品加工中,使用发色剂-亚硝酸钠时必须严格控制用量,确保使用安全。某一反应体系中反应物和生成物共有六种:NaNO2、H2O、NO、I2、NaI、HI。已知该反应中NaNO2只发生了如下过程:NaNO2→NO;写出该反应的化学方程式___________ 。
(6)ClO2是一种黄绿色的气体。铬(Cr)的一种固体氧化物Cr2O3与KClO3固体在高温条件下反应,只生成ClO2、Cl2和铬酸钾(K2CrO4)固体三种产物。若该反应中转移24mol电子,生成气体共___________ mol。
I.智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式为:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O。
(1)反应中
(2)用单线桥标出电子转移方向和数目
(3)反应产物中,所得氧化产物与还原产物微粒个数之比为
Ⅱ.有一种“地康法”制取氯气的反应原理如图所示:

(4)反应Ⅱ的化学方程式为
(5)在肉制品加工中,使用发色剂-亚硝酸钠时必须严格控制用量,确保使用安全。某一反应体系中反应物和生成物共有六种:NaNO2、H2O、NO、I2、NaI、HI。已知该反应中NaNO2只发生了如下过程:NaNO2→NO;写出该反应的化学方程式
(6)ClO2是一种黄绿色的气体。铬(Cr)的一种固体氧化物Cr2O3与KClO3固体在高温条件下反应,只生成ClO2、Cl2和铬酸钾(K2CrO4)固体三种产物。若该反应中转移24mol电子,生成气体共
您最近一年使用:0次
名校
解题方法
2 . 二氧化硫的污染治理是化学研究的重要课题。
(1)石灰石-石膏法是一种常见的“钙基固硫”方法。其中,石灰石的溶解率与脱硫效果有着密切的关系。
可将催化条件下CaCO3吸收SO2宏观反应分为三步:
i.CaCO3由固相溶解进入液相,溶解速率为RA;
ii.SO2由气相扩散进入液相,扩散速率为RB;
iii.在催化剂作用下,溶解的SO2和Ca2+发生化学反应,且反应在液相中进行,反应速率为RC。温度变化对总反应速率的影响如图所示。___________ (填“RA”、“RB”或“Rc”)控制。
②45~55℃(催化剂活性不变)曲线呈下降趋势的原因:一是二氧化硫溶解度随温度升高而降低;二是___________ 。
(2)利用MnO2与SO2反应既可消除污染又可以制备MnSO4,将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c( )随反应时间的变化如图所示。导致溶液中c(Mn2+)和c(
)随反应时间的变化如图所示。导致溶液中c(Mn2+)和c( )的变化产生明显差异的原因是:
)的变化产生明显差异的原因是:_______ 。 与NO2反应的离子方程式为
与NO2反应的离子方程式为___________ 。
②请描述水催化促进硫酸盐形成的化学机制:通过“水分子桥”,处于纳米液滴中的 或
或 可以将电子快速转移给周围的气相NO2分子,
可以将电子快速转移给周围的气相NO2分子,___________ 。
(1)石灰石-石膏法是一种常见的“钙基固硫”方法。其中,石灰石的溶解率与脱硫效果有着密切的关系。
可将催化条件下CaCO3吸收SO2宏观反应分为三步:
i.CaCO3由固相溶解进入液相,溶解速率为RA;
ii.SO2由气相扩散进入液相,扩散速率为RB;
iii.在催化剂作用下,溶解的SO2和Ca2+发生化学反应,且反应在液相中进行,反应速率为RC。温度变化对总反应速率的影响如图所示。
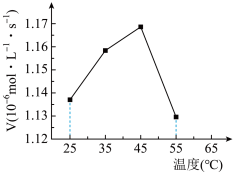
②45~55℃(催化剂活性不变)曲线呈下降趋势的原因:一是二氧化硫溶解度随温度升高而降低;二是
(2)利用MnO2与SO2反应既可消除污染又可以制备MnSO4,将含有SO2尾气和一定比例的空气通入MnO2悬浊液中,保持温度不变的情况下,测得溶液中c(Mn2+)和c(
 )随反应时间的变化如图所示。导致溶液中c(Mn2+)和c(
)随反应时间的变化如图所示。导致溶液中c(Mn2+)和c( )的变化产生明显差异的原因是:
)的变化产生明显差异的原因是: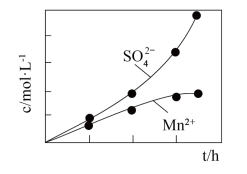
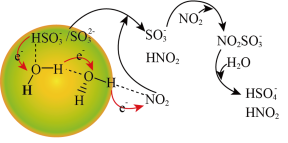
 与NO2反应的离子方程式为
与NO2反应的离子方程式为②请描述水催化促进硫酸盐形成的化学机制:通过“水分子桥”,处于纳米液滴中的
 或
或 可以将电子快速转移给周围的气相NO2分子,
可以将电子快速转移给周围的气相NO2分子,
您最近一年使用:0次
2023-12-25更新
|
308次组卷
|
5卷引用:江苏省丹阳高级中学2023届高三上学期第一次阶段考试化学试题
江苏省丹阳高级中学2023届高三上学期第一次阶段考试化学试题江苏省南师附中、天一中学、海安中学、海门中学四校2021-2022学年高三12月联考化学试题江苏省建湖高级中学2023-2024学年高三上学期暑期学情检测(一)化学试题江苏省如皋中学2023-2024学年高三上学期阶段考试(二) 化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
解题方法
3 . 利用分类和氧化还原反应的知识能实现物质的转化。
(1)请从下列试剂中选择合适的完成指定转化。
试剂:C、CO2、Na2CO3溶液、K2SO4溶液、盐酸。
①K2O(一种碱性氧化物)→K2CO3的化学方程式:___________ ;
②Na3PO4→H3PO4的离子方程式:___________ ;
③浓硫酸→SO2的化学方程式:___________ 。
(2)以石灰渣[主要成分是Ca(OH)2]为原料生产氯酸钾的流程如下:
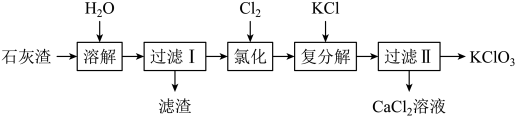
①氯化反应的温度为60℃,产物中的含氯化合物是CaCl2和Ca(ClO3)2,写出氯化反应的化学方程式:___________ ;
②写出复分解反应的化学方程式:___________ 。
(1)请从下列试剂中选择合适的完成指定转化。
试剂:C、CO2、Na2CO3溶液、K2SO4溶液、盐酸。
①K2O(一种碱性氧化物)→K2CO3的化学方程式:
②Na3PO4→H3PO4的离子方程式:
③浓硫酸→SO2的化学方程式:
(2)以石灰渣[主要成分是Ca(OH)2]为原料生产氯酸钾的流程如下:

①氯化反应的温度为60℃,产物中的含氯化合物是CaCl2和Ca(ClO3)2,写出氯化反应的化学方程式:
②写出复分解反应的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。下列反应可制得ClO2:NaClO3+ H2O2+ H2SO4→ClO2↑+Na2SO4+O2↑+H2O(未配平)
(1)反应中被氧化的元素是________ ,每生成2a个ClO2时有______ 个电子转移。
(2)写出配平后的方程式:___________ ,并用双线桥表示电子转移的方向和数目。
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:_____________________ 。
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(1)反应中被氧化的元素是
(2)写出配平后的方程式:
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将
 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
5 . 利用纳米铁粉及生物技术除去废水中的氮是当今环保领域重要的研究课题。
Ⅰ.纳米铁粉可用于去除废水中的硝态氮(以NO 表示),反应原理如图1所示。
表示),反应原理如图1所示。

(1)液相还原法制备纳米铁粉:采用硼氢化物如KBH4、NaBH4等与铁离子(Fe2+、Fe3+)混合反应。NaBH4(B为+3价,pH=8.6)溶液还原Fe2+,除生成等物质的量的纳米铁粉和一种气体外,还生成B(OH)3。写出该反应的离子方程式___________ 。
(2)有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除。其原因是___________ 。
(3)利用纳米铁粉与活性炭可提升硝态废水中硝态氮的去除效率。控制纳米铁粉与活性炭总质量一定,反应时间相同,测得废水中硝态氮残留率与混合物中 的关系如图2所示,
的关系如图2所示, 过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2,硝态氮残留率呈现如此变化的原因是
过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2,硝态氮残留率呈现如此变化的原因是___________ 。

Ⅱ.Fe2+能提高厌氧氨氧化菌生物活性,加快生物转化硝态氮生成氮气的速率。某科研小组利用厌氧氨氧化菌与纳米铁粉相结合的方法去除废水中的硝态氮。
(4)保持其他条件相同,在不同的温度下进行脱硝,测定废水中硝态氮的去除率与含氮产物的产率如图3所示。与60℃相比,80℃时产物产率变化的原因是___________ 。

(5)厌氧氨氧化菌将NO 转化为N2的可能机理如图4所示,其中虚线框中物质转化过程可描述为
转化为N2的可能机理如图4所示,其中虚线框中物质转化过程可描述为___________ 。

Ⅰ.纳米铁粉可用于去除废水中的硝态氮(以NO
 表示),反应原理如图1所示。
表示),反应原理如图1所示。
(1)液相还原法制备纳米铁粉:采用硼氢化物如KBH4、NaBH4等与铁离子(Fe2+、Fe3+)混合反应。NaBH4(B为+3价,pH=8.6)溶液还原Fe2+,除生成等物质的量的纳米铁粉和一种气体外,还生成B(OH)3。写出该反应的离子方程式
(2)有研究发现,在铁粉总量一定的条件下,水中的溶解氧过多不利于硝态氮去除。其原因是
(3)利用纳米铁粉与活性炭可提升硝态废水中硝态氮的去除效率。控制纳米铁粉与活性炭总质量一定,反应时间相同,测得废水中硝态氮残留率与混合物中
 的关系如图2所示,
的关系如图2所示, 过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2,硝态氮残留率呈现如此变化的原因是
过大和过小都会导致硝态氮残留率上升,但方向1上升幅度小于方向2,硝态氮残留率呈现如此变化的原因是
Ⅱ.Fe2+能提高厌氧氨氧化菌生物活性,加快生物转化硝态氮生成氮气的速率。某科研小组利用厌氧氨氧化菌与纳米铁粉相结合的方法去除废水中的硝态氮。
(4)保持其他条件相同,在不同的温度下进行脱硝,测定废水中硝态氮的去除率与含氮产物的产率如图3所示。与60℃相比,80℃时产物产率变化的原因是

(5)厌氧氨氧化菌将NO
 转化为N2的可能机理如图4所示,其中虚线框中物质转化过程可描述为
转化为N2的可能机理如图4所示,其中虚线框中物质转化过程可描述为
您最近一年使用:0次
6 . 二氧化氯消毒剂是国际公认的高效消毒灭菌剂。
(1)制备 的一种反应为:
的一种反应为: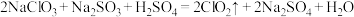 ,用双线桥法标出其电子转移的方向和数目
,用双线桥法标出其电子转移的方向和数目_______ 。
(2)实验室可用亚氯酸钠 溶液与氯气反应制
溶液与氯气反应制 ,此反应的化学方程式为
,此反应的化学方程式为_______ 。
(3) 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是_______ 。
(4) 可经过题图所示的转化制取
可经过题图所示的转化制取 。已知“反应II”为复分解反应。
。已知“反应II”为复分解反应。

①“反应I”的离子方程式为_______ 。
②过滤之后是洗涤,判断 沉淀是否洗涤干净的方法是
沉淀是否洗涤干净的方法是_______ 。
(5)一种“二氧化氯泡腾片”有效成分为 、
、 、
、 ,该泡腾片能快速溶于水,产生大量气泡,得到
,该泡腾片能快速溶于水,产生大量气泡,得到 溶液。取某品牌泡腾片1片溶于水配成
溶液。取某品牌泡腾片1片溶于水配成 溶液,为测定溶液中
溶液,为测定溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:
①取该溶液 ,加入锥形瓶中,用稀硫酸调节溶液
,加入锥形瓶中,用稀硫酸调节溶液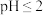 ,再加入足量
,再加入足量 晶体,发生反应:
晶体,发生反应: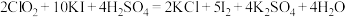
②用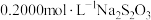 溶液和生成的碘单质反应,化学方程式如下:
溶液和生成的碘单质反应,化学方程式如下: ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液
溶液 。
。
则配成的 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为_______ 。(写出计算过程)
(1)制备
 的一种反应为:
的一种反应为: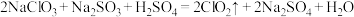 ,用双线桥法标出其电子转移的方向和数目
,用双线桥法标出其电子转移的方向和数目(2)实验室可用亚氯酸钠
 溶液与氯气反应制
溶液与氯气反应制 ,此反应的化学方程式为
,此反应的化学方程式为(3)
 可将废水中的
可将废水中的 转化为
转化为 而除去,本身被还原为
而除去,本身被还原为 ,该反应中氧化剂与还原剂的物质的量之比是
,该反应中氧化剂与还原剂的物质的量之比是(4)
 可经过题图所示的转化制取
可经过题图所示的转化制取 。已知“反应II”为复分解反应。
。已知“反应II”为复分解反应。
①“反应I”的离子方程式为
②过滤之后是洗涤,判断
 沉淀是否洗涤干净的方法是
沉淀是否洗涤干净的方法是(5)一种“二氧化氯泡腾片”有效成分为
 、
、 、
、 ,该泡腾片能快速溶于水,产生大量气泡,得到
,该泡腾片能快速溶于水,产生大量气泡,得到 溶液。取某品牌泡腾片1片溶于水配成
溶液。取某品牌泡腾片1片溶于水配成 溶液,为测定溶液中
溶液,为测定溶液中 的含量,进行了下列实验:
的含量,进行了下列实验:①取该溶液
 ,加入锥形瓶中,用稀硫酸调节溶液
,加入锥形瓶中,用稀硫酸调节溶液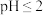 ,再加入足量
,再加入足量 晶体,发生反应:
晶体,发生反应: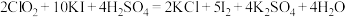
②用
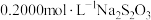 溶液和生成的碘单质反应,化学方程式如下:
溶液和生成的碘单质反应,化学方程式如下: ,恰好完全反应时消耗
,恰好完全反应时消耗 溶液
溶液 。
。则配成的
 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
7 . 氢化钠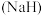 广泛应用于工业生产。
广泛应用于工业生产。
(1)氢化钠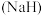 中氢元素的化合价为
中氢元素的化合价为_______ 。
(2) 能与水剧烈反应:
能与水剧烈反应: ,该反应中的氧化剂是
,该反应中的氧化剂是_______ ,氧化剂与还原剂的物质的量之比是_______ 。
(3)在高温下氢化钠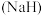 可将四氯化钛
可将四氯化钛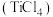 还原成金属钛,该反应的化学方程式为
还原成金属钛,该反应的化学方程式为_______ 。
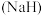 广泛应用于工业生产。
广泛应用于工业生产。(1)氢化钠
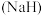 中氢元素的化合价为
中氢元素的化合价为(2)
 能与水剧烈反应:
能与水剧烈反应: ,该反应中的氧化剂是
,该反应中的氧化剂是(3)在高温下氢化钠
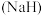 可将四氯化钛
可将四氯化钛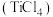 还原成金属钛,该反应的化学方程式为
还原成金属钛,该反应的化学方程式为
您最近一年使用:0次
2023-02-08更新
|
56次组卷
|
2卷引用:江苏省淮安市淮阴区2022-2023学年高二上学期11月期中化学试题
名校
解题方法
8 . 根据信息书写反应方程式;
现代工业上用氧化锌烟灰(主要成分为ZnO,含少量Pb、CuO和As2O3)制取高纯锌的部分工艺流程如图所示。

(1)已知:“溶浸”后浸出液中含 、
、 、
、 等。写出该过程中生成
等。写出该过程中生成 的相关离子方程式:
的相关离子方程式:___________ 。
(2)“氧化除杂”的目的是将“ ”转化为As2O5胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:
”转化为As2O5胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:___________ 。
现代工业上用氧化锌烟灰(主要成分为ZnO,含少量Pb、CuO和As2O3)制取高纯锌的部分工艺流程如图所示。

(1)已知:“溶浸”后浸出液中含
 、
、 、
、 等。写出该过程中生成
等。写出该过程中生成 的相关离子方程式:
的相关离子方程式:(2)“氧化除杂”的目的是将“
 ”转化为As2O5胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:
”转化为As2O5胶体,再经吸附聚沉除去。写出氧化反应的离子方程式:
您最近一年使用:0次
解题方法
9 . 海水是巨大的资源宝库,可以进行综合利用。从海水中提取淡水、食盐和溴的过程如图:
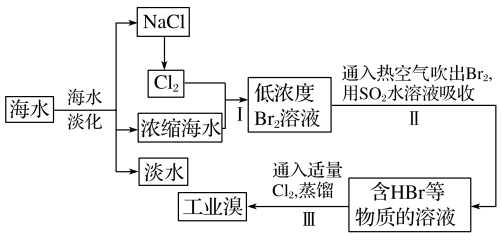
(1)步骤II用SO2水溶液吸收Br2,反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr。在该反应中,氧化剂是_______ (填化学式);若反应中生成2molHBr,则消耗_______ molSO2。
(2)根据上述反应可判断出SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是_______ 。
(3)写出步骤III的化学方程式:_______ 。

(1)步骤II用SO2水溶液吸收Br2,反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr。在该反应中,氧化剂是
(2)根据上述反应可判断出SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)写出步骤III的化学方程式:
您最近一年使用:0次
名校
解题方法
10 .  是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:
是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:

(1)写出“反应”步骤中生成 的化学方程式:
的化学方程式:_______ 。
(2)“尾气吸收”是吸收“电解”过程排出的少量 。写出“尾气吸收”的化学方程式:
。写出“尾气吸收”的化学方程式:_______ 。此吸收反应中,氧化剂与还原剂的物质的量之比为_______ 。
 是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:
是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:
(1)写出“反应”步骤中生成
 的化学方程式:
的化学方程式:(2)“尾气吸收”是吸收“电解”过程排出的少量
 。写出“尾气吸收”的化学方程式:
。写出“尾气吸收”的化学方程式:
您最近一年使用:0次



